Remove ads
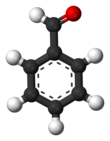
벤즈알데하이드(Benzaldehyde, C7H6O)는 가장 간단한 방향족 알데하이드다. 고편도유의 성분 중 하나이다.
| |||
| 이름 | |||
|---|---|---|---|
| 우선명 (PIN)
Benzaldehyde[1] | |||
| 체계명
Benzenecarbaldehyde | |||
| 별칭
Benzenecarboxaldehyde Phenylmethanal Benzoic aldehyde | |||
| 식별자 | |||
3D 모델 (JSmol) |
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.002.601 | ||
| EC 번호 |
| ||
| KEGG | |||
PubChem CID |
|||
| RTECS 번호 |
| ||
| UNII | |||
| UN 번호 | 1990 | ||
CompTox Dashboard (EPA) |
|||
| |||
| |||
| 성질 | |||
| C7H6O | |||
| 몰 질량 | 106.124 g·mol−1 | ||
| 겉보기 | colorless liquid strongly refractive | ||
| 냄새 | almond-like | ||
| 밀도 | 1.044 g/mL, liquid | ||
| 녹는점 | −57.12[2] °C (−70.82 °F; 216.03 K) | ||
| 끓는점 | 178.1 °C (352.6 °F; 451.2 K) | ||
| 6.95 g/L (25 °C)[3] | |||
| log P | 1.64[4] | ||
자화율 (χ) |
-60.78·10−6 cm3/mol | ||
굴절률 (nD) |
1.5456 | ||
| 점도 | 1.321 cP (25 °C) | ||
| 열화학 | |||
표준 생성 엔탈피 (ΔfH⦵298) |
−36.8 kJ/mol | ||
표준 연소 엔탈피 (ΔcH⦵298) |
−3525.1 kJ/mol | ||
| 위험 | |||
| 물질 안전 보건 자료 | J. T. Baker | ||
| GHS 그림문자 |  | ||
| 신호어 | 경고 | ||
GHS 유해위험문구 |
H302 | ||
GHS 예방조치문구 |
P264, P270, P301+312, P330, P501 | ||
| NFPA 704 (파이어 다이아몬드) | |||
| 인화점 | 64 °C (147 °F; 337 K) | ||
| 192 °C (378 °F; 465 K) | |||
| 폭발 한계 | 1.4–8.5% | ||
| 반수 치사량 또는 반수 치사농도 (LD, LC): | |||
LD50 (median dose) |
1300 mg/kg (rat, oral) | ||
| 관련 화합물 | |||
관련 화합물 |
Benzyl alcohol Benzoic acid | ||
Remove ads
벤즈알데하이드는 아몬드와 살구, 체리씨 등에 함유되어 있는 아미그달린을 통하여 얻어진다. 아미그달린은 효소 작용을 통해 벤즈알데하이드와 사이안화 수소, 글루코스로 분해된다.
벤즈알데하이드는 공기중에서 산화되어 벤조산으로 바뀌며, 수소첨가반응을 통해 벤질알코올이 생성되기도 한다. 무수(無水) 상태의 아세트산나트륨이나 아세트산무수물과 반응할 시 신남산(계피산)이 발생하는 것으로 알려져 있다.
70kg의 건장한 성인 남성을 기준으로 벤즈알데하이드의 치사량은 약 50 mL이며 미국 환경보호국에 의해 유해 물질로 지정되어 있다. 물론 각종 식품에 벤즈알데하이드가 향 첨가를 목적으로 쓰이지만, 소량 섭취는 거의 안전하다.
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.
Remove ads