
L-글루코스
화합물 / From Wikipedia, the free encyclopedia
L-글루코스(영어: L-glucose) 또는 L-포도당(L-葡萄糖)은 화학식이 C6H12O6 또는 O=CH[CH(OH)]5H인 유기 화합물로, 특히 알도헥소스 단당류 중 하나이다. 포도당의 L-이성질체로, 보다 더 일반적인 D-포도당의 거울상 이성질체이다.
간략 정보 이름, 식별자 ...
 | |
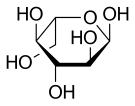 α-L-글루코피라노스의 하워스 투영식 | |
| 이름 | |
|---|---|
| IUPAC 이름
L-glucose | |
| 식별자 | |
| |
3D 모델 (JSmol) |
|
| 약어 | L-Glc |
| ChEBI | |
| ChemSpider |
|
| EC 번호 |
|
PubChem CID |
|
| UNII | |
| |
| |
| 성질 | |
| C6H12O6 | |
| 몰 질량 | 180.156 g·mol−1 |
| 밀도 | 1.54 g/cm3 |
| 91 g/100 mL | |
| 위험 | |
| 물질 안전 보건 자료 | ICSC 0865 |
닫기
L-포도당은 살아 있는 생물체에서는 자연적으로 생성되지 않지만 실험실에서 합성될 수 있다. L-포도당은 D-포도당과 맛으로 구별되지 않지만,[1] 해당과정의 첫 번째 효소인 헥소키네이스에 의해 인산화될 수 없기 때문에 살아 있는 생물체에서 에너지원으로 사용될 수 없다. 알려진 예외 중 하나는 L-포도당을 산화시킬 수 있는 효소인 D-트레오-알도스 1-탈수소효소를 포함하고 있는 식물성 병원성 세균인 버크홀데리아 카리오필리(Burkholderia caryophylli)이다.[2]
D-포도당과 마찬가지로 L-포도당은 일반적으로 4가지 고리 구조의 이성질체(α-L-글루코피라노스 및 β-L-글루코피라노스(가장 일반적으며, 6원자 고리 포함), α-L-글루코푸라노스 및 β-L-글루코푸라노스(5원자 고리 포함) 중 하나로 존재한다. 수용액에서 이들 이성질체는 중간생성물 단계인 열린 사슬 형태를 거쳐 몇 시간 내에 상호전환이 가능하다.