
육플루오린화 황
From Wikipedia, the free encyclopedia
육플루오린화 황(육불화황)(화학식: SF6)은 플루오린과 황의 화합물로, 황 원자를 중심으로 플루오린 원자가 정팔면체 구조를 취하고 있다.
간략 정보 이름, 식별자 ...
| |||
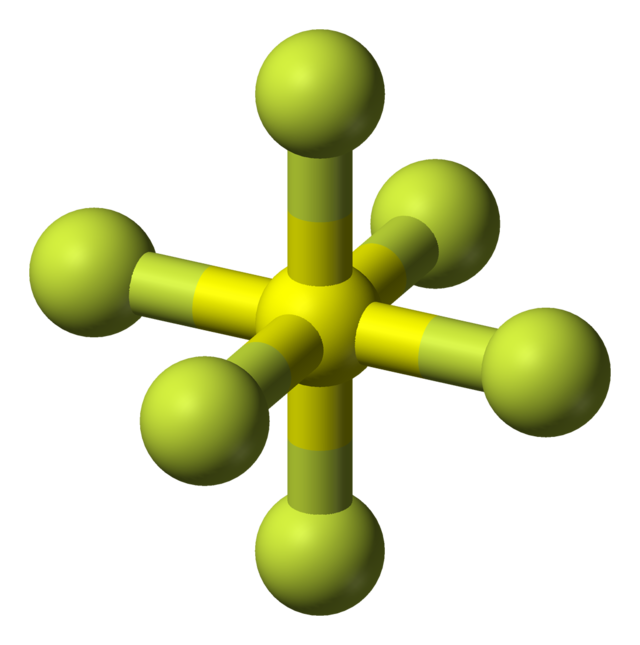 | |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름
Sulfur hexafluoride | |||
| 체계명
Hexafluoro-λ6-sulfane[1] | |||
| 별칭
Elagas Esaflon | |||
| 식별자 | |||
3D 모델 (JSmol) |
|||
| ChEBI | |||
| ChemSpider |
| ||
| ECHA InfoCard | 100.018.050 | ||
| EC 번호 |
| ||
| 2752 | |||
| KEGG |
| ||
| MeSH | Sulfur+hexafluoride | ||
PubChem CID |
|||
| RTECS 번호 |
| ||
| UNII |
| ||
| UN 번호 | 1080 | ||
CompTox Dashboard (EPA) |
|||
| |||
| |||
| 성질 | |||
| SF6 | |||
| 몰 질량 | 146.06 g/mol | ||
| 겉보기 | 무색 기체 | ||
| 냄새 | odorless[2] | ||
| 밀도 | 6.17 g/L | ||
| 녹는점 | −64 °C; −83 °F; 209 K | ||
| 끓는점 | −50.8 °C (−59.4 °F; 222.3 K) | ||
| 임계점 (T, P) | 45.51±0.1 °C, 3.749±0.01 MPa[3] | ||
| 0.003% (25 °C)[2] | |||
| 용해도 | slightly soluble in water, very soluble in 에탄올, 헥세인, 벤젠 | ||
| 증기 압력 | 2.9 MPa (at 21.1 °C) | ||
자화율 (χ) |
−44.0×10−6 cm3/mol | ||
| 열전도율 |
| ||
| 점도 | 15.23 μPa·s[5] | ||
| 구조 | |||
| Orthorhombic, oP28 | |||
| Oh | |||
배위 기하 구조 |
Orthogonal hexagonal | ||
| Octahedral | |||
| 0 D | |||
| 열화학 | |||
열용량 (C) |
0.097 kJ/(mol·K) (constant pressure) | ||
표준 몰 엔트로피 (S |
292 J·mol−1·K−1[6] | ||
표준 생성 엔탈피 (ΔfH⦵298) |
−1209 kJ·mol−1[6] | ||
| 약리학 | |||
| V08DA05 (WHO) | |||
| 라이선스 데이터 |
| ||
| 위험 | |||
| 물질 안전 보건 자료 | External MSDS | ||
| S-phrases (outdated) | S38 | ||
| NFPA 704 (파이어 다이아몬드) | |||
| NIOSH (미국 건강 노출 한계): | |||
PEL (허용) |
TWA 1000 ppm (6000 mg/m3)[2] | ||
REL (권장) |
TWA 1000 ppm (6000 mg/m3)[2] | ||
IDLH (직접적 위험) |
N.D.[2] | ||
| 관련 화합물 | |||
관련 sulfur fluorides |
Disulfur decafluoride 사플루오린화 황 | ||
관련 화합물 |
Selenium hexafluoride Sulfuryl fluoride Tellurium hexafluoride Polonium hexafluoride | ||
닫기
인체에 무해하나 흡입 시 성대에 영향을 주어 목소리가 일시 변화된다. 지구 온난화를 가속하는 가스이며, 1960년대부터 절연제 등으로 넓게 사용되고 있다. 이 기체는 인공적인 온실 효과를 만들어내는 기체이다. 사용량은 많지 않았으나, 최근 들어서 수요량이 늘어나고 있다. 이산화탄소, HFCs, PFCs와 함께 대표적인 온실 가스이다.


