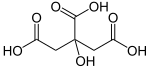
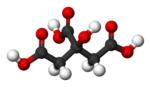
시트르산
화합물 / From Wikipedia, the free encyclopedia
시트르산(영어: citric acid) 또는 구연산(枸櫞酸)은 감귤류의 과일에서 주로 발견되는 약한 유기산이며, 화학식은 C
6H
8O
7이다. 생화학에서 시트르산은 산소 호흡을 하는 모든 생물의 대사 과정에서 일어나는 시트르산 회로의 중간생성물이다.
간략 정보 이름, 식별자 ...
| |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름
citric acid[1] | |||
| 체계명
2-hydroxypropane-1,2,3-tricarboxylic acid | |||
| 식별자 | |||
| |||
3D 모델 (JSmol) |
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider |
| ||
| DrugBank |
| ||
| ECHA InfoCard | 100.000.973 | ||
| EC 번호 |
| ||
| E 번호 | E330 (산화 방지제, ...) | ||
| KEGG |
| ||
PubChem CID |
|||
| RTECS 번호 |
| ||
| UNII | |||
CompTox Dashboard (EPA) |
|||
| |||
| |||
| 성질 | |||
| C6H8O7 | |||
| 몰 질량 | 192.123 g/mol (무수물), 210.14 g/mol (일수화물)[2] | ||
| 겉보기 | 결정성 흰색 고체 | ||
| 냄새 | 냄새 없음 | ||
| 밀도 | 1.665 g/cm3 (무수물) 1.542 g/cm3 (18 °C, 일수화물) | ||
| 녹는점 | 156 °C (313 °F; 429 K) | ||
| 끓는점 | 310 °C (590 °F; 583 K) 175 °C에서 분해[3] | ||
| 54% w/w (10 °C) 59.2% w/w (20 °C) 64.3% w/w (30 °C) 68.6% w/w (40 °C) 70.9% w/w (50 °C) 73.5% w/w (60 °C) 76.2% w/w (70 °C) 78.8% w/w (80 °C) 81.4% w/w (90 °C) 84% w/w (100 °C)[4] | |||
| 용해도 | 아세톤, 에탄올, 다이에틸 에터, 아세트산 에틸, DMSO에 용해됨 C 6H 6, CHCl3, CS2, 톨루엔에 불용성[3] | ||
| ethanol에서의 용해도 | 62 g/100 g (25 °C)[3] | ||
| amyl acetate에서의 용해도 | 4.41 g/100 g (25 °C)[3] | ||
| diethyl ether에서의 용해도 | 1.05 g/100 g (25 °C)[3] | ||
| 1,4-Dioxane에서의 용해도 | 35.9 g/100 g (25 °C)[3] | ||
| log P | −1.64 | ||
| 산성도 (pKa) | pKa1 = 3.13[5] pKa2 = 4.76[5] pKa3 = 6.39,[6] 6.40[7] | ||
굴절률 (nD) |
1.493–1.509 (20 °C)[4] 1.46 (150 °C)[3] | ||
| 점도 | 6.5 cP (50% aq. sol.)[4] | ||
| 구조 | |||
| 단사정계 | |||
| 열화학 | |||
열용량 (C) |
226.51 J/(mol·K) (26.85 °C)[8] | ||
표준 몰 엔트로피 (S |
252.1 J/(mol·K)[8] | ||
표준 생성 엔탈피 (ΔfH⦵298) |
−1543.8 kJ/mol[4] | ||
표준 연소 엔탈피 (ΔcH⦵298) |
−1960.6 kJ/mol[8] −1972.34 kJ/mol (monohydrate)[4] | ||
| 약리학 | |||
| A09AB04 (WHO) | |||
| 위험 | |||
| 주요 위험 | 피부 및 눈에 자극적 | ||
| 물질 안전 보건 자료 | HMDB | ||
| GHS 그림문자 |  [5] [5] | ||
| 신호어 | 경고 | ||
GHS 유해위험문구 |
H319[5] | ||
GHS 예방조치문구 |
P305+351+338[5] | ||
| NFPA 704 (파이어 다이아몬드) | |||
| 인화점 | 155 °C (311 °F; 428 K) | ||
| 345 °C (653 °F; 618 K) | |||
| 폭발 한계 | 8%[5] | ||
| 반수 치사량 또는 반수 치사농도 (LD, LC): | |||
LD50 (median dose) |
3000 mg/kg (쥐, 구강) | ||
닫기
매년 백만 톤 이상의 시트르산이 제조된다. 시트르산은 향료, 킬레이트제, 산성화제로 광범위하게 사용된다.[9] 시트르산은 자연적인 보존제이며, 음식이나 음료수에 산성 또는 신맛을 첨가하기 위해 사용한다. 또한 시트르산은 환경 친화적인 청소제로도 쓰이며, 커피포트 등에 굳은 석회질을 녹이는데도 쓰인다.
시트레이트(citrate)는 시트르산의 유도체로 용액에서 발견되는 염, 에스터(에스테르), 다원자 음이온이다. 예를 들어, 염은 시트르산 삼나트륨(trisodium citrate), 에스터는 트라이에틸 시트레이트(triethyl citrate)이다. 염의 일부분인 경우, 시트르산 이온의 화학식은 C6H5O73- 또는 C3H5O(COO)33-로 표기한다.