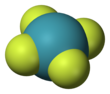
사플루오린화 제논
From Wikipedia, the free encyclopedia
사플루오린화 제논(Xenon tetrafluoride, 화학식 XeF
4)은 제논 원자와 플루오린 원자가 결합한 화합물이다. 최초로 발견된 비활성 기체의 이진상 화합물이다.[3] 제논과 플루오린 F
2의 화학 반응을 통해 합성시킨다. 화학반응식은 다음과 같다.[4][5]
- Xe + 2 F
2 → XeF
4
간략 정보 이름, 식별자 ...
 | |||
| |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름
Xenon tetrafluoride | |||
| 식별자 | |||
3D 모델 (JSmol) |
|||
| ChemSpider |
| ||
| ECHA InfoCard | 100.033.858 | ||
PubChem CID |
|||
| UNII | |||
CompTox Dashboard (EPA) |
|||
| |||
| |||
| 성질 | |||
| XeF 4 | |||
| 몰 질량 | 207.2836 g mol−1 | ||
| 겉보기 | White solid | ||
| 밀도 | 4.040 g cm−3, solid | ||
| 녹는점 | 117 °C (243 °F; 390 K) sublimes[1] | ||
| Reacts | |||
| 구조 | |||
배위 기하 구조 |
D4h | ||
| square planar | |||
| 0 D | |||
| 열화학 | |||
표준 몰 엔트로피 (S |
146 J·mol−1·K−1[2] | ||
표준 생성 엔탈피 (ΔfH⦵298) |
−251 kJ·mol−1[2] | ||
닫기
이 과정은 발열 과정이며 제논 원자가 251 kJ/mol의 에너지를 방출한다.[3]
사플루오린화 제논은 상온에서 무색의 결정체 고체 형태이다. 결정 구조는 1963년 핵자기 공명 분광법(NMR 분광법)과 X선 결정학 연구를 통해 밝혀졌다.[6][7] 원자가껍질 전자쌍 반발 이론에 따라 화합물의 분자 구조는 평면 사각형을 이룬다.[8]