배위 결합
화학 결합의 종류 위키백과, 무료 백과사전
화학 결합의 종류 위키백과, 무료 백과사전
배위 결합(配位結合, 영어: coordinate covalent bond)은 두 원자가 공유 결합을 할 때 결합에 관여하는 전자가 형식적으로 한 쪽 원자에서만 제공되어 결합된 경우를 말한다. 보통의 공유 결합과 배위결합간의 차이는 인위적으로 구분된 것이지만, 서적 등에 많이 쓰인다. 또한, 결합력과 결합에 대한 설명은 다른 극성 공유 결합과 같다.
이 문서의 내용은 출처가 분명하지 않습니다. (2012년 4월) |
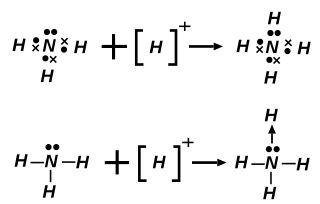
배위 결합은 루이스 염기 (전자쌍 주개)가 루이스 산 (전자쌍 받개)에게 전자쌍을 주는 것으로 형성된다. 전자쌍 받개가 음전하를 받아들일 때, 전자쌍 주개가 양전하를 받는다.
고전적으로는 비공유 전자쌍을 가지고 있는 화합물이라면 공유 결합을 가질 수 있다.
배위 결합은 특히 금속 이온을 포함하는 착화합물을 설명하는 데 자주 쓰인다. 착화합물은 몇몇 루이스 염기는 루이스 산(전자쌍 받개, 금속 양이온)에게 비공유 전자쌍을 준다. 이 결합으로 생성되는 화합물을 착화합물이라고 부르고, 전자쌍 주개를 리간드라고 부른다. 이 착화합물을 더 잘 설명할 수 있는 이론은 리간드장 이론이다.
종종 산소, 황, 질소와 할로젠화 이온을 가진 많은 화학 결합물들은 리간드의 역할을 할 수 있다. 일반적인 리간드는 물(H2O)이다. 물은 금속 이온과 착화합물을 이룬다. (예를 들어 6수화 제II구리 [Cu(H2O)6]2+)
암모니아 (NH3)나 플루오린(F-), 염소 (Cl-)와 사이아노기 (CN-)같은 음이온들 또한 일반적인 리간드이다.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.