
멜라민
From Wikipedia, the free encyclopedia
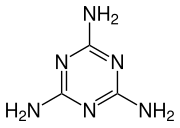
멜라민(영어: melamine[mˈeləmˌiːn], 독일어: Melamin)은 유기염기(염기성 유기 화합물)의 하나이며 분자식은 C3H6N6이고, IUPAC 이름은 1,3,5-트리아진-2,4,6-트리아민(1,3,5-triazine-2,4,6-triamine)이다.
간략 정보 이름, 식별자 ...
 | |||
| |||
| 이름 | |||
|---|---|---|---|
| 우선명 (PIN)
1,3,5-Triazine-2,4,6-triamine | |||
| 별칭
2,4,6-Triamino-s-triazine Cyanurotriamide Cyanurotriamine Cyanuramide | |||
| 식별자 | |||
| |||
3D 모델 (JSmol) |
|||
| ChEBI | |||
| ChemSpider |
| ||
| ECHA InfoCard | 100.003.288 | ||
| KEGG |
| ||
PubChem CID |
|||
| UNII | |||
CompTox Dashboard (EPA) |
|||
| |||
| |||
| 성질 | |||
| C3H6N6 | |||
| 몰 질량 | 126.123 g·mol−1 | ||
| 겉보기 | White solid | ||
| 밀도 | 1.573 g/cm3[1] | ||
| 녹는점 | 343 °C (649 °F; 616 K) (decomposition)[1] | ||
| 끓는점 | Sublimes | ||
| 3240 mg/ L (20 °C)[2] | |||
| 용해도 | very slightly soluble in hot alcohol틀:What, 벤젠, glycerol, 피리딘 insoluble in ether, 벤젠, CCl4 | ||
| log P | -1.37 | ||
| 산성도 (pKa) | 5.0 (conjugated acid)[3] | ||
| 염기도 (pKb) | 9.0[3] | ||
자화율 (χ) |
-61.8·10−6 cm3/mol | ||
굴절률 (nD) |
1.872[1] | ||
| 구조 | |||
| Monoclinic | |||
| 열화학 | |||
표준 연소 엔탈피 (ΔcH⦵298) |
-1967 kJ/mol | ||
| 위험 | |||
| > 500 °C (932 °F; 773 K) | |||
| 반수 치사량 또는 반수 치사농도 (LD, LC): | |||
LD50 (median dose) |
3850 mg/kg (rat, oral) | ||
닫기
일반적인 상온의 물에는 약간(1리터에 약 3g) 녹지만, 수온이 높아지면 비교적 잘 녹는다. 약 345 °C 이상의 온도에서는 파괴되면서 융해가 일어난다.
멜라민은 사이안아마이드(cyanamide)의 3중화합체(trimer)이다. 사이안아마이드처럼 질량의 66%가 질소이며, 레진의 성분으로서 소화기에 쓰이는데 그 이유는 연소가 되면 질소를 배출하기 때문이다. 사이안아마이드의 이합체(dimer)인 2사이안2아마이드(dicyandiamide, 또는 cyanoguanidine)도 역시 소화기 분말의 성분이다.
멜라민은 포유 동물의 살충제인 시로마진(cyromazine)을 섭취했을 때 체내에서 생성된다(metabolite).[4] 식물 또한 시로마진을 멜라민으로 전환한다고 보고되었다.[5][6]

