チクングニア熱
ウィキペディアから
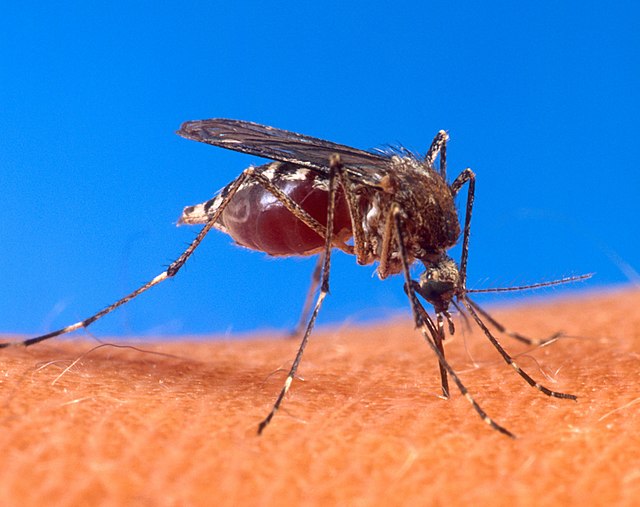
チクングニア熱(チクングニアねつ、Chikungunya fever、CHIKV)は、ネッタイシマカやヒトスジシマカなどにより媒介されるウイルス性の伝染病。トガウイルス科アルファウイルス属のチクングニアウイルスがヒトに感染することにより発症する。おなじく蚊媒介性のデング熱やウエストナイル熱と症状が類似している。日本では感染症法に基づく4類感染症および検疫法に基づく検疫感染症に指定されている。チクングニヤ熱、チクングンヤ熱などとも表記される。
症状
2日から長くても2週間程度の潜伏期間の後に、40℃に達する高熱と斑状丘疹があり、関節が激しく痛む。他に頭痛や結膜炎、羞明(眩しがること)などを伴うことがある。発熱は2日ほど続き急に終息するが、関節痛、頭痛、不眠、全身疲労などは5日から7日ほど継続する[1]。関節痛は年齢にも依るが2年ほど続くこともある[2] [3]。
また近年の流行では発熱することなく関節痛を訴える患者も多い。関節痛は朝に酷くなる傾向があり、軽い運動で楽になるが激しく動かすと悪化する。数日間痛みが和らぎ再び悪化することもよくある。膝や肩、背骨などでひどく、手足首や指の関節などにはそれほど影響がない。また職業柄酷使する関節ほど症状が酷い傾向がある。
成人では多くないが、小児とくに新生児では嘔吐、下痢、脳髄膜炎などを生じる場合がある。神経性の網膜炎やブドウ膜炎などを合併することもあるが、予後は一般的に良好で、たいていの患者が視覚を回復する[4]。
診断
症状はデング熱と類似しており、確定診断にはRT-PCR、ウイルスの分離、血清検査などの検査が必要である [5]。
- ウイルスの分離は特定の細胞株を患者血に暴露して応答を調べる方法である。患者血暴露で細胞が変性し、さらにチクングニアウイルスの特異中和抗体血清を添加した場合に変性しなければ、チクングニアウイルス陽性とする。決定的な診断法であるが1-2週間かかり、レベル3施設を必要とする。
- RT-PCRは全血からウイルス特異的な遺伝子を増幅する方法で1-2日で済む。
- 血清検査はウイルス特異的なIgMの量をELISAではかる方法である。より多量の血液が必要で2-3日かかるうえ、オニョンニョンウイルスやセムリキ森林ウイルスのような近縁ウイルスとの混同の虞がある。
病原体
チクングニアウイルス(CHIKV)はトガウイルス科アルファウイルス属に属する節足動物媒介性ウイルスである。カプシドは直径60-70 nm。58°Cで失活し、また乾燥に弱い。ウイルス株はアフリカ西部、アフリカ南部から東部、アジアの3系統に大別できる。このうちアジアのウイルスはネッタイシマカやヒトスジシマカが媒介しており、ヒト-蚊-ヒトという感染環を形成している。一方アフリカでの保有宿主は猿で、Aedes属の蚊が媒介する森林サイクルを形成している[6]。
病理
研究は乏しい。上皮や内皮の細胞、線維芽細胞や単球由来マクロファージが感受性であるのに対し、リンパ球、単球、単球由来樹状細胞は非感受性である。ウイルスはpH依存的エンドサイトーシスによって侵入し、感染によりアポトーシスが誘導され細胞変性が起きる。I型・II型のインターフェロンによって感染は阻害される。
予防
最も効果的な予防法は媒介蚊との接触を避け、蚊の繁殖を防止することである。DEET、icaridin、PMD、IR3535のような昆虫忌避剤、長袖や長ズボンの着用も効果がある。衣服をピレスロイド処理することもできる。窓や扉に網戸を設ければ蚊の家屋への侵入を防ぐことになるが、ネッタイシマカやヒトスジシマカは昼行性であり通常屋外で接触することから効果は限定的である。
ワクチン開発
ワクチンは2000年に治験が行われたが、実用化されなかった。[7]。
チクングニア熱から回復した患者から得た抗体はマウスを感染から守ることができる[8]。 ウイルス様粒子を用いて猿に対して感染防御を成立させ、かつその猿からの受動免疫で免疫不全マウスを致死量のウイルスから守ることができたことから、液性免疫が働いていることが示された[9]。
DNAワクチンも検討されている。チクングニアウイルスのカプシドとエンベロープの遺伝子配列をもとに設計したDNAワクチンによって、マウスに液性および細胞性の免疫応答を誘導することができた[10]。
治療
致死率は0.1%と極めて低いが特異療法は存在しないため、発熱に対する通常の対症療法を行う。鎮痛剤はアセトアミノフェンを第一選択とし、効かない場合に他の鎮痛剤を試みる。ステロイドやアスピリンは副作用の恐れがあり勧められない。回復期の患者に対しては、軽い運動や理学療法を勧める。こうした治療は確定診断を待つことなく行うことができる[4]。
クロロキンはチクングニア熱の症状、特に関節炎を緩和する可能性がある。アスピリンやNSAIDで緩和しない関節炎に対し、1日あたり250 mgのクロロキン燐酸塩が効果を示したとする研究がある[11]。しかし、培養細胞や猿を用いた研究ではクロロキンはチクングニア熱に対して効果がないとされる。
予後
病気からの回復は年齢によって異なる。若い患者が5-15日で回復するのに対し、中年では1-2.5月を要し、年を取るほど時間がかかる。また病気の程度も若いほうが軽い。妊娠中の感染は重症化の原因にはならないが、母子感染の確率は50%程度とされるので注意が必要である。
多くの患者で足に浮腫が認められるが、循環器や腎臓肝臓に異常はなく原因は不明である。
疫学

サハラ砂漠以南のアフリカ、インド、東南アジアなどで発生している。アフリカではサルを自然宿主とする森林サイクルが存在しているが[13]、東南アジアでの感染サイクルは主にヒト-蚊-ヒトである。人間から人間への感染は認められない。
雨期が終わり媒介蚊が増えるとともに流行が始まる。流行は普通は数年の間隔をあけて繰り返し、沈静期にはサル、ネズミ、その他の野生動物が保有宿主になっていると考えられている。しかし流行期にはヒトが保有宿主となっている。[4]
チクングニア熱はネッタイシマカに刺されることで伝播していくが、レユニオンの集団感染で分離されたウイルス株はヒトスジシマカによって媒介される能力を獲得したことが考えられている[14] 。これはウイルスのエンベロープ遺伝子(E1)に生じた点変異によりヒトスジシマカへの感染力が増強された結果であることが示されている[15][16]。ヒトスジシマカによって伝播されうるようになったことから、日本を含めヒトスジシマカが生息する地域でチクングニア熱の爆発的な流行が起きる可能性が高くなったと考えられる [17]。
2009年5月にはタイのトラン県で流行があり、母子感染を防ごうと帝王切開で出産した乳児がすでに感染していたという事例があった。このことは経胎盤感染が可能であることを想定させるが、実験的な検証はなされていない[18]。
歴史
この病気はタンザニアとモザンビークの境界に広がるマコンデ平原で1952年に流行があり、Marion Robinson[19]とW.H.R. Lumsden[20]が1955年に報告したのが最初である。
chikungunyaという名前はマコンデ語の「曲げるもの」という言葉に由来し、体を屈めて関節痛に耐える患者の様子を形容したものとされている。
発見以来、アフリカ、南アジア、東南アジアなどで突発的流行を繰り返しており、さらに拡大しつつある。不顕性感染で終わる可能性が大きいとされているが、しかし2005年以降の流行では、おそらくウイルスの遺伝子変異によって、劇症化の傾向がある。インド洋の島レユニオンでは、2006年5月18日までに人口78万人のほぼ3分の1に当たる25万8,000人が感染、219人が死亡している。またインドでも2006年に各地で流行している。2007年1月24日、日本での感染を初めて確認する。
この病気の流行は記録上1779年に遡る可能性がある[21]。 この年代はウイルスが1700年頃に発生したという分子遺伝学的データと符合する[22]。
関連項目
- ボルバキア
- World mosquito program
出典
外部リンク
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
