
コバルト酸リチウム
リチウムイオン電池正極材料 / ウィキペディア フリーな encyclopedia
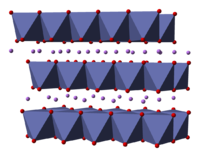
コバルト酸リチウム (コバルトさんリチウム) は二酸化リチウムコバルト (にさんかリチウムコバルト) または酸化リチウムコバルト(III) (さんかリチウムコバルト さん、英: lithium cobalt(III) oxide) の慣用名[注釈 1]であり、組成式 LiCoO2 で表わされる化合物である。 リチウムイオン二次電池の正極として用いられる。LiCoO2 の構造は、リチウム層とコバルトと酸素原子の八面体で構成されるスラブが交互に積層した構造であることが[2]、理論的にも、 X線回折、電子顕微鏡、粉末中性子回折、EXAFSなどの手法を用いて実験的にも知られている[3]。結晶の空間群はヘルマン・モーガン記号で 
概要 Lithium cobalt oxide, 識別情報 ...
| Lithium cobalt oxide[1] | |
|---|---|
 | |
 | |
lithium cobalt(III) oxide | |
別称 lithium cobaltite | |
| 識別情報 | |
| CAS登録番号 | 12190-79-3 |
| PubChem | 23670860 |
| 特性 | |
| 化学式 | LiCoO2 |
| モル質量 | 97.87 g mol−1 |
| 危険性 | |
| 主な危険性 | harmful |
| Rフレーズ | R42/43 |
| Sフレーズ | S36 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
閉じる
LiCoO2 を正極に用いる電池は容量が大きい代償として反応性が高く、リチウム・ニッケル・アルミニウム酸化物系などの新型よりも熱的安定性(英語版)に欠ける。このため、 LiCoO2 電池は高温 (>130 ℃) での使用時や過充電の際に熱暴走の懸念がある。温度が上昇すると、LiCoO2 は分解して酸素を発生し、その酸素が電解質の有機溶媒と反応してしまう。この反応は発熱の大きい反応であり、周囲のセルにまで熱暴走が拡大したり、周囲の可燃物に引火する危険性がある[5]。
この化合物のインターカレーション型電極としての有用性は1980年、オックスフォード大学の水島公一とジョン・グッドイナフらにより発見された[6]。