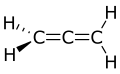Doppio legame
tipo di legame covalente Da Wikipedia, l'enciclopedia libera
In chimica, un doppio legame è un legame chimico che coinvolge un numero doppio di elettroni rispetto ad un legame singolo (o "legame semplice").
Nella formula di struttura un doppio legame viene rappresentato da due segmenti paralleli congiungenti i due atomi attraverso i quali si forma il doppio legame.
L'energia di legame associata ad un doppio legame è maggiore dell'energia di un legame semplice, per cui nel caso del doppio legame gli atomi risentono di una forza attrattiva maggiore, ovvero la loro lunghezza di legame è minore. Inoltre a causa del loro elevato contenuto energetico i doppi legami presentano una maggiore reattività rispetto ai legami semplici.
I doppi legami nei composti organici
In chimica organica il doppio legame e il triplo legame vengono chiamati insaturazioni[1] e i composti che contengono almeno uno di essi vengono definiti composti insaturi
I doppi legami tra due atomi di carbonio di una molecola organica sono formati da un legame σ e un legame π, ai quali sono associate energie di legame differenti, per cui l'apertura del doppio legame avviene sempre rompendo il legame meno forte, che è il legame π.
Quando una molecola organica contiene due o più doppi legami, essi sono detti:
- cumulati: se legano almeno 3 atomi di carbonio tra loro consecutivi;[2]
- coniugati: se sono intervallati da un legame singolo;[3]
- isolati: se non rientrano in nessuno dei due casi precedenti.[4]
- Esempio di molecola con doppi legami cumulati (propadiene)
- Esempio di molecola con doppi legami coniugati (butadiene)
- Esempio di molecola con doppi legami isolati (1,5-cicloottadiene)
Esempi
Esempi di sostanze chimiche che contengono un doppio legame sono:
- alcheni (C=C)
- azocomposti (N=N)
- immine (C=N)
- solfossidi (S=O)
- gruppo carbonilico (C=O).
Note
Voci correlate
Altri progetti
Collegamenti esterni
Wikiwand - on
Seamless Wikipedia browsing. On steroids.