Idrossido di calcio
composto chimico Da Wikipedia, l'enciclopedia libera
L'idrossido di calcio (genericamente indicato come calce spenta o calce idratata) è un composto con formula chimica Ca(OH)2. È un cristallo incolore o una polvere bianca ed è prodotto per idratazione a secco dell'ossido di calcio (denominato anche calce o calce viva).
| Idrossido di calcio | |
|---|---|
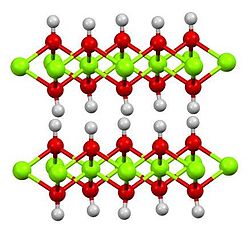 | |
 | |
| Nome IUPAC | |
| diidrossido di calcio | |
| Nomi alternativi | |
| calce spenta calce idratata | |
| Caratteristiche generali | |
| Formula bruta o molecolare | Ca(OH)2 |
| Massa molecolare (u) | 74,10 |
| Aspetto | cristallo incolore o polvere bianca |
| Numero CAS | |
| Numero EINECS | 215-137-3 |
| PubChem | 14777 e 6093208 |
| SMILES | [OH-].[OH-].[Ca+2] |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 2.24 |
| Costante di dissociazione basica a 298 K | 2,3442×10−2 |
| Solubilità in acqua | 1,7 g/l a 293 K[1] |
| Costante di solubilità a 298 K | 4,86×10−6 |
| Temperatura di fusione | 580 °C (decomposizione) |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| pericolo | |
| Frasi H | 318 |
| Consigli P | 280 - 305+351+338 - 313 [1] |
Comportamento chimico
Se riscaldato a 580 °C l'idrossido di calcio si decompone in ossido di calcio e acqua[1].
Una soluzione acquosa satura di idrossido di calcio (circa 0,5%) è detta acqua di calce, ed è una base molto forte che reagisce violentemente con gli acidi.
Il latte di calce è una sospensione di particelle di idrossido di calcio in acqua[2], utile e ampiamente utilizzata in diversi processi chimici.
Usi
Riepilogo
Prospettiva
A causa della sua proprietà di base forte, l'idrossido di calcio ha molti vari usi tra i quali si annoverano:
- in edilizia, con il nome di calce idrata, viene impiegato come componente di malte, intonaci, stucchi e pitture;
- lasciato in ammollo in vasche d'acqua crea una pasta che galleggia in superficie, questo tipo di pasta/malta viene chiamato "grassello di calce", viene distribuito in forma di pasta a mollo nell'acqua in sacchi di plastica;
- in pittura, viene usato come pigmento pittorico, con il nome di bianco di calce bianca, bianco di Firenze, calce spenta e gesso di Firenze;
- il trattamento delle acque luride e il miglioramento del suolo acido (è ad esempio responsabile del colore intenso delle ortensie);
- la doratura del cuoio;
- l'utilizzo come sostituto della soda caustica;
- come reagente ampiamente utilizzato:
- nell'industria chimica, per la neutralizzazione degli acidi;
- nelle industrie di raffinamento del petrolio, per la fabbricazione di additivi agli olii (alchilsalicilicato, solfatico, fenatico);
- nell'industria chimica per la fabbricazione di stearato di calcio;
- per neutralizzazione di ambienti acidificati, in particolare le acque sporche in serbatoi;
- nell'industria alimentare per l'elaborazione dell'acqua (per produzione di alcool e bibite analcoliche);
- nella preparazione di alcuni cibi umani trasformati in ambiente fortemente alcalino, ad esempio il Nixtamal in America latina;
- nell'agro-chimica per neutralizzare l'acidità del terreno;
- per eliminare salamoia di carbonati di calcio e magnesio nella fabbricazione di sale (come alimento) e in farmacopea;
- nel metodo calce-soda per diminuire la durezza dell'acqua;
- come componente:
- nell'industria petrolchimica per produrre grassi solidi;
- nella fabbricazione dei pattini dei freni;
- nella fabbricazione di ebanite;
- per la preparazione di miscele in polvere pigmentate, per pittura e decorazioni;
- nelle miscele antiparassitarie e fungicide in agricoltura soprattutto per neutralizzare l'acidità del solfato di rame e ottenere la famosa poltiglia bordolese che ha salvato la viticoltura nel mondo. Tale composto era in uso già in epoca romana[senza fonte].
- in acquariologia marina, l'acqua ricca di ioni di calcio idrossido viene immessa col metodo goccia a goccia dopo aver fatto posare la polvere, per il nutrimento dei coralli e delle alghe calcaree e per abbassare i fosfati presenti;
- in odontoiatria, per la medicazione di denti il cui canale radicolare è in necrosi. Le proprietà basiche del composto permettono di disinfettare e togliere il dolore causato dai batteri. Il composto è usato solo come medicazione provvisoria.[3]
Rischi
Assumere dosi eccessive di idrossido di calcio può provocare sintomi pericolosi[4], tra i quali:
- Ipotensione
- Difficoltà di respirazione
- Spurgo gastrointestinale
- Cambiamento drastico del pH nel sangue, causando danni agli organi.
Note
Voci correlate
Altri progetti
Collegamenti esterni
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
