Timeline
Chat
Prospettiva
Chelazione
Da Wikipedia, l'enciclopedia libera
Remove ads
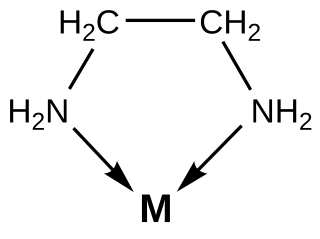
La chelazione è una reazione chimica in cui solitamente un atomo metallico, comportandosi da acido di Lewis, viene legato da un reagente detto chelante tramite più di un legame coordinativo. La struttura del composto risultante costituisce un particolare complesso molto stabile che vede l'atomo centrale essere circondato a tenaglia dal chelante, come se fosse stretto tra le chele di un granchio (da cui il termine chelazione). Il chelante è spesso definito legante polidentato (nello specifico, bidentato, tridentato, ecc.).
In ambito biologico, tramite chelazione l'emoglobina lega il ferro e la clorofilla lega il magnesio. In chimica la chelazione viene sfruttata per effettuare titolazioni complessometriche, per favorire la solubilizzazione o per alcune applicazioni tecnologiche atte a prevenire l'effetto di acque incrostanti. In medicina la chelazione viene sfruttata nella terapia chelante per il trattamento di alcune intossicazioni dovute all'accumulo di metalli nell'organismo: una volta chelato, il metallo perde le sue caratteristiche (e quindi nel caso perde la tossicità) per poi venire eliminato legato assieme al chelante, in metallurgia molecole polimeriche chelanti idrosolubili vengono anche usate come convertitore di ruggine per gli acciai e creare strati di conversione per aumentarne la resistenza alla corrosione. In agricoltura elementi altrimenti poco solubili nel suolo, come ad esempio il ferro, in caso di carenze possono essere somministrati alle piante per via fogliare sotto forma chelata.
Remove ads
Termodinamica
Riepilogo
Prospettiva
La stabilità termodinamica di un chelato è legata all'aumento di entropia insita nello stesso processo di chelazione. Ad esempio, si considerino le due differenti complessazioni dello stesso ione metallico, Cu2+ in soluzione acquosa, con un legante simile (gruppo amminico) dove la prima è una reazione di chelazione:[1]
- [Cu(H2O)6]2+ + 2 NH3 [Cu(H2O)4(NH3)2]2+ + 2 H2O
Le due reazioni hanno variazione di entalpia standard comparabili (rispettivamente -54 kJ/mol e -46 kJ/mol), mentre la variazione di entropia standard è nettamente differente e in ultima analisi rappresenta il fattore a cui è legato il maggior carattere negativo dell'energia libera standard legata alla chelazione. Il valore di ΔS° è +23 J K−1 mol−1 per la reazione chelante e -8,4 J K−1 mol−1 nell'altro caso; ciò si può evidenziare dall'aumento totale di molecole che si ottiene dalla chelazione, verificabile dalla differenza della somma dei coefficienti stechiometrici dei prodotti e dei reagenti. Nel caso in cui non si ha chelazione la variazione di entropia invece è piccola, essendo praticamente invariato il numero di specie chimiche implicate.
Remove ads
Comuni chelanti in chimica
Gli agenti chelanti più comunemente sfruttati in chimica sono:
- EDTA
- Acetilacetonato (acac)
- Poliammine quali la dietilentriammina (dien), l'etilendiammina (en), la trietilentetrammina (tren), il tetrazociclotetradecano (cyclam)
- Ossalato (ox)
- Carbonato, che può legare anche con i due ossigeni negativi
- Eteri corona
- 2,2'-bipiridina (bipy)
- Glicinato (gly)
- Nitrilotriacetato (nta)
Note
Voci correlate
Altri progetti
Collegamenti esterni
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads

