Loading AI tools
Da Wikipedia, l'enciclopedia libera
I triazoturi,[1] nome sistematico del nome comune "azoturi" (ambiguo) e impropriamente detti anche azidi (traduzione pedestre dall'inglese), sono composti salini binari formati dall'azoto con un metallo (M), di formula generale M(N3)n, oppure composti organici in cui il gruppo N3 è unito ad un alchile o arile, di formula R-N3. Il "triazoturo di idrogeno" (HN3) è il nome sistematico dell'acido azotidrico (nome comune).[1]
| ione azoturo | |
|---|---|
 | |
| Nome IUPAC | |
| ione triazoturo(1-) | |
| Caratteristiche generali | |
| Massa molecolare (u) | 42,021 g/mole |
| Aspetto | colore bianco, inodore, solido cristallino. |
| Numero CAS | |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
 
| |
| attenzione | |
| Frasi H | --- |
| Consigli P | --- |
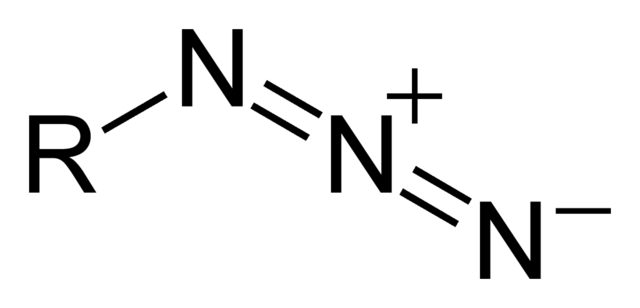
N3− è un anione pressoché lineare isoelettronico con CO2 e N2O, con distanze di legame pari 116 pm.
Si ottengono facendo gorgogliare protossido d'azoto in ammoniuri alcalini fusi:
Questo comportamento viene sfruttato nei detonatori militari (azoturo di piombo) e commerciali (capsule esplosive degli airbag), con il più comune azoturo di sodio; altri composti sono l'azoturo di mercurio o di argento.
L'azoturo di sodio (NaN3) è un composto bianco, assai velenoso, usato nei laboratori come preservante di fluidi biologici (plasma, siero, diluizioni anticorpali ed altri campioni biologici contenenti proteine), poiché è dotato di proprietà battericide. Trova infine uso, come già accennato, come carica propellente negli airbag.
Un secondo uso applicativo riguarda la sintesi chimica; gli azoturi sono impiegati per inserire in una molecola la specie N-. Recentemente è stato dimostrato che il composto azabicicloeptadiene[2] (il cui anione per cessione dello N- si trasforma in antracene) è molto meno pericoloso e agisce nello stesso modo in condizioni assai più favorevoli.
L'anione azide è tossico per l'organismo umano, in quanto inibisce il complesso IV e di conseguenza la catena di trasporto degli elettroni nella fosforilazione ossidativa. Ha effetti simili a quelli dell'avvelenamento da cianuro (inibizione sintesi di ATP).

I ricercatori che lo hanno sintetizzato scrivono: La sensibilità di C2N14 è al di là delle nostre capacità di misura. Il più piccolo peso disponibile per test di urto e frizione ne provoca la decomposizione esplosiva... Durante la registrazione di spettri IR e Raman si sono verificate esplosioni per semplice esposizione a luce laser a bassa intensità.[3]
L'azoturo di piombo, ad esempio, si decompone secondo la seguente reazione:
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.