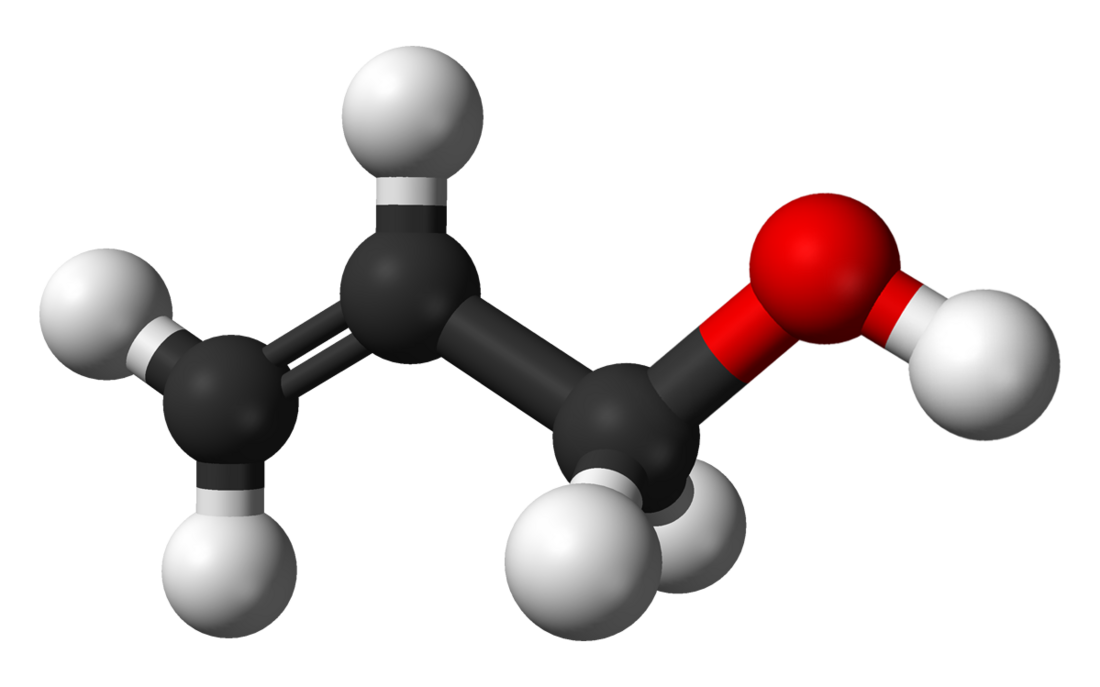
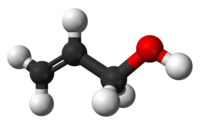
L'alcol allilico è il composto organico con formula di struttura CH2=CHCH2OH. In condizioni normali è un liquido incolore con odore irritante di senape. È molto solubile in acqua, alcoli, etere e cloroformio. Risulta più tossico della maggior parte degli alcoli a basso peso molecolare. Viene utilizzato principalmente per produrre glicerolo, acroleina e altri composti allilici.[3][4]
| Alcol allilico | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| 2-propen-1-olo | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C3H6O |
| Massa molecolare (u) | 58,08 |
| Aspetto | liquido incolore |
| Numero CAS | |
| Numero EINECS | 203-470-7 |
| PubChem | 7858 |
| SMILES | C=CCO |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 0,85[1] |
| Solubilità in acqua | 320 g/l a 20 °C[1] |
| Temperatura di fusione | −129 °C (144 K)[1] |
| Temperatura di ebollizione | 97 °C (370 K)[1] |
| Tensione di vapore (Pa) a 20 °C K | 23,9 hPa[1] |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | -171,8[2] |
| C0p,m(J·K−1mol−1) | 138,9[2] |
| Proprietà tossicologiche | |
| DL50 (mg/kg) | 64 oral rat[1] |
| Indicazioni di sicurezza | |
| Punto di fiamma | 21 °C[1] |
| Limiti di esplosione | 2,5–18%[1] |
| Temperatura di autoignizione | 375 °C[1] |
| Simboli di rischio chimico | |
  
| |
| pericolo | |
| Frasi H | 225 - 301 - 310 - 330 - 319 - 335 - 315 - 400 - 412 [1] |
| Consigli P | 210 - 280 - 303+361+353 - 305+351+338 - 501 [1] |
Sintesi
L'alcol allilico fu sintetizzato per la prima volta nel 1856 da Auguste André Thomas Cahours e August Wilhelm von Hofmann per saponificazione dello ioduro di allile.[5] Oggi l'alcol allilico può essere prodotto industrialmente in vari modi; i processi più importanti sono l'idrolisi del cloruro di allile con idrossido di sodio a 150 ºC :
- CH2=CHCH2Cl + NaOH → CH2=CHCH2OH + NaCl
e l'isomerizzazione catalitica dell'ossido di propilene.[3]
In laboratorio si può preparare per reazione del glicerolo con acido ossalico o acido formico:[6]
Proprietà
L'alcol allilico è un liquido stabile a temperatura ambiente, mentre scaldato sopra i 100 ºC tende a polimerizzare. L'alcol allilico possiede un gruppo ossidrilico e un doppio legame, e di conseguenza può dar luogo a varie reazioni come ossidazione, riduzione, idrogenazione, condensazione e addizione.[3]
Usi
La maggior parte dell'alcol allilico è usato per la sintesi di glicerolo. Come usi minori è anche un intermedio nella produzione di eteri e esteri allilici, oli siccativi, plastificanti, ritardanti antifiamma, fungicidi e conservanti.[3]
Tossicità / Indicazioni di sicurezza
L'alcol allilico è un composto facilmente infiammabile, tossico per inalazione, ingestione o contatto con la pelle. C'è il sospetto di possibili effetti cancerogeni. È pericoloso per gli organismi acquatici con effetti di lunga durata.[1]
Note
Bibliografia
Altri progetti
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.