Utente:Itis geymonat/Sandbox/Elettrone valenza
Da Wikipedia, l'enciclopedia encyclopedia
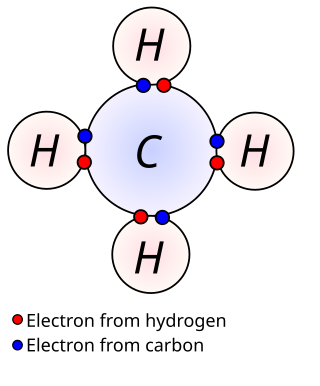
In chimica, un elettrone di valenza è un elettrone associato ad un atomo, e che può partecipare alla formazione di un legame chimico; in un singolo legame covalente, entrambi gli atomi del legame contribuiscono con un elettrone di valenza allo scopo di formare un doppietto condiviso. La presenza di elettroni di valenza può determinare le proprietà chimiche degli elementi e la possibilità di legarsi ad altri elementi: Per un main group element, l’elettrone di valenza può trovarsi solo nell’ultimo orbitale. Negli elementi di transizione, un elettrone di valenza può anche essere in un orbitale interno.
Un atomo con un orbitale completo di elettroni di valenza (corrispondente ad una configurazione elettronica s2p6) tende ad essere chimicamente neutro. Un atomo con uno o due elettroni di valenza in più di un orbitale completo è altamente reattivo, perché gli elettroni di valenza in più sono facilmente rimovibili per formare uno ione positivo. Un atomo con uno o sue elettroni di valenza in meno di un orbitale completo è comunque altamente reattivo, perché tendono tutti e due a ottenere l’elettrone di valenza mancante (quindi a formare uno ione negativo), o condivider elettroni (quindi formare un legame covalente).
Like an electron in an inner shell, a valence electron has the ability to absorb or release energy in the form of a photon. An energy gain can trigger an electron to move (jump) to an outer shell; this is known as atomic excitation. Or the electron can even break free from its associated atom's valence shell; this is ionization to form a positive ion. When an electron loses energy (thereby causing a photon to be emitted), then it can move to an inner shell which is not fully occupied.