
Piruvato carbossilasi
Da Wikipedia, l'enciclopedia encyclopedia
La piruvato carbossilasi è un enzima che catalizza la seguente reazione chimica, tappa della gluconeogenesi e reazione anaplerotica del ciclo di Krebs:
- piruvato + HCO3- + ATP ⇄ ossalacetato + ADP + Pi
Questa voce sull'argomento enzimi è solo un abbozzo.
Contribuisci a migliorarla secondo le convenzioni di Wikipedia. Segui i suggerimenti del progetto di riferimento.
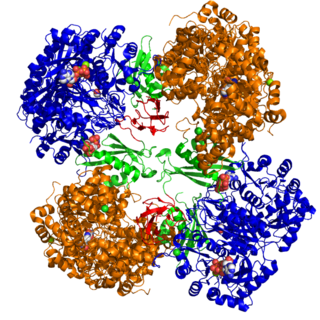
È un complesso enzimatico formato da quattro subunità identiche. Ogni subunità ha un gruppo prostetico di biotina legato covalentemente ad un residuo di lisina. Ciascuna subunità è dotata di tre siti specifici:
- Un sito carrier della biotina legato a un residuo di Lisina;
- Un primo sito catalitico dove lo ione carbonato viene convertito a carbossifosfato, con consumo di ATP; sempre in questo sito viene poi sganciato dal carbossifosfato fosfato inorganico, mentre l'anidride carbonica è agganciata alla biotina, formando il complesso cabossibiotinil-enzima;
- Un secondo sito catalatico dove il complesso biotinil enzima cede al piruvato anidride carbonica.