From Wikipedia, the free encyclopedia
Բրուգադա համախտանիշ (ԲրՀ), գենետիկ հիվանդություն, որի ժամանակ խախտվում է սրտի էլեկտրական ակտիվությունը։ Այն մեծացնում է սրտի առիթմիաների և հանկարծակի սրտային մահվան առաջացման վտանգը։ Այս համախտանիշը ունեցողները կարող են ունենալ ուշագնացության դրվագներ։ Բրուգադա համախտանիշով հիվանդները ունենում են առիթմիայի դրվագներ հանգստի ժամանակ և դրանք երբեմն հարուցվում են տենդով[1][2]։
| Բրուգադա համախտանիշ | |
|---|---|
 | |
| Տեսակ | հազվագյուտ հիվանդություն և հիվանդության կարգ |
| Հետևանք | Փորոքային ֆիբրիլյացիա |
| Բժշկական մասնագիտություն | սրտաբանություն |
| ՀՄԴ-9 | 746.89 |
| Անվանվել է | Pedro Brugada?, Josep Brugada?, Ramon Brugada? և Brugada brothers? |
Բրուգադա համախտանիշով հիվանդների մոտ մեկ քառորդը ունի ընտանիքի անդամ, ով նույնպես տառապում է այս հիվանդությամբ։ Որոշ դեպքերում կարող է պայմանավորված լինել նոր գենետիկ մուտացիայով կամ որոշ դեղամիջոցներով[1]։ Ախտահարված ամենատարածված գենը SCN5A- ն է, որը կոդավորում է սրտի նատրիումական անցուղիները[3]։ Ախտորոշումը սովորաբար իրականացվում է էլեկտրոսրտագրությամբ (ԷՍԳ), սակայն փոփոխությունները կարող են ոչ միշտ առկա լինել։ Դեղամիջոցներ, ինչպիսին է այմալինը, կարող են օգտագործվել ԷՍԳ փոփոխությունները բացահայտելու համար։ Նմանատիպ ԷՍԳ կարող է հայտնաբերվել որոշակի էլեկտրոլիտային խանգարումների ժամանակ կամ երբ սրտի արյան մատակարարումը նվազել է[4]։
Այս համախտանիշի համար բուժում դեռևս չկա[5]։ Հանկարծակի սրտային մահվան բարձր ռիսկով հիվանդներին ցուցված է իմպլանտացվող կարդիվերտեր դեֆիբրիլյատորի (ICD) տեղադրումը[6]։ Առանց ախտանշանների հիվանդների մոտ մահացության վտանգը շատ ավելի ցածր է և պարզ չէ թե ինչպես բուժել նրանց[5][7]։ Իզոպրոտերենոլը կարող է օգտագործվել կարճ ժամանակով այն դեպքերում, երբ առկա են հաճախակի կյանքին սպառնացող ռիթմեր, իսկ քինիդինը կարող է օգտագործվել ավելի երկար ժամկետով[5][8]։ Կարող է խորհուրդ տրվել մարդկանց ընտանիքի անդամների ստուգում[5]։
Համախտանիշը հանդիպում է 10,000 մարդուց 1-30-ի մոտ։ Ավելի հաճախ հանդիպում է արական սեռի և ասիացիների մոտ[1]։ Ախտանշանների սկիզբը սովորաբար հասուն տարիքում է։ Այն անվանակոշվել է իսպանացի սրտաբաններ Պեդրո և Ջոզեփ Բրուգադաների պատվին, ովքեր և նկարագրել են համախտանիշը 1992 թվականին[5][9]։ Նրանց եղբայր Ռամոն Բրուգադը առաջինն էր, ով 1998 թվականին նկարագրեց գենետիկ պատճառով դեպք[10]։
Չնայած այս համախտանիշը ունեցող շատ մարդիկ չեն ունենում ախտանշաններ, երբեմն այն կարող է բերել ուշագնացության կամ հանկարծակի սրտային մահվան՝ առաջացնելով այնպիսի ծանր առիթմիա, ինչպիսին է փորոքային ֆիբրիլյացիան կամ պոլիմորֆ փորոքային հաճախասրտությունը[7]։ Ուշագնացությունները կարող են առաջանալ առիթմիայի կարճատև դրվագների հետևանքով, երբ ռիթմը վերականգնվում է ինքնուրույն։Եթե վտանգավոր առիթմիան ինքնուրույն չի անցնում և շտապ չի բուժվում, ապա կարող է առաջանալ սրտի կանգ՝ մահացու ելքով։ Այնուամենայնիվ այս համախտանիշով հիվանդների մոտ ուշագնացություն կարող է առաջանալ նույնիսկ նորմալ ռիթմի դեպքում՝ ԶՃ-ի կտրուկ անկման պատճառով (վազովագալ սինկոպէ)։
Ռիթմի խանգարումները սովորաբար ի հայտ են գալիս հանգիստ վիճակում՝ ծանր ճաշից հետո կամ նույնիսկ քնած ժամանակ[2]։ Այս վիճակները կապված թափառող նյարդի ակտիվության շրջանների հետ։ Առիթմիան կարող է ի հայտ գալ նաև տենդի ժամանակ կամ մեծ քանակությամբ ալկոհոլ ընդունելուց հետո։ Որոշ դեղամիջոցներ կարող են վատացնել վիճակը և բերել վտանգավոր առիթմիաների առաջացմանը[11]։
Սրտի յուրաքանչյուր բջիջ հաղորդակցվում է մյուսների հետ էլեկտրական ազդակների միջոցով, որոնք Բրուգադա համախտանիշի դեպքում խանգարվում են։ Որպես գենետիկ խանգարում, այս հիվանդությունն առաջանում է մարդու ԴՆԹ- ում փոփոխությունների՝ մուտացիաների, հետևանքով։ Բրուգադա համախտանիշի հետ ասոցացված առաջին նկարագրված մուտացիան սրտի նատրիումական անցուղիները կոդավորող գենում էր։ Համախտանիշի պատճառ հանդիսացող մուտացիաների մեծ մասը կապված է նատրիումական կամ այլ իոնային անցուղիների հետ[4]։
Բրուգադա համախտանիշին բնորոշ ԷՍԳ պատկեր կարող են առաջացնել բազմաթիվ պատճառներ, ներառյալ որոշ դեղամիջոցներ, էլեկտրոլիտային խանգարումներ, ինչպիսին է արյան մեջ կալիումի մակարդակի նվազումը և սրտի որոշակի հատվածների, հատկապես աջ փորոքի արտատար տրակտի, արյան մատակարարման իջեցումը[4]։ Այսպիսի դեղորայքին են պատկանում հակաառիթմիկ դեղեր, ինչպիսիք են ֆլեկաինիդը, վերապամիլը և պրոպրանոլոլը, հակադեպրեսանտներ, ինչպիսին է ամիտրիպտիլինը, և վագալ ակտիվությունը բարձրացնող դեղեր, ինչպիսին է ացետիլխոլինը։ ԷՍԳ այդպիսի փոփոխություններ կարելի է տեսնել նաև ալկոհոլի կամ կոկաինի չարաշահման դեպքում[4]։
Բրուգադա համախտանիշը ժառանգվում է աուտոսոմ դոմինանտ ձևով, ինչը նշանակում է, որ համախտանիշի առաջացման համար անհրաժեշտ է թիրախ գենի միայն մեկ օրինակ։ Այնուամենայնիվ, ախտորոշված անձը կարող է առաջինն ընտանիքում ունենալ Բրուգադա համախտանիշ, եթե այն առաջանում է որպես նոր մուտացիա[2]։ Բրուգադա համախտանիշի ժամանակ ամենհաճախ ախտահարվող գենը SCN5A գենն է, որը պատասխանատու է սրտի նատրիումական անցուղիների համար։ Բրուգադա համախտանիշի հետ կապված SCN5A-ի մուտացիաները հիմնականում առաջացնում են նատրիումի իոնների հոսքի նվազեցում։ Այնուամենայնիվ, Բրուգադա համախտանիշի դեպքերի միայն 20% -ն է կապված SCN5A-ի մուտացիաների հետ, քանի որ հիվանդների մեծամասնության մոտ գենետիկական փորձարկմամբ հնարավոր չի լինում բացահայտել գենետիկ մուտացիայի պատասխանատուներին[2]։ SCN5A գենի ավելի քան 290 մուտացիաներ են հայտնաբերվել մինչ օրս, որոնցից յուրաքանչյուրը նատրիումական անցուղիների գործառույթը փոփոխում է տարբեր ձևերով[12]։ Այս տարբերությունները մասամբ բացատրում են տարբեր անձանց մոտ հիվանդության ծանրության տարբերությունները, սկսած վտանգավոր վիճակներից, որը առաջացնում է մահը երիտասարդ տարիքում, մինչև անախտանիշ դեպքեր, երբ որևէ խնդիր չի առաջանում։ Այնուամենայնիվ, Բուգադա համախտանիշի գենետիկան բարդ է, և հավանական է, որ վիճակը շատ գեների փոխազդեցության արդյունք է։ Այս բարդ փոխհարաբերությունների պատճառով ընտանիքի որոշ անդամներ, որոնք ունեն կոնկրետ մուտացիա, կարող են ունենալ Բրուգադա համախտանիշի նշաններ, իսկ մյուսները՝ ոչ (փոփոխվող պենետրանտություն)[13]։
Առկա են Բրուգադա համախտանիշի հետ ասոցացված նաև այլ գեներ։ Դրանցից որոշները պատասխանատու են նատրիումական անցուղիների այլ հատվածների համար, որոնք հայտնի են, որպես β ենթամիավորներ (SCN1B, SCN2B, SCN3B) մինչդեռ մյուսները կոդավորում են այլ տիպի նատրիումական նացուղիներ (SCN10A)։ Որոշ գեներ կոդավորում են կալցիումական կամ կալիումական անցուղիներ (CACNA1C, CACNB2, KCND3, KCNE3, KCNJ8)[14], իսկ մի մասը կոդավորում են իոնային անցուղիների հետ փոխազդող սպիտակուցներ (GPD1L, PKP2, MOG1, FGF12)։ Բրուգադա համախտանիշի հետ ասոցացված գեները ներառում են․
| Տիպ | OMIM | Գեն | Նշումներ |
|---|---|---|---|
| ԲրՀ1 | 601144 | SCN5A | NaV1.5 – սրտային նատրիումական անցուղու ենթամիավոր, որը իրականացնում է նատրիումական հոսքը INa[3]։ |
| ԲրՀ2 | 611778 | GPD1L | Գլիցերոլ-3-ֆոսֆատ դեհիդրոհենազի նման պեպտիդ – նվազած GPD1-L ակտիվությունը բերում է NaV1.5 ֆոսֆորիլացմանը և INa նվազմանը[3]։ |
| ԲրՀ3 | 114205 | CACNA1C | CaV1.2 – վոլտաժ կախյալ կալցիումական անցուղիների ենթամիավոր, որը պայմանավորում է L տիպի կալցիումական հոսքը ICa(L)[15]։ |
| ԲրՀ4 | 600003 | CACNB2 | CaVβ2B – վոլտաժ կախյալ կալցիումական անցուղիների β-2 ենթամիավոր, որը պայմանավորում է L տիպի կալցիումական հոսքը ICa(L)[15]։ |
| ԲրՀ5 | 600235 | SCN1B | NaVβ1 – նատրիումական անցուղիների β-1 ենթամիավոր, որը պայմանավորում է նատրիումական հոսքը INa[15]։ |
| ԲրՀ6 | 604433 | KCNE3 | MiRP2 – վոլտաժ կախյալ կալիումական անցուղիների β ենթամիավոր։ Կարգավորում է դեպի դուրս կալիումի ժամանակավոր հոսքը Ito[15]։ |
| ԲրՀ7 | 608214 | SCN3B | NaVβ3 – նատրիումական անցուղիների β-3 ենթամիավոր, որը պայմանավորում է նատրիումական հոսքը INa[3]։ |
| ԲրՀ8 | 600935 | KCNJ8 | Kir6.1, պայմանավորում է կալիումի ներհոսքը IKir[3]։ |
| ԲրՀ9 | 114204 | CACNA2D1 | Վոլտաժ կախյալ կալցիումական անցուղիների α2δ ենթամիավոր, որը պայմանավորում է L տիպի կալցիումական հոսքը ICa(L)[3]։ |
| ԲրՀ10 | 605411 | KCND3 | KV4.3, ժամանակավոր կալիումական արտահոսքի α ենթամիավոր Ito[3]։ |
| ԲրՀ11 | 607954 | RANGRF | Encodes MOG1 – ազդում է NaV1.5-ի կարգավորման վրա[3]։ |
| ԲրՀ12 | 602701 | SLMAP | Սարկոլեմայի թաղանթ ասոցացված սպիտակուց, T- խողովակների և սարկոպլազմատիկ ցանցի միավոր, ազդում է NaV1.5 կարգավորման վրա[3]։ |
| ԲրՀ13 | 601439 | ABCC9 | SUR2A, IK(ԱԵՖ) անցուղիների ադենոզին եռֆոֆատ (ԱԵՖ)- կապող բաղադրիչ[3]։ |
| ԲրՀ14 | 601327 | SCN2B | NaVβ2 – նատրիումական անցուղիների Beta-2 ենթամիավոր, որը պայմանավորում է նատրիումական հոսքը INa[3]։ |
| ԲրՀ15 | 602861 | PKP2 | Պլակոֆիլին- 2 – փոփոխում է INa[3]։ |
| ԲրՀ16 | 601513 | FGF12 | Ֆիբրոբլաստի աճի գործոն- 1 – մուտացիան նվազեցնում է INa[3]։ |
| ԲրՀ17 | 604427 | SCN10A | NaV1.8 – նյարդային նատրիումական անցուղու ենթամիավոր[15]։ |
| ԲրՀ18 | 604674 | HEY2 | Տրանսկրիպցիայի գործոն[3]։ |
| ԲրՀ19 | 603961 | SEMA3A | Սեմաֆորին[3]։ |
| ԲրՀ20 | 601142 | KCNAB2 | KVβ2, վոլտաժ կախյալ կալիումական անցուղիների β2 ենթամիավոր - ուժեղացնում է Ito[15]։ |
Բրուգադա համախտանիշի հետ կապված որոշ մուտացիաներ կարող են հանգեցնել նաև սրտի այլ հիվանդությունների։ Նրանք, ովքեր ունեն մեկից ավելի սրտային հիվանդություններ, որոնք առաջանում են միևնույն մուտացիայի հետևանքով համարվում են « համակցված համախտանիշ » կրողներ։ Այդպիսի համախտանիշի օրինակ է Բրուգադա և երկար QT համախտանիշները (LQT3), որոնք պայմանավորված են SCN5A-ի մուտացիայով, որը նվազեցնում է գագաթնային նատրիումական հոսքը, բայց միաժամանակ թողնում է մշտական հոսք[4]։ Նկարագրված է Բրուգադա համախտանիշի համակցումը աջ փորոքային առիթմոգեն կարդիոմիոպաթիայի հետ, որը առաջանում է PKP2 գենի մուտացիայի հետևանքով` առաջացնելով Բրուգադա համախտանիշին բնորոշ ԷՍԳ, սակայն ԱՓԱԿ-ին բնորոշ կառուցվածքային փոփոխություններ[16]։

Բրուգադա համախտանիշի ժամանակ դիտվող առիթմիաները սովորաբար այնպիսի վտանգավոր տիպեր են, ինչպիսիք են փորոքային ֆիբրիլյացիան կամ պոլիմորֆ փորոքային հաճախասրտությունը, սակայն Բրուգադա համախտանիշով հիվանդների մոտ հավանական է նաև հաճախասրտությունների ավելի քիչ վտանգավոր տիպերի առաջացումը, օրինակ՝ ԱՎ հանգուցային ռե-էնթրի հաճախասրտություն[17] կամ դանդաղասրտության առաջացումը, օրինակ՝ սինուսային հանգույցի դիսֆունկցիան[18]։ Կան մի քանի մեխանիզմներ, որոնցով այս համախտանիշի համար պատասխանատու գենետիկ մուտացիաները առաջացնում են վերոնշյալ առիթմիաները[19]։ Ոմանք պնդում են, որ դրանց առաջացման հիմնական պատճառը սրտի որոշ հատվածներում, հատկապես աջ փորոքում, էլեկտրական հաղորդականության դանդաղումն է։ Այս դանդաղ հաղորդումը թույլ է տալիս «կարճ օղակներին» ձևավորել, խոչընդոտում են որոշ հատվածներում էլեկտրական գրգիռի անցմանը՝ թույլ տալով անցնել այլ ուղղությամբ։ Այս երևույթը կարող է հիմք դառնալ ռե-էնթիրի մեխանիզմով առիթմիաների առաջացմանը[4]։ Նրանք, ովքեր կողմ են այս տեսակետին (հայտնի է, որպես ապաբևեռացման վարկած), պնդում են, որ դանդաղեցումը կարող է բացատրել, թե ինչու են Բրուգադա համախտանիշի հետ կապված առիթմիաները հակված առաջանալ միջին տարիքում[19]։
Մյուսները ենթադրում են, որ առիթմիաների հիմնական պատճառը սրտի ներքին (էնդոկարդի) և արտաքին (էպիկարդի) շերտերի միջև առկա էլեկտրական հատկությունների տարբերություն է (հայտնի է որպես վերաբևեռացման վարկած)[4]։ Սրտի կծկման ժամանակ յուրաքանչյուր բջջի էլեկտրական գործունեության ձևը (հայտնի է որպես գործողության պոտենցիալ) տարբերվում է էպիկարդի և էնդոկարդիի միջև։ Էպիկարդի բջիջներում գործողության պոտենցիալը ցույց է տալիս ակնհայտ վայրէջ հատված, նախնական վերելքից հետո։ Այս խորությունը շատ ավելի քիչ է երևում էնդոկարդիո բջիջներում։ Էնդոկարդի և էպիկարդի միջև տարբերությունը առավել հստակ երևում է աջ փորոքի շրջանում։ Բրուգադա համախտանիշի դեպքում այս տարբերությունները ավելի արտահայտված են`յուրաքանչյուր ցիկլի ընթացքում կարճ ժամանակով ստեղծելով էնդոկարդից դեպի էպիկարդ հոսք, ինչն էլ բերում է բնորոշ ԷՍԳ-ի առաջացմանը։ Էպի- և էնդոկարդի միջև էլեկտրական հատկությունների այս տարբերությունները նկարագրվում են որպես «վերաբևեռացման տրանսմուրալ դիսպերսիա», որը, եթե բավականաչափ մեծ է, կարող է հանգեցնել էլեկտրական ազդակների պաշարմանը որոշ շրջաններում։ Այս ամենն ի վերջո թույլ է տալիս գրգռման ալիքին, որը սովորաբար անցնում է մեկ ուղղությամբ, ճանապարհորդել մեկ կետի շուրջ և հիմք հանդիսանալ առիթմիաների առաջացմանը[4]։
Բրուգադա համախտանիշի ժամանակ առիթմիաների առաջացմանը նպաստող այլ գործոն է սրտի կառուցվածքի փոփոխությունները[19]։ Մինչ Բրուգադա համախտանիշ ունեցող մարդկանց սիրտը կարող է նորմալ երևալ, սպիացումը և ֆիբրոզը հաճախ հանդիպում են որոշակի շրջաններում, մասնավորապես աջ փորոքի արտատար տրակտում։ Քանի որ Բրուգադա համախտանիշը կարող է պայմանավորված լինել տարբեր գեների մուտացիաներով, հնարավոր է տարբեր մեխանիզմներ են պատասխանատու տարբեր հիվանդների առիթմիաների համար[19]։

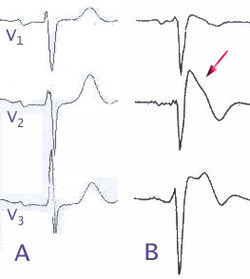
Բրուգադա համախտանիշը ախտորոշվում է ԷՍԳ բնորոշ փոփոխությունները հայտնաբերելու միջոցով[11]։ ԷՍԳ- ում հայտնաբերված փոփոխությունները ներառում են ST էլևացիա V1- V3 արտածումներում և Հիսի խրձի աջ ոտիկի պաշարում։ Կարող է լինել սրտի մեջ էլեկտրական հաղորդման դանդաղեցման վկայություն, որը ներկայանում է երկար PR միջակայքով։ Այս օրինաչափությունները կարող են միշտ առկա լինել, սակայն կարող են հայտնվել միայն որոշակի դեղերի օգտագործման դեպքում (տես ստորև), երբ մարդն ունի ջերմություն, ֆիզիկական ակտիվության ընթացքում կամ այլ խթանիչների արդյունքում։ ԷՍԳ պատկերը կարող է ավելի ակնհայտ դառնալ, երբ ԷՍԳ-ի ժամանակ որոշ էլեկտրոդներ տեղադրվում են սովորականից տարբեր դիրքերում[20]։
Բրուգադա ԷՍԳ-ի երեք ձևեր են նկարագրված[11]
Ներկայիս ուղեցույցների համաձայն, միայն 1-ին տիպի ԷՍԳ- ն (ի հայտ գալիս կամ ինքնաբուխ կամ դեղորայքի ազդեցությունից) կարող է օգտագործվել Բրուգադա համախտանիշ ախտորոշոум հաստատելու համար, քանի որ 2-րդ եւ 3-րդ տիպերը ոչ հազվադեպ երևում են առողջ մարդկանց մոտ[7]։
Որոշ դեղեր, մասնավորապես, հակառիթմիկ դեղամիջոցները, որոնք պաշարում են նատրիումական անցուղիները, կարող են հայտնաբերել 1-ին տիպի Բրուգադա պատկերը զգայուն մարդկանց մոտ։ Այս դեղերը կարող են օգնելո ախտորոշել Բրուգադա համախտանիշը կասկածելի մարդկանց մոտ (օրինակ՝ անբացատրելի սրտի կանգ տարածները, Բրուգադա համախտանիշով ընտանիքի անդամ ունեցողները), բայց ում մոտ չի հայտնաբերվել ախտորոշիչ ԷՍԳ- ն։ Այս դեպքերում նատրիումական անցուղիների պաշարիչները տրվում են վերահսկվող միջավայրում[20]։ Առավել հաճախ օգտագործվող դեղերն են այմալինը, ֆլեկաինիդը, և պրոկաինամիդը․ այմալինը կարող է լինել առավել արդյունավետ[21]։ Պետք է նախազգուշական միջոցներ ձեռնարկել այդ դեղերը կիրառելիս, քանի որ առիթմիայի առաջացման փոքր ռիսկ կա[20]։
Գենետիկ հետազոտությունները կարող են օգտակար լինել Բրուգադա համախտանիշով հիվանդների հայտնաբերման համար, առավել հաճախ, երբ ընտանիքում այս համախտանիշով անդամ կա, բայց երբեմն կատարվում է այն մարդու մոտ, ով մահացել է հանկարծակի և անսպասելիորեն[2]։ Այնուամենայնիվ, այս հետազոտության արդյունքների մեկնաբանումը դժվար է։ Ընտանիքում, որտեղ բոլորը կրում են հիվանդությունն առաջացնող նույն գեները, մի մասի մոտ նշանները կարող են արտահայտվել, մյուսների մոտ՝ ոչ[2]։ Սա նշանակում է, որ Բրուգադա համախտանիշի հետ կապված գենետիկական մուտացիայի կրումը պարտադիր պայման չէ անձի այդ հիվանդությամբ ախտահարված լինելու համար։ Բացի այդ, SCN5A գենի հաճախակի առաջացող մուտացիաներ որևէ խնդիր չեն առաջացնում[22]։
Ինվազիվ էլեկտրոֆիզիոլոգիական հետազոտությունները, որոնց ընթացքում հատուկ լարեր են անցկացվում երակի միջով և խթանվում ու գրանցվում է սրտի էլեկտրական ակտիվությունը, երբեմն կարող են օգտագործվել Բրուգադա համախտանիշով հիվանդի մոտ վտանգավոր առիթմիայի առաջացման ռիսկը[23]։ Ռիսկի ստրատիֆիկացումը կատարվում է նաև միջինացված ազդակով ԷՍԳ օգտագործելով[2]։ Ամբուլատոր ԷՍԳ մոնիտորինգը, ներառյալ շարունակական ձայնագրիչի իմպլանտացիան, երբեմն օգտագործվում են գնահատելու համար, թե արդյոք Բրուգադա համախտանիշ ունեցող անձի մոտ գլխապտույտը կամ ուշագնացությունը կապված են առիթմիայի հետ, թե կան այլ պատճառներ, օրինակ`վազովագալ սինկոպե[24]։

Բրուգադա համախտանիշի բուժման հիմնական նպատակն է հանկարծակի սրտային մահվան պատճառ հանդիսացող առիթմիաների վերացումը (փորոքային ֆիբրիլյացիա, պոլիմորֆ փորոքային հաճախասրտություն)[25]։ Քանզի այս հիվանդությամբ անձանց մի մասը ավելի մեծ ռիսկ ունի, նրանք ավելի ինտենսիվ միջոցառումների կարիք ունեն, իսկ մյուսները, ովքեր ունեն ավելի ցածր ռիսկ՝ ընդհակառակը[7]։ Բացի Բրուգադա համախտանիշ ունեցող անձի բուժումը, շատ կարևոր է հետազոտել նրանց ընտանիքի անդամներին`տեսնելու, թե արդյոք նրանք նույնպես ունեն հիվանդությունը[7]։
Բրուգադա համախտանիշի բոլոր կրողների մոտ, անկախ ռիսկից, առաջին գծի թերապիա է համարվում կենսակերպի փոփոխությունները[7]։ Մարդիկ պետք է իմանան և խուսափեն առիթմիաների ռիսկը բարձրացնող ակտիվություններից։ Այդ ակտիվությունների թվին են պատկանում ալկոհոլի չարաշահումը, որոշակի դեղամիջոցների կիրառումը[11] և պիտի իրականացվի տենդի անմիջապես բուժում պարացետամոլով[7]։ Թեև Բրուգադա համախտանիշի դեպքում առիթմիաները սովորաբար առաջանում են հանգստի կամ նույնիսկ քնի ժամանակ, որոշ մարդիկ ունենում են էպիզոդներ ֆիզիկական ծանրաբեռնվածության ժամանակ։ Որոշ բժիշկներ, հետևաբար, կարող են խորհուրդ տալ խուսափել ծանր ֆիզիկական լարվածությունից, իսկ ավելի մեղմ ֆիզիկական ակտիվությունը կարող է լինել օգտակար[26][27]։
Հանկարծակի սրտային մահվան բարձր ռիսկով անձանց ցուցված է կարդիովերտեր-դեֆիբրիլյատորի (ICD) իմպլանտացիան[7]։ Մաշկի տակ տեղադրվող այս փոքր սարքերը մշտապես վերահսկում են սրտի ռիթմը։ Եթե սարքը հայտնաբերում է կյանքին սպառնացող առիթմիա, այն սրտին փոքր էլեկտրական հարված է հասցնում և վերականգնում նորմալ ռիթմ[28]։ ICD- ն կարող է նաև գործել որպես ռիթմավար, որը կանխում է դանդաղասրտության էպիզոդները Բրուգադա համախտանիշով հիվանդների մոտ։
ICD-ի տեղադրումը համեմատաբար ցածր ռիսկային միջամտություն է և հաճախ կատարվում է տեղային անզգայացման պայմաններում[28]։ Այնուամենայնիվ, կարող են առաջանալ բարդություններ, ինչպիսիք են վարակը, արյունահոսությունը կամ ոչ անհրաժեշտ հարվածներ, որոնք երբեմն կարող են լուրջ լինել[29]։ Քանի որ ICD-ի տեղադրումը այնուամենայնիվ փոքր ռիսկային և սարքը թանկարժեք է, միջամտությունը կատարվում է միայն ՀՍՄ-ի բարձր ռիսկ ունեցող անձանց մոտ[7]։
Քինիդինը հակաառիթմիկ դեղամիջոց է, որը կարող է նվազեցնել Բրուգադա համախտանիշով որոշ մարդկանց մոտ առաջացած լուրջ առիթմիաների հավանականությունը[8][30]։ Այն առավել հաճախ օգտագործվում է ICD- ով մարդկանց մոտ, ովքեր ունեցել են վտանգավոր առիթմիաների մի քանի դրվագներ, բայց կարող են նաև բարձր ռիսկով, սակայն առանց տեղադրված ICD-իմարդկանց շրջանում[7]։
Իզոպրենալինը, որը նման է ադրենալինին, կարող է օգտագործվել Բրուգադա համախտանիշով այն մարդկանց շրջանում, ովքեր հաճախակի են ունենում կյանքին սպառնացող առիթմիաներ, որոնք հայտնի են որպես «էլեկտրական փոթորիկ»[7]։ Այս դեղը պետք է տրվի ներերակային անընդհատ ինֆուզիայի ձևով, հետևաբար, հարմար չէ երկարաժամկետ օգտագործման համար։
Բրուգադա համախտանիշի բուժման հաջորդ տարբերակը ռադիոհաճախային կաթետերային աբլյացիան է[31]։ Այս միջամտության ժամանակ լարերը անցկացնում են սրտի մեջ ոտքի երակով, կամ կրծոսկրի տակ գտնվող փոքր անցքով։ Այս լարերը օգտագործվում են սրտում առիթմիաների առաջացման համար պատասխանատու հատվածը հայտնաբերելու համար։ Այս լարերից մեկի ծայրը օգտագործվում է փոքրիկ այրվածքներ առաջացնելու համար, որոնք դիտավորությամբ վնասում են խնդիրն առաջացնող սրտի մասերը։ Ներկայիս ուղեցույցները ենթադրում են, որ այս բուժումը պետք է կիրառվի այն անձանց մոտ, ովքեր ICD-ից կրկնակի հարվածներ են ունեցել[7]։
Համախտանիշը հանդիպում է 10,000 մարդուց 1-30-ի մոտ։ Ավելի հաճախ հանդիպում է արական սեռի և ասիացիների մոտ[1]։ Չնայած տուժածները ծնվում են հիվանդությամբ, ախտանշանները սովորաբար արտահայտվում են միայն հասուն տարիքում։ Որոշ դեպքերում նշաններն արտահայտվում են մանկության շրջանում և արական ու իգական սեռի մոտ այս դեպքում հավասարաչափ են հանդիպում[32]։
Բրուգադա համախտանիշը ավելի տարածված է ասիական ծագում ունեցող մարդկանց շրջանում։ Թայլանդում և Լաոսում երիտասարդների շրջանում ՀՍՄ-ի ամենատարածված պատճառն է[33]։ Այդ երկրներում Բրուգադա համախտանիշը, ամենայն հավանականությամբ, պատասխանատու է հանկարծակի գիշերային մահացության համախտանիշի բազմաթիվ դեպքերի համար։ Տեղական անունները տարբեր են․ Ֆիլիպիններում, հիվանդությունը հայտնի է որպես «Բանգունգուտ», որը նշանակում է «ճիչ, որին հաջորդում է հանկարծակի մահը քնի ընթացքում»[33], իսկ Թաիլանդում այն հայտնի էր որպես Լայ Թայ, Ճապոնիայում՝ Պոկկուրի[34][35]։ Տիպ1 Բրուգադա համախտանիշի ԷՍԳ- ն ավելի հաճախ հանդիպում է ասիական բնակչության մեջ (0% - 0.36%), քան Եվրոպայում (0% - 0.25%) և ԱՄՆ-ում (0.03%): Նմանապես, Եվրոպայի (0.0% -0.6%) կամ ԱՄՆ- ի (0.02%) համեմատ, 2-րդ եւ 3-րդ տիպի ԷՍԳ-ն ավելի տարածված է Ասիայում (0.12% -2.23%)[36]։
Բրուգադա համախտանիշը անվանակոշվել է իսպանացի սրտաբաններ Պեդրո և Ջոզեփ Բրուգադաների պատվին, ովքեր և նկարագրել են համախտանիշը 1992 թվականին[9], թեև բնորոշ ԷՍԳ- ի և հանկարծակի սրտային մահվան կապը հայտնաբերվել է 1989 թվականին[37]։ Բրուգադա համախտանիշը 1997 թվականին նկարագրվել է որպես թայ տղամարդկանց հանկարծակի սրտային մահվան պատճառ[35]։ Համախտանիշի հետ կապված SCN5A գենի մուտացիաները առաջին անգամ հայտնաբերվել և նկարագրվել են Ռամոն Բրուգադայի կողմից 1998 թվականին[38]։ Հետագայում շատ այլ մուտացիաներ են հայտնաբերվել, որոնք ազդում են առնվազն 19 գեների վրա[12]։ 2000-ական թվականներին ուսումնասիրությունները հանգեցրին առիթմիաների առաջացման մեխանիզմների շուրջ մրցակցող տեսությունների առաջ քաշմանը[10]։ Հետազոտությունները շարունակվում են՝ բացահայտելով նոր գենետիկական տարբերակներ, ուսումնասիրելով մեխանիզմները և ավելի լավ բուժման մեթոդները[10]։
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.