ट्राइटियम
विकिपीडिया से, मुक्त विश्वकोश
ट्राइटियम हाइड्रोजन का एक रेडियोधर्मी समस्थानिक होता है। इसे ट्राइटॉन भी कहते हैं। ट्राइटियम के नाभिक में एक प्रोटॉन और दो न्यूट्रॉन होते हैं, जबकि हाइड्रोजन के सबसे प्रचुर मात्रा में उपलब्ध समस्थानिक प्रोटियम में मात्र एक प्रोटॉन ही होता है और न्यूट्रॉन अनुपस्थित होता है।[1] इस समस्थानिक का नाम एक ग्रीक शब्द से मिलकर बना है, जिसका अर्थ थर्ड या तृतीय होता है। ट्राइटियम की उत्पत्ति हैवी वाटर मॉडरेट रिएक्टर में ड्यूटीरियम माध्यम में न्यूट्रान के टकराव से होती है।[2] इस प्रक्रिया में कुछ मात्रा में ट्राइटियम बनता है। ट्राइटियम का आण्विक भार ३.०१६०४९२ होता है। मानक तापमान और दबाव पर ट्राइटियम गैस रूप में रहता है। ऑक्सीजन से मिश्रित होने पर यह ये तरल रूप धारण करता है, जिसे ट्राइटीकृत जल (ट्राइटिएटेड वाटर) कहते हैं। ये रबड़, प्लास्टिक और कुछ तरह के इस्पातों के लिए पारगम्य होता है।[1]
| ट्राइटियम | |
|---|---|
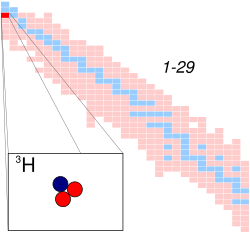 ट्राइटियम | |
| सामान्य | |
| नाम, चिह्न | ट्राइटियम, ट्राइटॉन,३H |
| न्यूट्रॉन | २ |
| प्रोटोन | १ |
| न्यूक्लाइड आंकड़े | |
| प्राकृतिक भंडार | ट्रेस |
| अर्धायु काल | ४,५००±८ दिन |
| क्षय उत्पाद | 3He |
| समस्थानिक द्रव्यमान | ३.०१६०४९२ u |
| स्पिन | १/२+ |
| एक्सेस ऊर्जा | १४,९४९.७९४± ०.००१ keV |
| बाइंडिंग ऊर्जा | ८,४८१.८२१± ०.००४ keV |
| क्षय मोड | क्षय ऊर्जा |
| बीटा उत्सर्जन | ०.०१८५९० MeV |
ट्राइटियम की खोज १९२० में वाल्टर रसेल ने की थी। वहीं विल्फर्ड एफ. लिबी ने यह खोज की थी कि ट्राइटियम का प्रयोग डेटिंग वाटर की तरह किया जा सकता है, जो मदिरा उत्पादन के लिए निर्माण किया जाता है। हाइड्रोजन की तरह ट्राइटियम को सीमाबद्ध नहीं किया जा सकता। ट्राइटियम और ड्यूटेरियम को परमाणु ईंधन की तरह प्रयोग किया जाता है।[3] वैज्ञानिकों के अनुसार ये चर्चा का विषय रहा है, कि ट्राइटियम को प्रस्तावित फ़्यूज़न रियेक्टरों[2] में अधिक मात्र में प्रयोग करने पर रेडियोधर्मी प्रदूषण संभव है।[4] विभिन्न देशों में ट्राइटियम के प्रयोग पर निषेध है।[1] सूर्य पर जो प्रक्रियाएँ होती हैं, उन में हाइड्रोजन के दोनों ड्यूटेरियम और ट्राइटियम के अणुओं के मेल से अधिक मात्रा में ऊर्जा पैदा होती है। ड्यूटेरियम और ट्राइटियम के एक ग्राम से उतनी ही ऊर्जा उत्पन होती है जितनी ८ टन तेल से पैदा की जा सकती है।[5]
ट्राइटियम लगभग हाइड्रोजन से मिलता जुलता होता है, जिसके कारण यह सरलता से मिलकर कार्बनिक बंध बना लेते हैं। ट्राइटियम बीटा का मजबूत उत्सर्जक नहीं है जिस कारण यह काफी खतरनाक होता है। खाना, पानी और त्वचा द्वारा अवशोषण किए जाने के कारण सांस लेने या खाना खाने के दौरान काफी हानिकारक होता है।
- ट्राईटियम डायल वाली घड़ी
- ट्राइटियम भरी ट्यूबलाइट
सन्दर्भ
बाहरी कड़ियाँ
Wikiwand - on
Seamless Wikipedia browsing. On steroids.

