Loading AI tools
מוויקיפדיה, האנציקלופדיה החופשית
בכימיה קוונטית ובמכניקת הקוונטים, הכלאת אורביטלים אטומיים (מכונה גם היברידיזציית אורביטלים) היא ערבוב של האורביטלים של אטומים היוצרים קשר כימי, כלומר מולקולה, זה עם זה.
האורביטלים, שהם מסלולי האלקטרונים במרחב, מתערבבים, או מכליאים האחד את השני, כדי ליצור אורביטלים חדשים שמתאימים למולקולה במקום האורביטלים הנפרדים שמתאימים לאטומים בודדים.
בניסוח פיזיקלי של מכניקת הקוונטים, האורביטלים המוכלאים הם המצבים העצמיים של המולקולה, במקום האורביטלים הנפרדים שהם המצבים העצמיים של האטומים.
אורביטל בכלל, ואורביטל אטומי בפרט, מייצג את ההסתברות של האלקטרון להימצא בנפח מסוים על פני זמן מסוים. לכן הכלאה אטומית היא חישוב מחדש של ההסתברויות הללו בהינתן הקשר הכימי המתגבש, מעיין יישום של חוק בייס לעולם הכימיה הקוונטית, כאשר הנתון הוא הקשר הכימי.
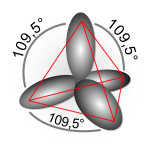
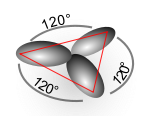
תיאור הכלאת אורביטלים משמש להבנת הקשר בין המבנה הגאומטרי של המולקולה, לבין פערי האנרגיה באורביטלים האלקטרוניים שלה.
הכלאה אורביטלית יעילה מאוד כשמדובר באורביטלים המתקבלים עבור אלקטרון לו תנע זוויתי נמוך, כלומר אורביטלי s ואורביטלי p.
כדי להיעזר בהכלאה אורביטלית להבנה מלאה של רמות האנרגיה במולקולה נדרש ידע מעמיק בתורת הקוונטים. עם זאת, ניתן להשתמש בה להבנת הצורה המולקולרית, והבנה חלקית של רמות האנרגיה על פי כמה כללים בסיסיים:

דוגמה טובה לכך היא מולקולת האֶתֶן, במולקולה זו כל אטום פחמן נקשר לשלשה אטומים אחרים משלושה כיוונים שונים, לכן כיווניותו שלוש, כלומר עליו להיעזר בשלושה אורביטלים ובארבעה אלקטרונים. עבור כל אטום פחמן ישנם שני קשרים יחידים וקשר כפול אחד. הקשר הכפול חייב להיווצר מהקבלה של אורביטלי פאי, ושני הקשרים היחידים נוצרים מחפיפה בין אורביטלי סיגמא.
מבט בטבלה המחזורית מגלה את ההערכות האלקטרונית של אטום פחמן במצב היסוד (לארבעת האלקטרונים העליונים)-
הכיווניות 3 לכן עלינו לערבב שלשה אורביטלים, כאשר לפחות אחד מהם חייב להיות s, ועל פי הנוסחה: (הכיווניות פחות אחת)×(אורביטלי P) + (אורביטליS) המדובר הוא בהכלאה בין שני אורביטלי p ואורביטל s אחד, נהוג לסמנה כ sp2. נוצרו שלושה אורביטלים חדשים, כל אחד מהם sp2. לידיעת אכלוס האלקטרונים בהם יש לדעת את גובה האנרגיה שלהם, שאותה ניתן לאמוד בעזרת חישובי תוחלת - משקלי אורביטלי ה p הוא שני שלישים, ומשקל אורביטל ה s הוא שליש לכן האנרגיה של האורביטלים המעורבבים היא: שליש מהאנרגיה של אורביטל s ועוד שני שלישים מהאנרגיה של אורביטל p.
כעת נוצרו שלושה אורביטלי sp2 נמוכים באנרגיה, ואורביטל P אחד נותר מעליהם באנרגיה, האכלוס החדש צריך להיות: sp2 2 sp2 1 sp2 1 p 0, אלא שכדי ליצור את הקשרים אחד האלקטרונים עובר עירור והתוצאה היא sp2 1 sp2 1 sp2 1 p 1
לכן מצאנו במולקולת אֶתֶן סביב אטום הפחמן- 3 קשרי סיגמא, כל אחד נוצר מחפיפה של אורביטלי sp2. וקשר פאי אחד, שנוצר מהקבלה בין שני אורבטלי 2p. וכן ניתן להעריך בצורה גסה את המאזן האנרגטי מההברידיזציה- לפני ההיברידיזציה היו שני אלקטרונים באורביטל s ו2 באורביטל p. אחריה היו 4 אלקטרונים בשני שלישים הדרך בין אורביטל s וp. כלומר 2 אלקטרונים טיפסו שני שלישים של הדרך, ושני אלקטרונים ירדו שליש הדרך, כלומר בסה"כ המולקולה הפסידה כמות אנרגיה הזהה לשני שלישים פער האנרגיה בין אורביטלי 2p ל 2s. (הרווח האנרגטי מתהליך זה, יתגלה בעת יצירת הקשר הכימי אז חפיפת האורביטלים תהפוך את התהליך לאקסותרמי).
| יש לפשט ערך זה: הערך מנוסח באופן טכני מדי, וקשה להבנה לקהל הרחב. | |
שימוש פשוט בתוצאות של התורה נעזר בכללי אצבע של הכלאה אורביטלית:
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.