
Tétraoxyde de xénon
composé chimique / De Wikipedia, l'encyclopédie encyclopedia
Le tétraoxyde de xénon est un solide cristallin de couleur jaune de formule XeO4 qui n'est stable qu'en dessous de −35,9 °C[2],[3] ; au-dessus de cette température, il se décompose en explosant pour libérer du xénon et de l'oxygène. Dans la molécule XeO4, le xénon est à l'état d'oxydation +8 tandis que l'oxygène est à l'état d'oxydation -2. L'oxygène est le seul élément connu à pouvoir porter le xénon à son état d'oxydation le plus élevé ; le fluor s'arrête à l'état +6 avec l'hexafluorure de xénon XeF6, sans doute pour des raisons d'encombrement stérique.
Faits en bref Identification, No CAS ...
| Tétraoxyde de xénon | |
 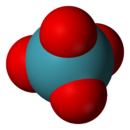 Structure du tétraoxyde de xénon |
|
| Identification | |
|---|---|
| No CAS | 12340-14-6 |
| Propriétés chimiques | |
| Formule | O4XeXeO4 |
| Masse molaire[1] | 195,291 ± 0,007 g/mol O 32,77 %, Xe 67,23 %, |
| Propriétés physiques | |
| T° fusion | −35,9 °C (explosion) |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Fermer