
Orthoformiate d'éthyle
composé chimique / De Wikipedia, l'encyclopédie encyclopedia
L'orthoformiate d'éthyle est l'orthoester triéthylique de l'acide formique. Il est facilement disponible commercialement mais il peut être aussi préparé par réaction entre du chloroforme (CHCl3) et l'éthanolate de sodium (NaC2H5O)[4]:
- CHCl3 + 3 Na + 3 EtOH → HC(OEt)3 + 3/2 H2 + 3 NaCl
Faits en bref Identification, Nom UICPA ...
| Orthoformiate d'éthyle | |||
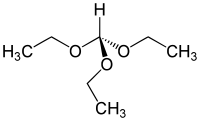
| |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | (diéthoxyméthoxy)éthane | ||
| Synonymes |
triéthoxyméthane, orthométhanoate d'éthyle |
||
| No CAS | 122-51-0 | ||
| No ECHA | 100.004.138 | ||
| No CE | 204-550-4 | ||
| No RTECS | RM6475000 | ||
| PubChem | 31214 | ||
| SMILES | |||
| InChI | |||
| Propriétés chimiques | |||
| Formule | C7H16O3 [Isomères] |
||
| Masse molaire[1] | 148,200 1 ± 0,007 6 g/mol C 56,73 %, H 10,88 %, O 32,39 %, |
||
| Propriétés physiques | |||
| T° fusion | −76 °C[2] | ||
| T° ébullition | 146 °C[2] | ||
| Masse volumique | 0,891 g·cm-3 à 25 °C[2] | ||
| Point d’éclair | 35 °C[2] | ||
| Pression de vapeur saturante | 2,9 mmHg (20 °C)[2] | ||
| Propriétés optiques | |||
| Indice de réfraction |  1,391[2] 1,391[2]
|
||
| Précautions | |||
| SGH[2],[3] | |||
| H226 et P210 H226 : Liquide et vapeurs inflammables P210 : Tenir à l’écart de la chaleur/des étincelles/des flammes nues/des surfaces chaudes. — Ne pas fumer. |
|||
| Transport | |||
Numéro ONU : 2524 : ORTHOFORMIATE D’ÉTHYLE Classe : 3 Étiquette :  3 : Liquides inflammables Emballage : Groupe d'emballage III : matières faiblement dangereuses. |
|||
| Écotoxicologie | |||
| DL50 | 7060 mg/kg (rat, oral)[3] | ||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
Fermer
L'orthoformiate d'éthyle sert, en chimie, de solvant et/ou de réactif comme dans la synthèse d'aldéhyde de Bodroux-Chichibabin[5] :
En chimie de coordination, l'orthoformiate d'éthyle est utilisé pour substituer l'eau des complexes métalliques aqueux par des molécules d'éthanol[6] :
- [Ni(H2O)6](BF4)2 + 6 HC(OC2H5)3 → [Ni(C2H5OH)6](BF4)2 + 6 HC(O)(OC2H5) + 6 HOC2H5

