
Méthylsilane
composé chimique / De Wikipedia, l'encyclopédie encyclopedia
Le méthylsilane est un composé chimique de formule SiH3CH3. Il s'agit d'un gaz incolore très inflammable et pyrophorique à l'odeur nauséeuse formant des mélanges explosifs avec l'air. Il peut être produit en quantité par la réaction du chlorosilane SiH3Cl avec un excès de diméthylzinc Zn(CH3)2, ce qui libère également du chlorure de méthylzinc ClZnCH3[3] :
Faits en bref Identification, Nom UICPA ...
| Méthylsilane | |||
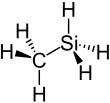  Structure du méthylsilane |
|||
| Identification | |||
|---|---|---|---|
| Nom UICPA | méthylsilane | ||
| No CAS | 992-94-9 | ||
| No ECHA | 100.012.362 | ||
| No CE | 213-598-5 | ||
| PubChem | 70434 | ||
| SMILES | |||
| InChI | |||
| Apparence | gaz incolore à l'odeur nauséeuse | ||
| Propriétés chimiques | |||
| Formule | CH6Si [Isomères] |
||
| Masse molaire[1] | 46,143 8 ± 0,001 5 g/mol C 26,03 %, H 13,11 %, Si 60,86 %, |
||
| Propriétés physiques | |||
| T° fusion | −156,8 °C[2] | ||
| T° ébullition | −57,5 °C[2] | ||
| Masse volumique | 0,628 g·cm-3[2] (liquide à −57,5 °C) |
||
| T° d'auto-inflammation | 160 °C[2] | ||
| Limites d’explosivité dans l’air | entre 1,3 % vol. (25 g·m-3) et 88,9 % vol. (1 735 g·m-3)[2] |
||
| Point critique | 79,3 °C et 4,37 MPa[2] | ||
| Point triple | −156,8 °C[2] (fusion) | ||
| Précautions | |||
| SGH[2] | |||
| H220 et H280 H220 : Gaz extrêmement inflammable H280 : Contient un gaz sous pression ; peut exploser sous l'effet de la chaleur |
|||
| Transport[2] | |||
Code Kemler : 23 : gaz inflammable Numéro ONU : 3161 : GAZ LIQUÉFIÉ INFLAMMABLE, N.S.A. Classe : 2.1 Étiquette :  2.1 : Gaz inflammables (correspond aux groupes désignés par un F majuscule); Emballage : - |
|||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
Fermer
La réaction du méthylsilane avec le cation silicium Si+ donne plusieurs composés organosiliciés actifs[4].
Le méthylsilane est par exemple utilisé pour l'épitaxie en phase vapeur aux organométalliques (MOVPE) de couches minces de carbure de silicium SiC dopé au germanium (Ge:SiC)[5].

