
Hexafluorure de sélénium
composé chimique / De Wikipedia, l'encyclopédie encyclopedia
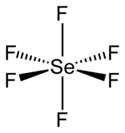
L'hexafluorure de sélénium est un composé chimique de formule SeF6. C'est un gaz incolore à l'odeur généralement décrite comme « repoussante ». Il s'agit d'une molécule hypervalente à géométrie octaédrique qui n'a pas d'application commerciale[2]. Les liaisons Se–F ont une longueur de 168,8 pm.
| Hexafluorure de sélénium | |||
| |||
| Structure de l'hexafluorure de sélénium | |||
| Identification | |||
|---|---|---|---|
| No CAS | 7783-79-1 | ||
| No ECHA | 100.149.506 | ||
| No CE | 620-577-8 | ||
| Apparence | gaz incolore à l'odeur âcre[1] | ||
| Propriétés physiques | |||
| T° fusion | −46,6 °C[1] (sublimation) | ||
| T° ébullition | −34,7 °C[1] (sous pression) | ||
| Masse volumique | 8,687 kg·m-3[1] | ||
| Point critique | 72,4 °C[1] | ||
| Point triple | −34,7 °C[1] | ||
| Précautions | |||
| SGH[1] | |||
| H280, H314, H330 et EUH071 H280 : Contient un gaz sous pression ; peut exploser sous l'effet de la chaleur H314 : Provoque de graves brûlures de la peau et des lésions oculaires H330 : Mortel par inhalation EUH071 : Corrosif pour les voies respiratoires |
|||
| Transport[1] | |||
Code Kemler : 268 : gaz toxique et corrosif Numéro ONU : 2194 : HEXAFLUORURE DE SÉLÉNIUM Classe : 2.3 Étiquettes :  2.3 : Gaz toxiques (correspond aux groupes désignés par un T majuscule, c'est-à-dire T, TF, TC, TO, TFC et TOC).  8 : Matières corrosives Emballage : - |
|||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
On peut obtenir du SeF6 à partir de sélénium et de fluor F2 ou en faisant réagir du dioxyde de sélénium SeO2 avec du trifluorure de brome BrF3. Le produit obtenu est ensuite purifié par sublimation.
La réactivité de l'hexafluorure de sélénium est intermédiaire entre celle de l'hexafluorure de tellure TeF6 et celle de l'hexafluorure de soufre SF6, ce dernier étant chimiquement inerte par rapport à l'hydrolyse jusqu'à haute température. Le SeF6 est également résistant à l'hydrolyse. Il peut traverser de l'hydroxyde de sodium NaOH ou de l'hydroxyde de potassium KOH à 10 % sans réagir, mais réagit avec l'ammoniac NH3 gazeux à 200 °C[3].


