From Wikipedia, the free encyclopedia
در ترمودینامیک، فرآیند همفشار یا فرآیند ایزوباریک فرآیندی است، که در آن فشار سیستم ثابت می ماند: . گرمای منتقل شده به سیستم کار انجام میدهد. این گرمای منتقل شده، انرژی داخلی () سیستم را نیز تغییر میدهد.

در این مقاله از قرارداد علامت فیزیکی برای کار استفاده میشود. طبق این قرارداد، کار مثبت توسط سیستم انجام می شود. با استفاده از این قرارداد، طبق قانون اول ترمودینامیک:
در این فرمول کار است، انرژی درونی است و گرما است.[1] کار انجام شده توسط سیستم بسته، به صورت زیر تعریف می شود:
در روابط d نشان دهنده دیفرانسیل است، درحالیکه Δ به معنای تغییر در کل فرآیند است. از آنجا که فشار ثابت است:
با استفاده از قانون گازهای ایده آل، رابطهی زیر به دست میآید:

نشان دهنده ثابت گازها و نشان دهنده مقدار ماده است. فرض میشود که در طی فرآیند ثابت باقی میماند. (به عنوان مثال، هیچ انتقال فاز در طی واکنش شیمیایی وجود ندارد) با توجه به قضیه همپاری،[2] تغییر در انرژی داخلی توسط رابطهی زیر، به دمای سیستم مربوط میشود.
بهطوریکه ، ظرفیت گرمایی مولی در یک حجم ثابت است.
جایگزینی دو معادله آخر در اولین معادله، معادلههای زیر را تولید میکند:
که در آن ظرفیت گرمایی مولی در فشار ثابت است.
برای یافتن ظرفیت گرمایی مولی ویژه گاز درگیر، معادلات زیر برای هر گاز عمومی که از نظر کالری کامل باشد، اعمال می شود. خاصیت γ، شاخص آدیاباتیک یا نسبت ظرفیت گرمایی نامیده می شود. برخی از منابع منتشر شده ممکن است به جای γ از k استفاده کنند.
گرمای ویژه مولی فرآیند همحجم:
گرمای ویژه مولی همفشار:
مقادیر γ برای گازهای دواتمی مانند هوا و اجزای اصلی آن و برای گازهای تکاتمی مانند گازهای نجیب است. فرمول های مربوط به گرماهای ویژه در این موارد خاص به این صورت است:
تکاتمی:
و
دواتمی:
و
یک روند همفشار در نمودار P-V با یک خط افقی مستقیم نشان داده شده است. این خط حالات ترموستاتیک اولیه و نهایی را به هم متصل می کند. اگر فرآیند به سمت راست حرکت کند،فرآیند گسترش است. اگر فرآیند به سمت چپ حرکت کند، یک فرآیند فشرده سازی است.
انگیزه علامت گزاری قراردادی مشخص، برای کمیت های ترمودینامیکی، از توسعه اولیه موتورهای حرارتی ناشی می شود. هنگام طراحی موتور حرارتی، هدف این است، که سیستم کار تولید کند. منبع انرژی در یک موتور حرارتی، یک ورودی گرم است.
یک فرآیند همحجم با معادله توصیف میشود. تغییر یافتهی این معادله برای فرآیند همفشار به صورت زیر خواهد بود. با جایگزینی معادله دوم در معادله اول:
کمیت یک تابع حالت است. این تابع با نام آنتالپی شناخته شده است و با حرف H نشان داده میشود. بنابراین،معادله یک فرآیند همفشار را می توان به طور خلاصه تر به این صورت نمایش داد:
آنتالپی و ظرفیت گرمایی ویژه حجمی، کمیتهای ریاضی بسیار مفیدی هستند، زیرا هنگام تجزیه و تحلیل یک فرآیند در یک سیستم باز، هنگامی که فشار سیال ثابت است، وضعیت کار صفری، اتفاق می افتد. در یک سیستم باز، آنتالپی مقداری است که استفاده از آن برای پیگیری محتوای انرژی مایع مفید است.
انبساط برگشتپذیر یک گاز ایدهآل میتواند به عنوان نمونهای از فرآیند همفشار در نظر گرفته شود.[3] هنگامی که انبساط گاز کار / گاز اطراف در فشارهای مختلف انجام میشود، نحوه تبدیل گرما به کار مورد توجه خاصی قرار میگیرد.
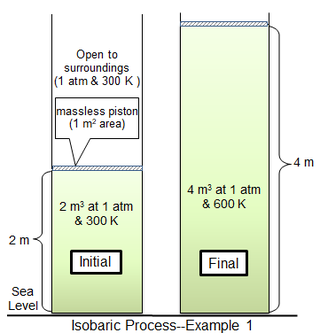
در مثال فرآیند اول، یک محفظه استوانهای با مساحت ، مول از یک گاز دواتمی ایدهآل با جرم مولکولی در را محصور کرده است. گاز اطراف آن در فشار و دمای است و از گاز درون سیلندر، توسط یک پیستون نازک جدا شده است. برای نمونه پیستون بدون جرم محدود، گاز سیلندر نیز در فشار است، با حجم اولیه . گرما به آرامی اضافه می شود، تا دمای گاز به طور یکنواخت بشود، پس از آن حجم گاز و پیستون متر بالاتر از موقعیت اولیه است. اگر حرکت پیستون به اندازه کافی آهسته باشد، فشار گاز در هر لحظه در کل فرآیند مقدار یکسانی () دارد.
برای یک گاز دواتمی کامل، ظرفیت گرمایی ویژه مولی در فشار ثابت ، یا است. ظرفیت گرمایی مولی در حجم ثابت ، یا است. نسبت از دو ظرفیت گرمایی است.[4]
گرمای مورد نیاز برای رساندن گاز از به :
میزان افزایش انرژی داخلی:
پس
سپس به روابط زیر میرسیم:
، که البته با تفاوت بین و یکسان است.
در اینجا، کار با گسترش علیه محیط اطراف کاملاً مصرف می شود. از کل گرمای اعمال شده () ، کار انجام شده () حدود از گرمای تامین شده است.

نمونه فرآیند دوم مشابه نمونه اول است، با این تفاوت که پیستون بدون جرم با یک پیستون با جرم جایگزین میشود، که فشار گاز سیلندر را تا دو برابر می کند و به میرساند. در دمای اولیه ( ) ، حجم گاز سیلندر است. گرما به آرامی اضافه میشود، تا دمای گاز به طور یکنواخت بشود، پس از آن حجم گاز و پیستون بالاتر از موقعیت اولیه است. اگر حرکت پیستون به اندازه کافی آهسته باشد، فشار گاز در هر لحظه در کل فرآیند تقریباً همان مقدار ( ) را دارد.
از آنجا که آنتالپی و انرژی داخلی مستقل از فشار هستند:
مانند مثال اول، حدود از گرمای تولید شده، به کار تبدیل می شود. اما در اینجا، کار به دو روش مختلف اعمال می شود: بخشی با گسترش جو اطراف و بخشی با بلند کردن پیستون کیلوگرمی تا فاصله .[5]
بنابراین، نیمی از کار توده پیستون را بلند میکند (کار جاذبه یا کار اعمال شده) ، در حالی که نیمی دیگر محیط را گسترش میدهد.
نتایج این دو نمونه فرآیند تفاوت بین کسری از گرما را، که به کار قابل استفاده تبدیل می شود () در مقابل کسری از گرما که به کار در برابر جو اطراف تبدیل شده، نشان می دهد. با نزدیک شدن فشار گاز انجامدهنده کار، به فشار محیط اطراف کار قابل استفاده به صفر می رسد، در حالی که حداکثر کار قابل استفاده در صورت عدم وجود فشار گاز اطراف به دست میآید. نسبت تمام کار انجام شده، به گرمای ورودی برای انبساط گاز ایدهآل طی فرآیند همفشار:
مقدار جرم () گاز در یک حجم در حال تغییر، باعث تغییر در چگالی () میشود. در این زمینه قانون ایده آل گاز نوشته شده است:
که در آن دمای ترمودینامیکی و جرم مولی است. وقتی و به صورت ثابت در نظر گرفته شوند، فشار می تواند ثابت بماند، زیرا ربع دمای چگالی () تحت یک نقشه برداری فشاری قرار میگیرد.[6]
صفت "همفشار(isobaric)" از کلمات یونانی ἴσος'' ('' isos '') به معنای "برابر" و βάρος (''baros'') به معنی "وزن" گرفته شده است.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.