From Wikipedia, the free encyclopedia
پیل الکتروشیمیایی (به انگلیسی: Electrochemical cell) پیلی است که در آن در اثر واکنش شیمیایی، جریان الکتریکی تولید میشود یا واکنشی شیمیایی بوسیله انرژی الکتریکی انجام میشود. باتریهای ۵/۱ ولت معمولی نمونهای از یک پیل الکتروشیمیاییاند. (گرچه که به بیان درستتر یک پیل گالوانیکاند.)
این مقاله نیازمند بررسی توسط یک متخصص است. لطفاً پارامتر دلیل یا بحث در این الگو را برای مشخصکردن مشکل مقاله استفاده کنید. |
این مقاله به هیچ منبع و مرجعی استناد نمیکند. |
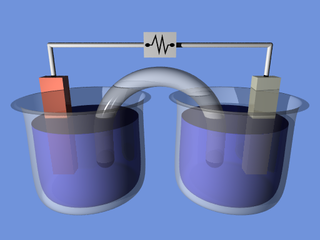
پیل الکتروشیمیایی چهار بخش دارد:
آند: که در آن واکنش آندی رخ میدهد.
کاتد: که در ان واکنش کاتدی رخ میدهد. کاتد بخشی از سطح است که هدایت الکتریکیاش بالا باشد وقابلیت انجام واکنش آن بالا باشد. برای مثال در چدن خاکستری گرافیتهای سطح کاتداند.
الکترولیت: که برای رخ دادن واکنش بین آند و کاتد است و باید هدایت الکتریکیاش بالا باشد. الکترولیت میتواند محلول ۰۰۰۱/۰ نمک خوراکی یا محلول نمکین آب دریا باشد.
پل: که بین آند و کاتد اتصال الکتریکی برای جابجایی الکترون برقرار میکند.
در پیل الکتروشیمیایی بایستی سرعت زایش و گیرش الکترون برابر باشد.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.