From Wikipedia, the free encyclopedia
Keemias on reaktsioonikoordinaat abstraktne ettekujutus reaktsiooni kulgemise teest lähteainetelt produktideni. Enamasti kujutatakse reageeriva süsteemi energia muutust protsessi kulgemise käigus piki reaktsiooni teed.

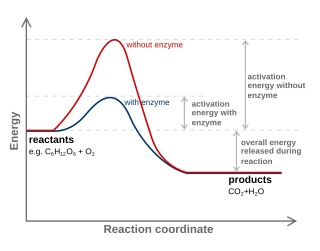
Reaktsioonis esinevat energiataseme muutust kujutatakse energiadiagrammidel: vertikaalteljel on süsteemi vaba energia ja horisontaaltelg – nimetatakse reaktsioonikoordinaat – kujutab reaktsiooni teed lähteainetest üle siirdeseisundi produktideni. Siirdeseisund on reaktsioonis kõrgeima energiaga olek.
Paremal olevatel diagrammidel on esitatud kaks erinevat tüüpi reaktsiooni: a) kaheastmeline reaktsioon, kus teises astmes saab moodustuda kaks isomeerset produkti, ja b) katalüütilise (siin ensüümkatalüüs) reaktsiooni võrdlus mittekatalüütilisega (näidatud on ka aktiveerimisenergia ensüümiga ja ilma ning protsessis vabanev energia).
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.