Mutación genética
De Wikipedia, la enciclopedia libre
En genética, se denomina mutación genética, mutación molecular o mutación puntual a los cambios que alteran la secuencia de nucleótidos del ADN. Estas mutaciones en la secuencia del ADN pueden llevar a la sustitución de aminoácidos en las proteínas resultantes. Un cambio en un solo aminoácido puede no ser importante si es conservativo y ocurre fuera del sitio activo de la proteína. De lo contrario, puede tener consecuencias severas, como por ejemplo:
- La sustitución de valina por ácido glutámico en la posición 6 de la cadena polipéptidica de la beta-globina da lugar a la enfermedad anemia de células falciformes en individuos homocigóticos, debido a que la cadena modificada tiene tendencia a cristalizar a bajas concentraciones de oxígeno.
- Las proteínas del colágeno constituyen una familia de moléculas estructuralmente relacionadas que son vitales para la integridad de muchos tejidos, incluidos los huesos y la piel. La molécula madura del colágeno está compuesta por tres cadenas polipeptídicas unidas en una triple hélice. Las cadenas se asocian primero por su extremo C-terminal y luego se enroscan hacia el extremo N-terminal. Para lograr este plegado, las cadenas de colágeno tienen una estructura repetitiva de tres aminoácidos: glicina - X - Y (X es generalmente prolina y Y puede ser cualquiera de un gran rango de aminoácidos). Una mutación puntual que cambie un solo aminoácido puede distorsionar la asociación de las cadenas por su extremo C-terminal evitando la formación de la triple hélice, lo que puede tener consecuencias graves. Una cadena mutante puede evitar la formación de la triple hélice, aun cuando haya dos monómeros de tipo salvaje. Al no tratarse de una enzima, la pequeña cantidad de colágeno funcional producido no puede ser regulada. La consecuencia puede ser la condición dominante letal osteogénesis imperfecta.

Entre las mutaciones genéticas, es posible distinguir varios factores:
- Mutación silenciosa o sinónima: Cuando no cambia la secuencia de aminoácidos de la cadena polipéptidica. Los cambios en el nucleótido no generan cambios estructurales o funcionales de la proteína.

- Mutación puntual, por sustitución de bases: Se producen al cambiar en una posición un par de bases por otro (son las bases nitrogenadas las que distinguen los nucleótidos de una cadena). Se distinguen dos tipos que se producen por diferentes mecanismos bioquímicos:
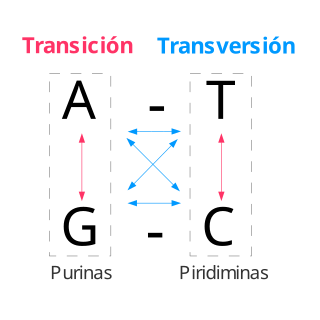
- Mutaciones transicionales o simplemente transiciones, cuando un par de bases es sustituido por su alternativa del mismo tipo. Las dos bases púricas son adenina (A) y guanina (G), y las dos pirimídicas son citosina (C) y timina (T). La sustitución de un par AT, por ejemplo, por un par GC, sería una transición.
- Mutaciones transversionales o transversiones, cuando un par de bases se sustituye por otra del otro tipo. Por ejemplo, la sustitución del par AT por TA o por CG.
- Mutación no sinónima: Cuando los cambios en las bases dan lugar a un nuevo aminoácido, generando cambios estructurales o funcionales en la secuencia de la proteína. Las expansiones clonales, que presentan una gran influencia en el desarrollo de enfermedades como el cáncer, suelen identificarse mediante la secuenciación en profundidad de un panel de genes asociados al cáncer. Sin embargo, los paneles suelen estar diseñados para detectar mejor las variantes de un solo nucleótido (SNV) por lo que muchas mutaciones no sinónimas que conducen a expansiones clonales no son detectadas por esta técnica. Para intentar cuantificar la pérdida de detección de mutaciones no sinónimas, se están desarrollando marcos genéticos poblacionales.[1]
- Mutación nula: Cuando afecta al centro activo o a un sitio cercano a este, provocando la posible falta de función. Si las mutaciones afectan a regiones menos críticas de una proteína, su efecto será probablemente menos grave, generando con frecuencia mutantes rezumantes o parcialmente inactivos.
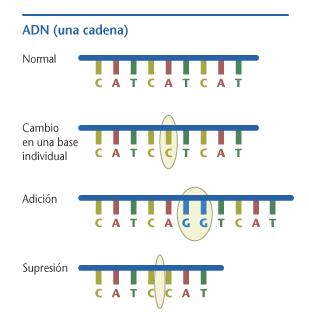
- Mutaciones de corrimiento o desfase: Cuando se añaden o se quitan pares de nucleótidos alterándose la longitud de la cadena. Si se añaden o se quitan pares en un número que no sea múltiplo de tres (es decir, si no se trata de un número exacto de codones), las consecuencias serán especialmente graves, porque a partir de ese punto, y no solo en él, toda la información quedará alterada. Hay dos casos llamados "indels":
- Mutación por deleción de nucleótidos: En la secuencia de nucleótidos se pierde uno y la cadena se acorta en una unidad.
- Mutación por inserción de nuevos nucleótidos: Dentro de la secuencia del ADN se introducen nucleótidos adicionales, interpuestos entre los que ya había, alargándose correspondientemente la cadena.
Además, pueden dar lugar a mutaciones sin sentido si se introduce un codón de terminación.
- Mutaciones en los sitios de corte y empalme (splicing)
Las mutaciones de corrimiento del marco de lectura también pueden surgir por mutaciones que interfieren con el splicing del ARN mensajero. El comienzo y final de cada intrón en un gen están definidos por secuencias conservadas de ADN. Si un nucleótido muta en una de las posiciones altamente conservada, el sitio no funcionará más, con las consecuencias predecibles para el ARNm maduro y la proteína codificada.
Hay muchos ejemplos de estas mutaciones, por ejemplo, algunas mutaciones en el gen de la beta globina en la beta talasemia son causadas por mutaciones de los sitios de splicing.se denomina mutación genética, mutación molecular o mutación puntual a los cambios que alteran la secuencia de nucleótidos del ADN. No se debe confundir con mutación génica, que se refiere a una mutación dentro de un gen. Estas mutaciones en la secuencia del ADN pueden llevar a la sustitución de aminoácidos en las proteínas resultantes. Un cambio en un solo aminoácido puede no ser importante si es conservativo y ocurre fuera del sitio activo de la proteína. De lo contrario, puede tener consecuencias graves, como por ejemplo:
La sustitución de valina por ácido glutámico en la posición 6 de la cadena polipéptidica de la beta-globina da lugar a la enfermedad anemia de células falciformes en individuos homocigóticos debido a que la cadena modificada tiene tendencia a cristalizar a bajas concentraciones de oxígeno.
Las proteínas del colágeno constituyen una familia de moléculas estructuralmente relacionadas que son vitales para la integridad de muchos tejidos, incluidos los huesos y la piel. La molécula madura del colágeno está compuesta por tres cadenas.
Mutaciones y cáncer
Resumir
Contexto
Algunos cánceres parecen desarrollarse sin mutaciones que afecten a genes conductores conocidos, lo que sugiere que podría haber un gran número de impulsores que son raros individualmente, por lo que no se están detectando vía los paneles génicos de secuenciación, pero comunes en conjunto.[1]
El análisis de los VAF, del inglés Variant allele frequency, permite desentrañar la selección de la mutación y no están restringidos a los genes, al contrario de lo que sucede en los métodos de detección de paneles de genes por ejemplo. La mayoría de las variantes sinónimas alcanzan alto VAF debido al autostopismo genético. Sin embargo, este análisis requiere que un gran número de individuos compartan la misma mutación para lograr estimaciones precisas. Por lo tanto, la estimación de los niveles totales de selección positiva de mutaciones que ocurren fuera de los genes habitualmente afectados utilizando los métodos existentes es un reto.[1]
En un estudio llevado a cabo por Poon, G.Y.P., Watson, C.J., Fisher, D.S. et al., se desarrolla un marco genético poblacional que utiliza la distribución de los VAF de las variantes sinónimas para cuantificar cuánta selección positiva queda sin explicar por las mutaciones en los genes conductores del cáncer canónicos.[1]
Bibliografía
- Alberts, Bruce, et al. Molecular Biology of the Cell, 4th ed. New York: Garland Publishing, 2000.
- Atherly, Alan G., Jack R. Girton, and John F. McDonald. The Science of Genetics. Philadelphia, PA: Saunders College Publishing, 1998.
- Cooper, D. N. Human Gene Mutation. Bios Scientific Publishers Ltd., 1999.
- Griffiths Anthony J. F., William M. Gelbart, Jeffrey H. Miller and Richard Lewontin (1999).Mutational Analysis. In Modern Genetic Analysis. W. H. Freeman and Company ISBN 0-7167-3597-0.
- Griffiths Anthony J. F., William M. Gelbart, Jeffrey H. Miller and Richard Lewontin (1999).The Molecular Basis of Mutation. In Modern Genetic Analysis. W. H. Freeman and Company ISBN 0-7167-3597-0.
- Griffiths A., Miller J., Suzuki D., Lewontin R. and Gelbart W. Genética, 7a edición. Madrid: McGraw-Hill (2002).
Referencias
Enlaces externos
Wikiwand - on
Seamless Wikipedia browsing. On steroids.