
Nicotinamida adenina dinucleótido
compuesto químico / De Wikipedia, la enciclopedia encyclopedia
Estimado Wikiwand AI, Seamos breves simplemente respondiendo estas preguntas clave:
¿Puede enumerar los principales datos y estadísticas sobre NADH?
Resumir este artículo para un niño de 10 años
El dinucleótido de nicotinamida y adenina, también conocido como nicotin adenin dinucleótido o nicotinamida adenina dinucleótido (abreviado NAD+ en su forma oxidada y NADH en su forma reducida), es una coenzima que se halla en las células vivas y que está compuesta por un dinucleótido, es decir, por dos nucleótidos, unidos a través de grupos fosfatos: uno de ellos es una base de adenina y el otro, una nicotinamida. Su función principal es el intercambio de electrones y protones y la producción de energía de todas las células.[cita requerida]
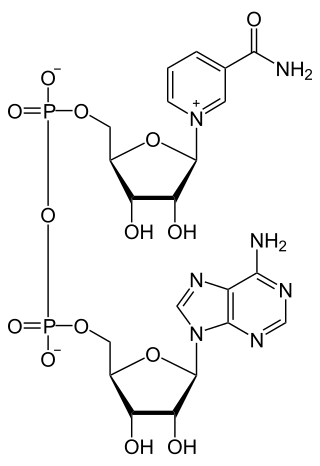 Fórmula química | ||
| Nombre IUPAC | ||
|
NAD+ | ||
| General | ||
| Otros nombres |
Difosfopiridina nucleótido (DPN+ ), Coenzima I. | |
| Fórmula estructural | Ver imagen | |
| Fórmula molecular |
C 21H 27N 7O 14P 2 | |
| Identificadores | ||
| Número CAS |
53-84-9 58-68-4 (NADH)[1] | |
| Número RTECS | UU3450000 | |
| ChEBI | 13389 | |
| ChemSpider | 5681 | |
| DrugBank | DB14128 | |
| PubChem | 925 | |
| UNII | 0U46U6E8UK | |
| Propiedades físicas | ||
| Apariencia | Polvo blanco | |
| Masa molar | 663,43 g/mol | |
| Punto de fusión | 333 K (60 °C) | |
| Peligrosidad | ||
| NFPA 704 |
1
1
0
| |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
En el metabolismo, el NAD+
está implicado en reacciones de reducción-oxidación, llevando los electrones de una a otra. Debido a esto, la coenzima se encuentra en dos formas: como un agente oxidante, que acepta electrones de otras moléculas. Actuando de ese modo da como resultado la segunda forma de la coenzima, el NADH, la especie reducida del NAD+
, y puede ser usado como agente reductor para donar electrones. Las reacciones de transferencia de electrones son la principal función del NAD+
, que también se emplea en otros procesos celulares, siendo el más notable su actuación como sustrato de enzimas que adicionan o eliminan grupos químicos de las proteínas en las modificaciones postraduccionales. Debido a la importancia de estas funciones, las enzimas involucradas en el metabolismo del NAD+
son objetivos para el descubrimiento de fármacos.
Desde un punto de vista económico, el elevado precio del NADH/NAD+ suele ser una desventaja en el uso de enzimas dependientes de cofactores en procesos biotecnológicos industriales. Por lo tanto, el desarrollo de cofactores biomiméticos sintéticos baratos es una tarea de investigación de importancia estratégica[2][3].
En los organismos, el NAD+
puede ser sintetizado a partir de biomoléculas sencillas como los aminoácidos de triptófano o ácido aspártico. Como alternativa, se pueden obtener componentes más completos de la coenzima a partir de los alimentos, como la vitamina llamada niacina. Asimismo, se conocen compuestos similares que provienen de las reacciones que descomponen la estructura del NAD+
. Estos componentes preformados pasan entonces a través de un camino de rescate que los recicla de nuevo a la forma activa. Parte del NAD+
se convierte también en nicotinamida adenina dinucleótido fosfato (NADP+
); la química de estas coenzimas relacionadas es similar a la del NAD+
, pero tiene diferentes papeles en el metabolismo.
