
Glutatión
compuesto químico / De Wikipedia, la enciclopedia encyclopedia
Estimado Wikiwand AI, Seamos breves simplemente respondiendo estas preguntas clave:
¿Puede enumerar los principales datos y estadísticas sobre Glutation?
Resumir este artículo para un niño de 10 años
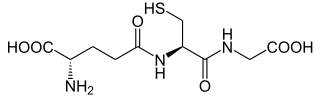
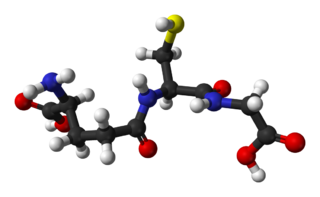
El glutatión (también glutationa) (GSH)[2] es un tripéptido constituido por los aminoácidos glutamato, cisteína y glicina. Contiene un enlace peptídico inusual entre el grupo amino de la cisteína y el grupo carboxilo de la cadena lateral del glutamato.
Se trata del principal antioxidante de las células, es ubicuo y ayuda a protegerlas de las especies reactivas del oxígeno, como los radicales libres y los peróxidos.[3]
La reducción de GSh es un péptido molecular pequeño. Una gran cantidad de péptidos en los organismos vivos, especialmente en las células hepáticas, protegen la membrana de las células hepáticas, promueven el ejercicio de la actividad de las enzimas hepáticas y se combinan con una variedad de productos químicos tóxicos para desintoxicar.[4] Es nucleofílico en azufre y ataca los aceptores conjugados electrofílicos venenosos. Los grupos tiol se mantienen en un estado reducido a una concentración de aproximadamente ~ 5 mM en células animales. En efecto, el glutatión reduce cualquier enlace disulfuro formado dentro de proteínas citoplasmáticas de cisteínas, al actuar como un donante de electrones. En el proceso, el glutatión se convierte en su forma oxidada, llamada disulfuro de glutatión (GSSG). En las células, el glutatión se encuentra principalmente en su estado reducido (GSH) y, en mucha menor proporción, en su estado oxidado (GSSG).
 | ||
 | ||
| Nombre IUPAC | ||
| Ácido(2S)-2-Amino-4-{[(1R)-1-[(carboximetil)carbamoil]-2-sulfaniletil]carbamoil}butanoico | ||
| General | ||
| Fórmula estructural |
| |
| Fórmula molecular | C10H17N3O6S | |
| Identificadores | ||
| Número CAS | 70-18-8[1] | |
| ChEBI | 60836 | |
| ChEMBL | 1543 | |
| ChemSpider | 111188 | |
| DrugBank | DB00143 | |
| PubChem | 124886 | |
| UNII | GAN16C9B8O | |
| KEGG | C00051 | |
|
C(CC(=O)N[C@@H](CS)C(=O)NCC(=O)O)[C@@H](C(=O)O)N
| ||
| Propiedades físicas | ||
| Masa molar | 307,084 g/mol | |

Ello es así ya que la enzima que "reduce" el tripéptido a partir de su forma oxidada, la glutatión reductasa, es constitutivamente activa e inducible en situaciones de estrés oxidativo. De hecho, la proporción GSH/GSSG dentro de las células se utiliza a menudo como "indicador" del estado oxidativo de la célula y de la toxicidad celular.[5]
- H2O2 + 2GSH------- GSSG + 2 H2O