Loading AI tools
La cinética de Michaelis-Menten describe la velocidad de reacción de muchas reacciones enzimáticas. Recibe este nombre en honor a Leonor Michaelis y Maude Menten. Este modelo sólo es válido cuando la concentración del sustrato es mayor que la concentración de la enzima, y para condiciones de estado estacionario, es decir, cuando la concentración del complejo enzima-sustrato es constante.
Para determinar la velocidad máxima de una reacción enzimática, la concentración de sustrato ([S]) se aumenta hasta alcanzar una velocidad constante de formación de producto. Esa es la velocidad máxima (Vmax) de la enzima. En ese caso los sitios activos de la enzima están saturados con sustrato.
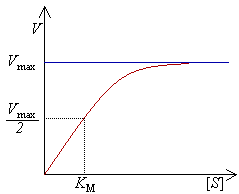
Diagrama de velocidad de reacción y constante de Michaelis-Menten.
La velocidad V indica el número de moléculas del sustrato que se convierten en producto por segundo. Con concentraciones crecientes de sustrato[S], la enzima va acercándose asintóticamente a su velocidad máxima Vmax, pero nunca la alcanza. Por esta razón, no hay un valor de [S] determinado para la Vmax. De todas formas, se puede definir un parámetro característico de la enzima empleando la concentración de sustrato a la cual se alcanza la mitad de la velocidad máxima (Vmax/2). Podemos resumir el significado de Vmax con las siguientes afirmaciones:[1][2]
- Corresponde al límite superior de la velocidad de reacción.
- Equivale al producto kcat*[E]t
- Permite inferir la concentración de enzima inicial
- Se obtiene gráficamente
- Graficando v vs. [S] es difícil encontrar V manualmente, por lo que se necesita usar un método de ajuste no lineal de los puntos experimentales.
Aunque es imposible medir exactamente la concentración de sustrato que da Vmax, las enzimas pueden caracterizarse mediante la concentración de sustrato a la cual la velocidad de reacción es la mitad de la velocidad máxima. Esta concentración de sustrato se conoce como constante de Michaelis-Menten (KM). Para enzimas que exhiben una cinética de Michaelis-Menten simple esta constante representa la constante de disociación del complejo enzima-sustrato (ES) (o la inversa de la afinidad entre enzima y sustrato). Valores bajos indican que el complejo ES está unido muy fuertemente y raramente se disocia sin que el sustrato reaccione para dar producto. En estos casos se obtendrá una KM diferente según el sustrato específico sobre el que actúe la enzima (como sucede en el caso de enzimas que actúan sobre sustratos análogos) y según las condiciones de reacción en que se realicen las mediciones.[3]
El significado de km se puede resumir en las siguientes afirmaciones:[1][2]
- Se expresa en unidades de concentración
- Numéricamente corresponde a la concentración a la que se alcanza el 50% de saturación de la enzima
- Está relacionada con la afinidad, es decir, la fuerza de unión entre la enzima y su sustrato. Valores grandes de km significan poca afinidad, mientras que valores pequeños de km (usualmente menores al rango milimolar) corresponden a una afinidad alta de la enzima por el sustrato.
- Es una constante aparente de disociación del complejo enzima - sustrato (E·S).
Nota: KM solo se puede usar para determinar la afinidad de una enzima por un sustrato, k2 es limitante de la velocidad, por ejemplo, si k2 << k-1 y KM se convierte en k-1/k1. Generalmente, k2 >> k-1 o bien k2 y k-1 son comparables.
La derivación de Michaelis y Menten está descrita por Briggs y Haldane. Se obtiene de la siguiente manera:
Se supone que la reacción enzimática es irreversible, y que el producto no se liga con la enzima después de la reacción.
Siguiendo la aproximación del estado estacionario, que señala que la concentración del complejo enzima-sustrato () es pequeña y se mantiene casi constante a lo largo de la reacción enzimática:
Se define:
Entonces:
(1)
La velocidad de reacción es:
(2)
La concentración total de la enzima:
Por lo tanto:
(3)
Sustituyendo (3) en (1) da:
Reordenando:
(4)
Sustituyendo (4) en (2) :
Esta ecuación se puede analizar experimentalmente con un diagrama de Lineweaver-Burke, un diagrama de Eadie-Hofstee o un diagrama de Hanes-Woolf.
- es el total de enzima. No es práctico medir la cantidad de complejo enzima-sustrato durante la reacción, por lo que debe escribirse ésta en términos de cantidad total o inicial de enzima, que es una cantidad conocida.
- o es la velocidad de formación del producto.
- o es la velocidad máxima. k2 se denomina con frecuencia kcat.
Cabe observar que [S] es grande comparada con Km, [S]/(Km + [S]) tiende a 1. La velocidad de formación de producto es igual a k2[E0] en ese caso.
Cuando [S] es igual a Km, [S]/(Km + [S]) vale 0.5. En ese caso, la velocidad de formación de producto es la mitad de la máxima (1/2 Vmax). Representando gráficamente V0 frente a [S] se puede fácilmente determinar Vmax y Km. Esto requiere una serie de experimentos a E0 constante y diferentes concentraciones de sustrato [S].
La gráfica de Michaelis - Menten se construye a partir de las velocidades iniciales de reacción de distintas concentraciones de sustrato obtenidas en un ensayo enzimático. El procedimiento a seguir es el siguiente:[4]
- Obtener la velocidad inicial de reacción (V) para cada concentración de sustrato a partir de los datos de un ensayo enzimático.
- Tabular los valores de V para cada concentración de sustrato [S].
- Elaborar una gráfica de dispersión de V vs. [S].
- Trazar una curva hiperbólica desde el origen y extender la curva hacia valores mayores de [S].
- Analizar por inspección la tendencia de la curva. La curva debe mostrar un comportamiento asintótico hacia un límite superior de la velocidad. Este valor límite es Vmax. Teóricamente Vmax es la velocidad inicial de reacción cuando [S] tiende a infinito.
- Sobre el eje de las abscisas, encontrar Vmax y dividir este valor entre 2.
- Encontrar por interpolación el valor de [S] que corresponde a 1/2 de Vmax. Este valor de concentración es Km.
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.


![{\displaystyle {\frac {d[ES]}{dt}}=k_{1}[E][S]-k_{-1}[ES]-k_{2}[ES]=0}](http://wikimedia.org/api/rest_v1/media/math/render/svg/2bb19158ff794158ceac860552fbfa1eacdf3558)
![{\displaystyle [ES]={\frac {k_{1}[E][S]}{k_{-1}+k_{2}}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/041c97c8ca3aa792f4fe79f75ec6b88ba19098aa)

![{\displaystyle [ES]={\frac {[E][S]}{K_{m}}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/6ae6e75fd92aa67bd80cf22f780cdb231efacee1)
![{\displaystyle {\frac {d[P]}{dt}}=k_{2}[ES]}](http://wikimedia.org/api/rest_v1/media/math/render/svg/0fc45725f2f145f603fcf61641d533d1bbcdb70d)
![{\displaystyle [E_{0}]=[E]+[ES]}](http://wikimedia.org/api/rest_v1/media/math/render/svg/98b6b65c6ec79a6eb4bdb476e877e3acfb8c6503)
![{\displaystyle [E]=[E_{0}]-[ES]}](http://wikimedia.org/api/rest_v1/media/math/render/svg/ba5fa93cfdb8b7ffec08ac9d5892a6df7b7c1694)
![{\displaystyle [ES]={\frac {([E_{0}]-[ES])[S]}{K_{m}}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/af25e5b446ab5bb7cf963aa5c695540414dd272a)
![{\displaystyle K_{m}[ES]+[S][ES]=[E_{0}][S]}](http://wikimedia.org/api/rest_v1/media/math/render/svg/823baafd833a562d3cf260b519b7c8b3f01afef4)
![{\displaystyle [ES]={\frac {[E_{0}][S]}{K_{m}+[S]}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/b3ab5a4bda584bb8c9de0f0eaf00e89e8295f81d)
![{\displaystyle {\frac {d[P]}{dt}}=k_{2}[E_{0}]{\frac {[S]}{K_{m}+[S]}}=V_{max}{\frac {[S]}{K_{m}+[S]}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/230401cdb47fc5cdca32646aacbc167e546a7d79)

![{\displaystyle d[P]/dt}](http://wikimedia.org/api/rest_v1/media/math/render/svg/8f415e22bec74938e981805ec4c3b6f30f654d49)

![{\displaystyle k_{2}[E_{0}]}](http://wikimedia.org/api/rest_v1/media/math/render/svg/330e872875cdd39e302bb163c79dd80d34a13ef4)
