Η καρκινογένεση, που ονομάζεται επίσης ογκογένεση (Carcinogenesis, ή oncogenesis, ή tumorigenesis), είναι ο σχηματισμός ενός καρκίνου, όπου τα φυσιολογικά κύτταρα μεταμορφώθηκαν σε καρκινικά κύτταρα. Η διαδικασία χαρακτηρίζεται από αλλαγές στα κυτταρικά, γενετικά και επιγενετικά επίπεδα και μη φυσιολογική κυτταρική διαίρεση. Η κυτταρική διαίρεση είναι μια φυσιολογική διαδικασία που συμβαίνει σχεδόν σε όλους τους ιστούς και υπό ποικίλες συνθήκες. Κανονικά, η ισορροπία μεταξύ του πολλαπλασιασμού και του προγραμματισμένου κυτταρικού θανάτου, με τη μορφή απόπτωσης, διατηρείται για να διασφαλιστεί η ακεραιότητα των ιστών και των οργάνων. Σύμφωνα με την επικρατούσα αποδεκτή θεωρία της καρκινογένεσης, η θεωρία της σωματικής μετάλλαξης, μεταλλάξεις στο DNA και επιμεταλλάξεις που οδηγούν σε καρκίνο διαταράσσουν αυτές τις κανονικές διαδικασίες παρεμβαίνοντας στον προγραμματισμό που ρυθμίζει τις διαδικασίες , ανατρέποντας τη φυσιολογική ισορροπία μεταξύ πολλαπλασιασμού και κυτταρικού θανάτου.[1][2][3][4][5] Αυτό έχει ως αποτέλεσμα την ανεξέλεγκτη κυτταρική διαίρεση και εξέλιξη αυτών των κυττάρων από φυσική επιλογή στο σώμα. Μόνο ορισμένες μεταλλάξεις οδηγούν σε καρκίνο, ενώ η πλειονότητα των μεταλλάξεων όχι. Παραλλαγές κληρονομικών γονιδίων μπορεί να προδιαθέτουν τα άτομα σε καρκίνο. Επιπλέον, περιβαλλοντικοί παράγοντες όπως καρκινογόνα και η ακτινοβολία προκαλούν μεταλλάξεις που μπορεί να συμβάλλουν στην ανάπτυξη καρκίνου. Τέλος, τυχαία λάθη στην κανονική αντιγραφή του DNA μπορεί να οδηγήσουν σε μεταλλάξεις που προκαλούν καρκίνο.[6] Συνήθως απαιτείται μια σειρά από πολλές μεταλλάξεις σε ορισμένες κατηγορίες γονιδίων πριν ένα φυσιολογικό κύτταρο μεταμορφωθεί σε καρκινικό κύτταρο.[7][8][9][10][11] Πρόσφατη ολοκληρωμένη ταξινόμηση σε επίπεδο ασθενή και η ποσοτικοποίηση των συμβάντων οδηγού σε ομάδες TCGA (The Cancer Genome Atlas) αποκάλυψε ότι υπάρχουν κατά μέσο όρο 12 συμβάντα οδηγού ανά όγκο, εκ των οποίων 0,6 είναι σημειακές μεταλλάξεις (point mutations) στα ογκογονίδια] ], 1,5 είναι ενισχύσεις ογκογονιδίων, 1,2 είναι σημειακές μεταλλάξεις σε ογκοκαταστολείς, 2,1 είναι διαγραφές ογκοκαταστολέων, 1,5 είναι οδηγοί απωλειών χρωμοσωμάτων, 1 είναι οδηγός κέρδος χρωμοσώματος, 2 είναι οδηγός απώλειες βραχίονα χρωμοσώματος και το 1,5 είναι οδηγός κέρδη χρωμοσωμικού βραχίονα .[12] Μεταλλάξεις σε γονίδια που ρυθμίζουν την κυτταρική διαίρεση, απόπτωση (κυτταρικός θάνατος) και επιδιόρθωση του DNA μπορεί να οδηγήσουν σε ανεξέλεγκτο κυτταρικό πολλαπλασιασμό και καρκίνο. Ο καρκίνος είναι βασικά μια ασθένεια ρύθμισης της ανάπτυξης των ιστών. Προκειμένου ένα φυσιολογικό κύτταρο να μετασχηματιστεί σε καρκινικό κύτταρο, τα γονίδια που ρυθμίζουν την κυτταρική ανάπτυξη και διαφοροποίηση πρέπει να τροποποιηθούν.[13] Γενετικές και επιγενετικές αλλαγές μπορούν να συμβούν σε πολλά επίπεδα, από κέρδος ή απώλεια ολόκληρων χρωμοσωμάτων, έως μετάλλαξη που επηρεάζει ένα μοναδικό νουκλεοτίδιο DNA, ή στη αποσιώπηση ή ενεργοποίηση ενός microRNA που ελέγχει την έκφραση 100 έως 500 γονιδίων.[14][15] Υπάρχουν δύο μεγάλες κατηγορίες γονιδίων που επηρεάζονται από αυτές τις αλλαγές. Τα ογκογονίδια μπορεί να είναι φυσιολογικά γονίδια που εκφράζονται σε ακατάλληλα υψηλά επίπεδα, ή τροποποιημένα γονίδια που έχουν νέες ιδιότητες. Και στις δύο περιπτώσεις, η έκφραση αυτών των γονιδίων προάγει τον κακοήθη φαινότυπο των καρκινικών κυττάρων. Τα ογκοκατασταλτικά γονίδια είναι γονίδια που αναστέλλουν την κυτταρική διαίρεση, την επιβίωση ή άλλες ιδιότητες των καρκινικών κυττάρων. Τα ογκοκατασταλτικά γονίδια συχνά απενεργοποιούνται από γενετικές αλλαγές που προάγουν τον καρκίνο. Τέλος, ογκοϊοί, ιοί που περιέχουν ένα ογκογονίδιο, κατηγοριοποιούνται ως ογκογονικοί επειδή πυροδοτούν την ανάπτυξη όγκου ιστών στον ξενιστή. Αυτή η διαδικασία αναφέρεται επίσης ως ιικός μετασχηματισμός.

Γενετικές και επιγενετικές
Υπάρχει ένα διαφορετικό σχήμα ταξινόμησης για τις διάφορες γονιδιωματικές αλλαγές που μπορεί να συμβάλλουν στη δημιουργία καρκινικών κυττάρων. Πολλές από αυτές τις αλλαγές είναι μεταλλάξεις ή αλλαγές στην νουκλεοτιδική αλληλουχία του γονιδιωματικού DNA. Υπάρχουν επίσης πολλές επιγενετικές αλλαγές που αλλάζουν εάν τα γονίδια εκφράζονται ή όχι. Ανευπλοειδία, η παρουσία ενός μη φυσιολογικού αριθμού χρωμοσωμάτων, είναι μια γονιδιωματική αλλαγή που δεν είναι μετάλλαξη και μπορεί να περιλαμβάνει είτε κέρδος είτε απώλεια ενός ή περισσότερων χρωμοσωμάτων μέσω σφαλμάτων στη μίτωση. Οι μεταλλάξεις μεγάλης κλίμακας περιλαμβάνουν είτε την διαγραφή, είτε το διπλασιασμό ενός τμήματος ενός χρωμοσώματος. Η γονιδιακή ενίσχυση συμβαίνει όταν ένα κύτταρο αποκτά πολλά αντίγραφα (συχνά 20 ή περισσότερα) μιας μικρής χρωμοσωμικής περιοχής, που συνήθως περιέχει ένα ή περισσότερα ογκογονίδια και παρακείμενο γενετικό υλικό. Χρωμοσωμική μετατόπιση συμβαίνει όταν δύο ξεχωριστές χρωμοσωμικές περιοχές συγχωνεύονται ανώμαλα, συχνά σε μια χαρακτηριστική θέση. Ένα πολύ γνωστό παράδειγμα αυτού είναι το χρωμόσωμα της Φιλαδέλφειας, ή η μετατόπιση των χρωμοσωμάτων 9 και 22, που εμφανίζεται στη χρόνια μυελογενή λευχαιμία και έχει ως αποτέλεσμα την παραγωγή της πρωτεΐνης σύντηξης BCR-abl, μιας ογκογόνου κινάσης τυροσίνης. Οι μεταλλάξεις μικρής κλίμακας περιλαμβάνουν σημειακές μεταλλάξεις, διαγραφές και εισαγωγές, που μπορεί να συμβούν στον προαγωγέα ενός γονιδίου και να επηρεάσουν την έκφρασή του, ή μπορεί να εμφανιστεί στην κωδικοποιητική αλληλουχία του γονιδίου και να αλλάξει τη λειτουργία ή τη σταθερότητα του προϊόντος της πρωτεΐνης του. Η διαταραχή ενός μεμονωμένου γονιδίου μπορεί επίσης να προκύψει από ενσωμάτωση γονιδιωματικού υλικού από ιό DNA ή ρετροϊό, και ένα τέτοιο συμβάν μπορεί επίσης να έχει ως αποτέλεσμα την έκφραση ιικών ογκογονιδίων στο προσβεβλημένο κύτταρο και τους απογόνους του.
Βλάβη στο DNA

Η βλάβη του DNA θεωρείται η κύρια αιτία καρκίνου.[16] Περισσότερες από 60.000 νέες φυσικές περιπτώσεις βλάβης του DNA προκύπτουν, κατά μέσο όρο, ανά ανθρώπινο κύτταρο, ανά ημέρα, λόγω ενδογενών κυτταρικών διεργασιών. Επιπρόσθετη βλάβη στο DNA μπορεί να προκύψει από την έκθεση σε εξωγενείς παράγοντες. Παράδειγμα εξωγενούς καρκινογόνου παράγοντα, αποτελεί ο καπνός του τσιγάρου που προκαλεί αυξημένη βλάβη στο DNA και αυτή η βλάβη στο DNA πιθανότατα προκαλεί την αύξηση του καρκίνου του πνεύμονα λόγω του καπνίσματος.[17] Σε άλλα παραδείγματα, το υπεριώδες φως από την ηλιακή ακτινοβολία προκαλεί βλάβη στο DNA που είναι σημαντική στο μελάνωμα,[18]η λοίμωξη από το ελικοβακτήριο του πυλωρού παράγει υψηλά επίπεδα δραστικών μορφών οξυγόνου που βλάπτουν το DNA και συμβάλλουν στον γαστρικό καρκίνο,[19] και ο μεταβολίτης Aspergillus flavus thw αφλατοξίνης είναι ένας παράγοντας που καταστρέφει το DNA και προκαλεί τον καρκίνο του ήπατος.[20] Η βλάβη του DNA μπορεί επίσης να προκληθεί από ουσίες που παράγονται στο σώμα. Τα μακροφάγα και τα ουδετερόφιλα σε ένα φλεγμονώδες επιθήλιο του παχέος εντέρου είναι η πηγή δραστικών ειδών οξυγόνου που προκαλούν τη βλάβη του DNA που ξεκινά ογκογένεση,[21] και τα χολικά οξέα, σε υψηλά επίπεδα στο κόλον των ανθρώπων που ακολουθούν δίαιτα πλούσια σε λιπαρά, προκαλούν επίσης βλάβη στο DNA και συμβάλλουν στον καρκίνο του παχέος εντέρου.[22] Τέτοιες εξωγενείς και ενδογενείς πηγές βλάβης του DNA υποδεικνύονται στα πλαίσια στο επάνω μέρος του σχήματος αυτής της ενότητας. Ο κεντρικός ρόλος της βλάβης του DNA στην εξέλιξη του καρκίνου υποδεικνύεται στο δεύτερο επίπεδο του σχήματος. Τα κεντρικά στοιχεία της βλάβης του DNA, οι επιγενετικές αλλοιώσεις και η ανεπαρκής επιδιόρθωση του DNA στην εξέλιξη του καρκίνου φαίνονται με κόκκινο χρώμα. Ανεπάρκεια στην επιδιόρθωση του DNA θα προκαλούσε τη συσσώρευση μεγαλύτερης βλάβης στο DNA και αυξάνει τον κίνδυνο για καρκίνο. Για παράδειγμα, άτομα με κληρονομική βλάβη σε οποιοδήποτε από τα 34 γονίδια επιδιόρθωσης του DNA διατρέχουν αυξημένο κίνδυνο καρκίνου, με ορισμένα ελαττώματα να προκαλούν έως και 100% πιθανότητα του καρκίνου (π.χ. μεταλλάξεις p53).[23] Τέτοιες μετάλλαξεις βλαστικής γραμμής εμφανίζονται σε ένα πλαίσιο στα αριστερά του σχήματος, με ένδειξη της συμβολής τους στην ανεπάρκεια επιδιόρθωσης του DNA. Ωστόσο, τέτοιες μεταλλάξεις βλαστικής σειράς (οι οποίες προκαλούν υψηλά διεισδυτικά καρκινικά σύνδρομα) είναι η αιτία μόνο για το ένα τοις εκατό των καρκίνων.[24] Η πλειοψηφία των καρκίνων ονομάζονται μη κληρονομικοί ή "σποραδικοί καρκίνοι". Περίπου το 30% των σποραδικών καρκίνων έχουν κάποια κληρονομική συνιστώσα που δεν έχει καθοριστεί επί του παρόντος, ενώ η πλειοψηφία, ή το 70% των σποραδικών καρκίνων, δεν έχουν κληρονομικό συστατικό.[25] Σε σποραδικούς καρκίνους, μια ανεπάρκεια στην επιδιόρθωση του DNA οφείλεται περιστασιακά σε μια μετάλλαξη σε ένα γονίδιο επιδιόρθωσης του DNA. Πολύ πιο συχνά, η μειωμένη ή απουσία έκφρασης των γονιδίων επιδιόρθωσης του DNA οφείλεται σε επιγενετικές αλλοιώσεις που μειώνουν ή αποσιωπούν την έκφραση του γονιδίου. Αυτό υποδεικνύεται στο σχήμα στο 3ο επίπεδο από την κορυφή. Για παράδειγμα, για 113 καρκίνους του παχέος εντέρου που εξετάστηκαν διαδοχικά, μόνο τέσσερις είχαν παρανοηματική μετάλλαξη στο γονίδιο επιδιόρθωσης του DNA MGMT, ενώ η πλειονότητα είχε μειωμένη έκφραση MGMT λόγω μεθυλίωσης της περιοχής προαγωγέα του MGMT (επιγενετική αλλαγή).[26] Όταν η έκφραση των γονιδίων επιδιόρθωσης του DNA μειώνεται, αυτό προκαλεί ανεπάρκεια επιδιόρθωσης DNA. Αυτό φαίνεται στο σχήμα στο 4ο επίπεδο από την κορυφή. Με ανεπάρκεια επιδιόρθωσης του DNA, η βλάβη του DNA επιμένει στα κύτταρα σε υψηλότερο από το τυπικό επίπεδο (5ο επίπεδο από την κορυφή στο σχήμα). Αυτή η υπερβολική ζημιά προκαλεί αυξημένη συχνότητα μετάλλαξης και/ή επιμετάλλαξης (6ο επίπεδο από την κορυφή του σχήματος). Πειραματικά, τα ποσοστά μετάλλαξης αυξάνονται σημαντικά σε κύτταρα ελαττωματικά σε επιδιόρθωση ασυμφωνίας DNA,[27][28] ή σε επισκευή ομόλογου ανασυνδυασμού (HRR).[29] οι χρωματοσωμικές αναδιατάξεις και η ανευπλοειδία αυξάνουν επίσης σε ελαττωματικά κύτταρα HRR. [30] Κατά τη διάρκεια της επιδιόρθωσης θραύσεων διπλού κλώνου DNA, ή επιδιόρθωσης άλλων βλαβών στο DNA, οι ελλιπώς καθαρισμένες θέσεις επισκευής μπορεί να προκαλέσουν επιγενετική σίγαση γονιδίου.[31][32] Οι σωματικές μεταλλάξεις και οι επιγενετικές αλλοιώσεις που προκαλούνται από βλάβη του DNA και οι ελλείψεις στην επιδιόρθωση του DNA συσσωρεύονται σε ελαττώματα πεδίου. Τα ελαττώματα πεδίου είναι ιστοί που εμφανίζονται φυσιολογικά με πολλαπλές αλλοιώσεις (που συζητούνται στην ενότητα παρακάτω) και είναι συνήθεις πρόδρομοι για την ανάπτυξη του διαταραγμένου και υπερπολλαπλασιαζόμενου κλώνου του ιστού σε έναν καρκίνο. Τέτοια ελαττώματα πεδίου (δεύτερο επίπεδο από το κάτω μέρος του σχήματος) μπορεί να έχουν πολυάριθμες μεταλλάξεις και επιγενετικές αλλοιώσεις. Είναι αδύνατο να προσδιοριστεί η αρχική αιτία για τους περισσότερους ειδικούς καρκίνους. Σε λίγες περιπτώσεις, υπάρχει μόνο μία αιτία: για παράδειγμα, ο ιός HHV-8 προκαλεί όλα τα σαρκώματα Καπόσι. Ωστόσο, με τη βοήθεια τεχνικών και πληροφοριών επιδημιολογίας του καρκίνου, είναι δυνατό να παραχθεί μια εκτίμηση μιας πιθανής αιτίας σε πολλές περισσότερες περιπτώσεις. Για παράδειγμα, ο καρκίνος του πνεύμονα έχει διάφορες αιτίες, συμπεριλαμβανομένης της χρήσης καπνού και του αερίου ραδονίου. Οι άνδρες που καπνίζουν σήμερα αναπτύσσουν καρκίνο του πνεύμονα σε ποσοστό 14 φορές μεγαλύτερο από εκείνο των ανδρών που δεν έχουν καπνίσει ποτέ καπνό: η πιθανότητα καρκίνου του πνεύμονα σε έναν σημερινό καπνιστή να προκαλείται από το κάπνισμα είναι περίπου 93%. Υπάρχει 7% πιθανότητα ο καρκίνος του πνεύμονα του καπνιστή να προκλήθηκε από αέριο ραδόνιο ή κάποια άλλη αιτία που δεν είναι καπνός.[33] Αυτές οι στατιστικές συσχετίσεις έδωσαν τη δυνατότητα στους ερευνητές να συμπεράνουν ότι ορισμένες ουσίες ή συμπεριφορές είναι καρκινογόνες. Ο καπνός του τσιγάρου προκαλεί αυξημένη εξωγενή βλάβη στο DNA και αυτή η βλάβη στο DNA είναι η πιθανή αιτία καρκίνου του πνεύμονα λόγω του καπνίσματος. Μεταξύ των περισσότερων από τις 5.000 ενώσεις στον καπνό του τσιγάρου, οι γονιδιοτοξικοί παράγοντες που βλάπτουν το DNA που εμφανίζονται και στις υψηλότερες συγκεντρώσεις και έχουν τις ισχυρότερες μεταλλαξιογόνες επιδράσεις είναι οι ακρολεΐνη, φορμαλδεΰδη, ακρυλονιτρίλιο, 1,3-βουταδιένιο, ακεταλδεΰδη, αιθυλενοξείδιο και ισοπρένιο.[17] Χρησιμοποιώντας τις τεχνικές της μοριακής βιολογίας, είναι δυνατός ο χαρακτηρισμός των μεταλλάξεων, των επιμεταλλάξεων ή των χρωμοσωμικών ανωμαλιών εντός ενός όγκου και σημειώνεται ταχεία πρόοδος στον τομέα της πρόγνωσης ορισμένων ασθενών με καρκίνο με βάση το φάσμα των μεταλλάξεων. Για παράδειγμα, έως και οι μισοί όγκοι έχουν ελαττωματικό γονίδιο p53. Αυτή η μετάλλαξη σχετίζεται με κακή πρόγνωση, καθώς αυτά τα καρκινικά κύτταρα είναι λιγότερο πιθανό να περάσουν σε απόπτωση, ή σε προγραμματισμένο κυτταρικό θάνατο όταν υποστούν βλάβη από τη θεραπεία. Οι μεταλλάξεις της τελομεράσης αφαιρούν πρόσθετους φραγμούς, επεκτείνοντας τον αριθμό των φορών που μπορεί να διαιρεθεί ένα κύτταρο. Άλλες μεταλλάξεις επιτρέπουν στον όγκο να αναπτύξει νέα αιμοφόρα αγγεία για να παρέχει περισσότερα θρεπτικά συστατικά, ή να μετασταθεί, εξαπλούμενος σε άλλα μέρη του σώματος. Ωστόσο, μόλις σχηματιστεί ένας καρκίνος, συνεχίζει να εξελίσσεται και να παράγει υποκλώνους. Αναφέρθηκε το 2012 ότι ένα μεμονωμένο δείγμα καρκίνου του νεφρού, που λήφθηκε από εννέα διαφορετικές περιοχές, είχε 40 "πανταχού παρούσες" μεταλλάξεις, που βρέθηκαν και στις εννέα περιοχές, 59 μεταλλάξεις κοινές σε ορισμένες, αλλά όχι και στις εννέα περιοχές, και 29 "ιδιωτικές" μεταλλάξεις που υπήρχαν μόνο σε μια περιοχή.[34] Οι γενεές των κυττάρων στις οποίες συσσωρεύονται όλες αυτές οι αλλοιώσεις του DNA είναι δύσκολο να εντοπιστούν, αλλά δύο πρόσφατες σειρές στοιχείων υποδηλώνουν ότι τα φυσιολογικά βλαστοκύτταρα μπορεί να είναι τα κύτταρα προέλευσης των καρκίνων.[35][36] Πρώτον, υπάρχει μια εξαιρετικά θετική συσχέτιση (Spearman's rho = 0,81, P < 3,5 × 10−8) μεταξύ του κινδύνου ανάπτυξης καρκίνου σε έναν ιστό και του αριθμού των φυσιολογικών διαιρέσεων βλαστοκυττάρων που λαμβάνουν χώρα στον ίδιο ιστό. Ο συσχετισμός εφαρμόστηκε σε 31 τύπους καρκίνου και επεκτάθηκε σε πέντε τάξεις μεγέθους.[37] Αυτή η συσχέτιση σημαίνει ότι εάν τα φυσιολογικά βλαστοκύτταρα από έναν ιστό διαιρεθούν μία φορά, ο κίνδυνος καρκίνου σε αυτόν τον ιστό είναι περίπου 1Χ. Αν διαιρεθούν 1.000 φορές, ο κίνδυνος καρκίνου είναι 1.000Χ. Και αν τα φυσιολογικά βλαστοκύτταρα από έναν ιστό διαιρούνται 100.000 φορές, ο κίνδυνος καρκίνου σε αυτόν τον ιστό είναι περίπου 100.000 φορές. Αυτό υποδηλώνει έντονα ότι ο κύριος παράγοντας στην έναρξη του καρκίνου είναι το γεγονός ότι τα "φυσιολογικά" βλαστοκύτταρα διαιρούνται, πράγμα που σημαίνει ότι ο καρκίνος προέρχεται από φυσιολογικά, υγιή βλαστοκύτταρα.[36] Δεύτερον, οι στατιστικές δείχνουν ότι οι περισσότεροι ανθρώπινοι καρκίνοι διαγιγνώσκονται σε άτομα μεγαλύτερης ηλικίας. Μια πιθανή εξήγηση είναι ότι οι καρκίνοι εμφανίζονται επειδή τα κύτταρα συσσωρεύουν βλάβες με την πάροδο του χρόνου. Το DNA είναι το μόνο κυτταρικό συστατικό που μπορεί να συσσωρεύσει βλάβη σε όλη τη διάρκεια της ζωής και τα βλαστοκύτταρα είναι τα μόνα κύτταρα που μπορούν να μεταδώσουν το DNA από το ζυγώτη στα κύτταρα αργά στη ζωή. Άλλα κύτταρα, που προέρχονται από βλαστοκύτταρα, δεν διατηρούν το DNA από την αρχή της ζωής τους μέχρι να εμφανιστεί ένας πιθανός καρκίνος. Αυτό σημαίνει ότι οι περισσότεροι καρκίνοι προέρχονται από φυσιολογικά βλαστοκύτταρα.[35][36]
Συμβολή ελαττωμάτων πεδίου

Ο όρος "καρκινοποίηση πεδίου" χρησιμοποιήθηκε για πρώτη φορά το 1953 για να περιγράψει μια περιοχή ή "πεδίο" του επιθηλίου που είχε προκαθοριστεί από (εκείνη την εποχή) με άγνωστες διεργασίες σε μεγάλο βαθμό ώστε να το προδιαθέσει προς την ανάπτυξη καρκίνου.[38] Έκτοτε, οι όροι "καρκινοποίηση πεδίου (field cancerization)" και "ελάττωμα πεδίου (field defect)" χρησιμοποιούνται για να περιγράψουν τον προκακοήθη ιστό στον οποίο είναι πιθανό να εμφανιστούν νέοι καρκίνοι. Τα ελαττώματα πεδίου έχουν εντοπιστεί σε σχέση με καρκίνους και είναι σημαντικά για την εξέλιξη σε καρκίνο.[39][40] Ωστόσο, όπως επισήμανε ο Ρούμπιν [41] η συντριπτική πλειονότητα των μελετών στην έρευνα του καρκίνου έχει γίνει σε καλά καθορισμένους όγκους in vivo, ή σε διακριτές νεοπλασματικές εστίες in vitro. Ωστόσο, υπάρχουν ενδείξεις ότι περισσότερο από το 80% των σωματικών μεταλλάξεων που βρέθηκαν σε μεταλλακτικούς φαινοτύπους οι ανθρώπινοι ορθοκολικοί όγκοι εμφανίζονται πριν από την έναρξη της τελικής κλωνικής επέκτασης…"[42] Περισσότερες από τις μισές σωματικές μεταλλάξεις που εντοπίστηκαν σε όγκους εμφανίστηκαν σε μια προνεοπλασματική φάση (σε ελάττωμα πεδίου), κατά την ανάπτυξη φαινομενικά φυσιολογικών κυττάρων. Θα ήταν επίσης αναμενόμενο ότι πολλές από τις επιγενετικές αλλοιώσεις που υπάρχουν σε όγκους μπορεί να έχουν συμβεί σε προνεοπλασματικά ελαττώματα του πεδίου.[43] Στο παχύ έντερο, ένα ελάττωμα πεδίου πιθανώς προκύπτει από τη φυσική επιλογή ενός μεταλλαγμένου ή επιγενετικά τροποποιημένου κυττάρου μεταξύ των βλαστοκυττάρων στη βάση μιας από τις εντερικές κρύπτες στην εσωτερική επιφάνεια του παχέος εντέρου. Ένα μεταλλαγμένο ή επιγενετικά τροποποιημένο βλαστοκύτταρο μπορεί να αντικαταστήσει τα άλλα κοντινά βλαστοκύτταρα με φυσική επιλογή. Αυτό μπορεί να προκαλέσει την εμφάνιση ενός επιθέματος μη φυσιολογικού ιστού. Το σχήμα σε αυτήν την ενότητα περιλαμβάνει μια φωτογραφία μιας πρόσφατης εκτομής και κατά μήκος ανοιγμένου τμήματος του παχέος εντέρου που δείχνει έναν καρκίνο του παχέος εντέρου και τέσσερις πολύποδες. Κάτω από τη φωτογραφία υπάρχει ένα σχηματικό διάγραμμα για το πώς μπορεί να έχει σχηματιστεί ένα μεγάλο επίθεμα μεταλλαγμένων ή επιγενετικά τροποποιημένων κυττάρων, που φαίνεται από τη μεγάλη περιοχή με κίτρινο χρώμα στο διάγραμμα. Μέσα σε αυτό το πρώτο μεγάλο επίθεμα στο διάγραμμα (ένας μεγάλος κλώνος κυττάρων), μπορεί να συμβεί μια δεύτερη τέτοια μετάλλαξη ή επιγενετική αλλοίωση, έτσι ώστε ένα δεδομένο βλαστοκύτταρο να αποκτά πλεονέκτημα σε σύγκριση με τα γειτονικά του και αυτό το αλλοιωμένο βλαστοκύτταρο μπορεί να επεκταθεί κλωνικά, σχηματίζοντας ένα δευτερεύον επίθεμα, ή υποκλώνο, μέσα στο αρχικό επίθεμα. Αυτό υποδεικνύεται στο διάγραμμα με τέσσερα μικρότερα μπαλώματα διαφορετικών χρωμάτων εντός της μεγάλης κίτρινης αρχικής περιοχής. Μέσα σε αυτά τα νέα επιθέματα (υποκλώνους), η διαδικασία μπορεί να επαναληφθεί πολλές φορές, υποδεικνύεται από τα ακόμη μικρότερα επιθέματα εντός των τεσσάρων δευτερευόντων επιθεμάτων (με ακόμη διαφορετικά χρώματα στο διάγραμμα) τα οποία διαστέλλονται κλωνικά, έως ότου προκύψουν βλαστοκύτταρα που δημιουργούν είτε μικρούς πολύποδες, ή αλλιώς κακοήθη νεοπλάσματα (καρκίνος). Στη φωτογραφία, ένα φαινομενικό ελάττωμα πεδίου σε αυτό το τμήμα ενός παχέος εντέρου έχει δημιουργήσει τέσσερις πολύποδες (με την ετικέτα το μέγεθος των πολύποδων, 6 mm, 5 mm και δύο των 3 mm, και έναν καρκίνο πλάτους περίπου 3 cm στη μεγαλύτερη διάστασή του). Αυτά τα νεοπλάσματα υποδεικνύονται επίσης (στο διάγραμμα κάτω από τη φωτογραφία) από 4 μικρούς μαύρους κύκλους (πολύποδες) και μια μεγαλύτερη κόκκινη περιοχή (καρκίνος). Ο καρκίνος στη φωτογραφία εμφανίστηκε στην περιοχή του τυφλού του παχέος εντέρου, όπου το παχύ έντερο ενώνεται με το λεπτό έντερο (με ετικέτα) και όπου εμφανίζεται η σκωληκοειδής απόφυση (με ετικέτα). Το λίπος στη φωτογραφία είναι εξωτερικά στο εξωτερικό τοίχωμα του παχέος εντέρου. Στο τμήμα του παχέος εντέρου που φαίνεται εδώ, το παχύ έντερο κόπηκε κατά μήκος για να εκτεθεί η εσωτερική του επιφάνεια και να εμφανιστεί ο καρκίνος και οι πολύποδες που εμφανίζονται μέσα στην εσωτερική επιθηλιακή επένδυση του παχέος εντέρου. Εάν η γενική διαδικασία με την οποία προκύπτουν σποραδικοί καρκίνοι του παχέος εντέρου είναι ο σχηματισμός ενός προνεοπλασματικού κλώνου που εξαπλώνεται με φυσική επιλογή, ακολουθούμενος από σχηματισμό εσωτερικών υποκλώνων εντός του αρχικού κλώνου και υποκλώνων μέσα σε αυτούς, τότε οι καρκίνοι του παχέος εντέρου γενικά θα πρέπει να συνδέονται με, και να προηγούνται από, τα πεδία αυξανόμενης ανωμαλίας, που αντικατοπτρίζουν τη διαδοχή των προκακοηθών συμβάντων. Η πιο εκτεταμένη περιοχή ανωμαλίας (η πιο εξωτερική κίτρινη ακανόνιστη περιοχή στο διάγραμμα) θα αντικατοπτρίζει το πιο πρώιμο συμβάν στο σχηματισμό ενός κακοήθους νεοπλάσματος. Σε πειραματική αξιολόγηση συγκεκριμένων ελλείψεων επιδιόρθωσης DNA σε καρκίνους, πολλές ειδικές ελλείψεις επιδιόρθωσης DNA αποδείχθηκαν επίσης ότι εμφανίζονται στα ελαττώματα πεδίου που περιβάλλουν αυτούς τους καρκίνους. Ο παρακάτω πίνακας δίνει παραδείγματα για τα οποία η ανεπάρκεια επιδιόρθωσης DNA σε έναν καρκίνο αποδείχθηκε ότι προκαλείται από επιγενετική αλλαγή και οι κάπως χαμηλότερες συχνότητες με τις οποίες βρέθηκε η ίδια επιγενετικά προκαλούμενη ανεπάρκεια επιδιόρθωσης του DNA στο ελάττωμα του περιβάλλοντος πεδίου.
| + Συχνότητα επιγενετικών αλλαγών στα γονίδια επιδιόρθωσης του DNA σε σποραδικούς καρκίνους και σε ελαττώματα παρακείμενου πεδίου | Καρκίνος | Γονίδιο | Συχνότητα σε καρκίνο | Συχνότητα σε ελάττωμα | Παραπομπή |
|---|---|---|---|---|---|
| Ορθοκολικός | MGMT | 46% | 34% | [44] | |
| Ορθοκολικός | MGMT | 47% | 11% | [45] | |
| Ορθοκολικός | MGMT | 70% | 60% | [46] | |
| Ορθοκολικός | MSH2 | 13% | 5% | [45] | |
| Ορθοκολικός | ERCC1 | 100% | 40% | [47] | |
| Ορθοκολικός | PMS2 | 88% | 50% | [47] | |
| Ορθοκολικός | XPF | 55% | 40% | [47] | |
| Κεφάλι και Λαιμός | MGMT | 54% | 38% | [48] | |
| Κεφάλι και Λαιμός | MLH1 | 33% | 25% | [49] | |
| Κεφάλι και Λαιμός | MLH1 | 31% | 20% | [50] | |
| Στομάχι | MGMT | 88% | 78% | [51] | |
| Στομάχι | MLH1 | 73% | 20% | [52] | |
| Οισοφάγος | MLH1 | 77%–100% | 23%–79% | [53] |
Μερικοί από τους μικρούς πολύποδες στο ελάττωμα του πεδίου που φαίνεται στη φωτογραφία του ανοιγμένου τμήματος του παχέος εντέρου μπορεί να είναι σχετικά καλοήθη νεοπλάσματα. Σε μια μελέτη του 1996 για πολύποδες μεγέθους μικρότερου από 10 mm που βρέθηκαν κατά τη διάρκεια της κολονοσκόπησης και ακολουθήθηκαν με επαναλαμβανόμενες κολονοσκοπήσεις για 3 χρόνια, το 25% παρέμεινε αμετάβλητο σε μέγεθος, το 35% υποχώρησε ή συρρικνώθηκε σε μέγεθος και το 40% μεγάλωσε σε μέγεθος.[54]
Αστάθεια του γονιδιώματος
Οι καρκίνοι είναι γνωστό ότι εμφανίζουν αστάθεια γονιδιώματος, ή "φαινότυπο μεταλλάκτη".[55] Το DNA που κωδικοποιεί την πρωτεΐνη εντός του πυρήνα είναι περίπου το 1,5% του συνολικού γονιδιωματικού DNA.[56] Μέσα σε αυτό το DNA που κωδικοποιεί την πρωτεΐνη (που ονομάζεται εξονίωμα (exome)), ένας μέσος καρκίνος του μαστού ή του παχέος εντέρου μπορεί να έχει περίπου 60 έως 70 μεταλλάξεις που αλλάζουν πρωτεΐνη, από τις οποίες περίπου 3 ή 4 μπορεί να είναι μεταλλάξεις "οδηγοί" και οι υπόλοιπες μπορεί να είναι μεταλλάξεις "επιβάτες (passenger) ".[43] Ωστόσο, ο μέσος αριθμός μεταλλάξεων αλληλουχίας DNA σε ολόκληρο το γονιδίωμα (συμπεριλαμβανομένου των μη κωδικοποιητικών περιοχών πρωτεΐνης) σε ένα δείγμα ιστού καρκίνου του μαστού είναι περίπου 20.000.[57] Σε ένα μέσο δείγμα ιστού μελανώματος (τα μελανώματα έχουν υψηλότερη συχνότητα μετάλλαξης εξονιώματος),[43]) ο συνολικός αριθμός μεταλλάξεων της αλληλουχίας DNA είναι περίπου 80.000.[58] Αυτές οι υψηλές συχνότητες μεταλλάξεων στις συνολικές αλληλουχίες νουκλεοτιδίων εντός των καρκίνων υποδηλώνουν ότι συχνά μια πρώιμη αλλαγή στο ελάττωμα του πεδίου οδηγεί σε καρκίνο (π.χ. η κίτρινη περιοχή στο διάγραμμα στην προηγούμενη ενότητα) είναι ανεπάρκεια στην επιδιόρθωση του DNA. Βρέθηκαν μεγάλα ελαττώματα πεδίου γύρω από καρκίνους του παχέος εντέρου (που εκτείνονται σε περίπου 10 cm σε κάθε πλευρά του καρκίνου)[47] να έχουν συχνά επιγενετικά ελαττώματα σε δύο ή τρεις πρωτεΐνες επιδιόρθωσης DNA (ERCC1, ERCC4 (XPF) και/ή PMS2) σε ολόκληρη την περιοχή του ελαττώματος πεδίου. Όταν η έκφραση των γονιδίων επιδιόρθωσης του DNA μειώνεται, η βλάβη του DNA συσσωρεύεται στα κύτταρα με ρυθμό υψηλότερο από το κανονικό, και αυτή η υπερβολική βλάβη προκαλεί αυξημένη συχνότητα μετάλλαξης ή/και επιμετάλλαξης. Τα ποσοστά μετάλλαξης αυξάνονται έντονα σε κύτταρα ελαττωματικά σε επιδιόρθωση ασυμφωνίας του DNA, [27][28] ή σε επιδιόρθωση με ομόλογο ανασυνδυασμό (homologous recombinational repair, HRR).[29] Μια ανεπάρκεια στην επιδιόρθωση του DNA, από μόνη της, μπορεί να επιτρέψει τη συσσώρευση βλάβης στο DNA και η επιρρεπής σε σφάλματα διαβλαβική σύνθεση (translesion synthesis) ορισμένων από τις κατεστραμμένες περιοχές μπορεί να προκαλέσει μεταλλάξεις. Επιπλέον, η ελαττωματική επιδιόρθωση αυτής της συσσωρευμένης βλάβης του DNA μπορεί να προκαλέσει επιμεταλλάξεις. Αυτές οι νέες μεταλλάξεις ή/και επιμεταλλάξεις μπορεί να παρέχουν πολλαπλασιαστικό πλεονέκτημα, δημιουργώντας ένα ελάττωμα πεδίου. Παρόλο που οι μεταλλάξεις/επιμεταλλάξεις στα γονίδια επιδιόρθωσης του DNA δεν παρέχουν, από μόνες τους, ένα επιλεκτικό πλεονέκτημα, μπορούν να μεταφερθούν ως επιβάτες στα κύτταρα, όταν το κύτταρο αποκτήσει μια πρόσθετη μετάλλαξη/επιμετάλλαξη που παρέχει ένα πολλαπλασιαστικό πλεονέκτημα.
Μη κυρίαρχες θεωρίες
Υπάρχει μια σειρά από θεωρίες καρκινογένεσης και θεραπείας του καρκίνου που δεν εμπίπτουν στην επικρατούσα τάση της επιστημονικής γνώμης, λόγω έλλειψης επιστημονικής λογικής, λογικής ή βάσης στοιχείων. Αυτές οι θεωρίες μπορούν να χρησιμοποιηθούν για να δικαιολογήσουν διάφορες εναλλακτικές θεραπείες για τον καρκίνο. Θα πρέπει να διακρίνονται από εκείνες τις θεωρίες καρκινογένεσης που έχουν λογική βάση στην κύρια βιολογία του καρκίνου και από τις οποίες μπορούν να γίνουν συμβατικά ελεγχόμενες υποθέσεις. Ωστόσο, αρκετές εναλλακτικές θεωρίες καρκινογένεσης βασίζονται σε επιστημονικά στοιχεία και αναγνωρίζονται όλο και περισσότερο. Ορισμένοι ερευνητές πιστεύουν ότι ο καρκίνος μπορεί να προκαλείται από ανευπλοειδία (αριθμητικές και δομικές ανωμαλίες στα χρωμοσώματα), [59] παρά με μεταλλάξεις ή επιμεταλλάξεις. Ο καρκίνος έχει επίσης θεωρηθεί ως μια μεταβολική ασθένεια, στην οποία ο κυτταρικός μεταβολισμός του οξυγόνου εκτρέπεται από το μονοπάτι που παράγει ενέργεια (οξειδωτική φωσφορυλίωση) στο μονοπάτι που δημιουργεί δραστικές μορφές οξυγόνου.[60] Αυτό προκαλεί μια ενεργειακή αλλαγή από την οξειδωτική φωσφορυλίωση στην αερόβια γλυκόλυση (φαινόμενο Warburg) και τη συσσώρευση δραστικών μορφών οξυγόνου που οδηγεί σε οξειδωτική καταπόνηση ("θεωρία οξειδωτικής καταπόνησης του καρκίνου").[60] Μια άλλη ιδέα της ανάπτυξης καρκίνου βασίζεται στην έκθεση σε ασθενή μαγνητικά και ηλεκτρομαγνητικά πεδία και τις επιπτώσεις τους στην οξειδωτική καταπόνηση, γνωστή ως μαγνητοκαρκινογένεση.[61] Ορισμένοι συγγραφείς αμφισβήτησαν την υπόθεση ότι οι καρκίνοι προκύπτουν από διαδοχικές τυχαίες μεταλλάξεις ως υπεραπλουστευτική, υποδηλώνοντας ότι ο καρκίνος προκύπτει από την αδυναμία του σώματος να αναστέλλει μια έμφυτη, προγραμματισμένη τάση πολλαπλασιασμού.[62] Μια σχετική θεωρία προτείνει ότι ο καρκίνος είναι ένας αταβισμός, μια εξελικτική επιστροφή σε μια προγενέστερη μορφή πολυκυτταρικής ζωής.[63] Τα γονίδια που είναι υπεύθυνα για την ανεξέλεγκτη κυτταρική ανάπτυξη και τη συνεργασία μεταξύ καρκινικών κυττάρων είναι πολύ παρόμοια με εκείνα που επέτρεψαν στις πρώτες πολυκύτταρες μορφές ζωής να ομαδοποιηθούν και να ανθίσουν. Αυτά τα γονίδια εξακολουθούν να υπάρχουν στα γονιδιώματα πιο πολύπλοκων μεταζωών, όπως των ανθρώπων, αν και τα πιο πρόσφατα εξελιγμένα γονίδια τα κρατούν υπό έλεγχο. Όταν τα νεότερα γονίδια ελέγχου αποτυγχάνουν για οποιονδήποτε λόγο, το κύτταρο μπορεί να επιστρέψει στον πιο πρωτόγονο προγραμματισμό του και να αναπαραχθεί εκτός ελέγχου. Η θεωρία είναι μια εναλλακτική στην αντίληψη ότι οι καρκίνοι ξεκινούν με απρόβλεπτα κύτταρα που υφίστανται εξέλιξη μέσα στο σώμα. Αντίθετα, διαθέτουν έναν σταθερό αριθμό πρωτόγονων γονιδίων που ενεργοποιούνται προοδευτικά, δίνοντάς τους πεπερασμένη μεταβλητότητα.[64] Μια άλλη εξελικτική θεωρία επαναφέρει τις ρίζες του καρκίνου στην προέλευση του ευκαρυωτικού κυττάρου (με πυρήνα) με μαζική οριζόντια μεταφορά γονιδίου, όταν τα γονιδιώματα των μολυσματικών ιών διασπάστηκαν (και ως εκ τούτου εξασθένησαν) από τον ξενιστή, αλλά τα θραύσματά τους ενσωματώθηκαν στο γονιδίωμα του ξενιστή ως ανοσολογική προστασία. Έτσι, ο καρκίνος ξεκινά όταν μια σπάνια σωματική μετάλλαξη ανασυνδυάζει τέτοια θραύσματα σε ένα λειτουργικό οδηγό πολλαπλασιασμού των κυττάρων.[65]

Συχνά, οι πολλαπλές γενετικές αλλαγές που οδηγούν σε καρκίνο μπορεί να χρειαστούν πολλά χρόνια για να συσσωρευτούν. Κατά τη διάρκεια αυτής της περιόδου, η βιολογική συμπεριφορά των προκακοήθων κυττάρων αλλάζει αργά από τις ιδιότητες των φυσιολογικών κυττάρων σε ιδιότητες που μοιάζουν με καρκίνο. Ο προκακοήθης ιστός μπορεί να έχει διακριτή εμφάνιση στο μικροσκόπιο. Μεταξύ των διακριτών χαρακτηριστικών μιας προκακοήθους βλάβης είναι ο αυξημένος αριθμός διαιρούμενων κυττάρων, η διακύμανση στο μέγεθος και το σχήμα του κυτταρικού πυρήνα, διακύμανση του κυττάρου στο μέγεθος και το σχήμα, απώλεια εξειδικευμένων κυτταρικών χαρακτηριστικών και απώλεια οργάνωσης Η δυσπλασία (Dysplasia) είναι ένας μη φυσιολογικός τύπος υπερβολικού κυτταρικού πολλαπλασιασμού που χαρακτηρίζεται από απώλεια φυσιολογικής διάταξης ιστού και κυτταρικής δομής σε προκακοήθη κύτταρα. Αυτές οι πρώιμες νεοπλασματικές αλλαγές πρέπει να διακρίνονται από την υπερπλασία (hyperplasia), μια αναστρέψιμη αύξηση της κυτταρικής διαίρεσης που προκαλείται από ένα εξωτερικό ερέθισμα, όπως μια ορμονική ανισορροπία ή χρόνιος ερεθισμός. Οι πιο σοβαρές περιπτώσεις δυσπλασίας αναφέρονται ως επιτόπιο καρκίνωμα (carcinoma in situ). Το "καρκίνωμα in situ" αναφέρεται σε μια ανεξέλεγκτη ανάπτυξη δυσπλαστικών κυττάρων που παραμένει στην αρχική του θέση και δεν έχει δείξει εισβολή σε άλλους ιστούς. Το καρκίνωμα in situ μπορεί να εξελιχθεί σε διηθητική κακοήθεια και συνήθως αφαιρείται χειρουργικά όταν ανιχνευθεί.
Κλωνική εξέλιξη
Ακριβώς όπως ένας πληθυσμός ζώων υφίσταται εξέλιξη, ένας μη ελεγχόμενος πληθυσμός κυττάρων μπορεί επίσης να υποστεί "εξέλιξη". Αυτή η ανεπιθύμητη διαδικασία ονομάζεται σωματική εξέλιξη, και είναι ο τρόπος με τον οποίο ο καρκίνος εμφανίζεται και γίνεται πιο κακοήθης με την πάροδο του χρόνου.[66] Οι περισσότερες αλλαγές στον κυτταρικό μεταβολισμό που επιτρέπουν στα κύτταρα να αναπτύσσονται με άτακτο τρόπο οδηγούν σε κυτταρικό θάνατο. Ωστόσο, μόλις ξεκινήσει ο καρκίνος, τα καρκινικά κύτταρα υποβάλλονται σε μια διαδικασία φυσικής επιλογής: τα λίγα κύτταρα με νέες γενετικές αλλαγές που ενισχύουν την επιβίωση ή την αναπαραγωγή τους πολλαπλασιάζονται γρηγορότερα και σύντομα κυριαρχούν στον αναπτυσσόμενο όγκο ως κύτταρα με λιγότερο ευνοϊκή γενετική αλλαγή.[67] Αυτός είναι ο ίδιος μηχανισμός με τον οποίο παθογόνα είδη όπως ο ανθεκτικός στη μεθικιλλίνη Staphylococcus aureus (Methicillin-resistant Staphylococcus aureus, MRSA) μπορεί να γίνει ανθεκτικός στα αντιβιοτικά και με τον οποίο ο HIV μπορεί να γίνει ανθεκτικός στα φάρμακα, και με τον οποίο οι ασθένειες των φυτών και τα εντόμων μπορούν να γίνουν ανθεκτικές στα φυτοφάρμακα. Αυτή η εξέλιξη εξηγεί γιατί μια υποτροπή καρκίνου περιλαμβάνει συχνά κύτταρα που έχουν αποκτήσει αντίσταση στα φάρμακα του καρκίνου ή αντίσταση στην ακτινοθεραπεία.
Βιολογικές ιδιότητες καρκινικών κυττάρων
Σε ένα άρθρο του 2000 από τους Douglas Hanahan και Robert Weinberg, οι βιολογικές ιδιότητες των κυττάρων κακοήθους όγκου συνοψίστηκαν ως εξής:[68]
- Απόκτηση αυτάρκειας σε σήματα ανάπτυξης, που οδηγεί σε ανεξέλεγκτη ανάπτυξη.
- Απώλεια ευαισθησίας στα σήματα κατά της ανάπτυξης, που οδηγεί επίσης σε ανεξέλεγκτη ανάπτυξη.
- Απώλεια ικανότητας για απόπτωση, που επιτρέπει την ανάπτυξη παρά τα γενετικά λάθη και τα εξωτερικά σήματα κατά της ανάπτυξης.
- Απώλεια ικανότητας για γήρανση, που οδηγεί σε απεριόριστες δυνατότητες αναπαραγωγής (αθανασία)
- Απόκτηση διατηρήσιμης αγγειογένεσης, που επιτρέπει στον όγκο να αναπτυχθεί πέρα από τους περιορισμούς της παθητικής διάχυσης θρεπτικών ουσιών.
- Απόκτηση ικανότητας εισβολής σε γειτονικούς ιστούς, η καθοριστική ιδιότητα του διηθητικού καρκινώματος.
- Απόκτηση ικανότητας διασποράς μετάστασης σε απομακρυσμένες θέσεις, ιδιότητα όψιμης εμφάνισης ορισμένων κακοήθων όγκων (καρκινωμάτων ή άλλων).
Η ολοκλήρωση αυτών των πολλαπλών βημάτων θα ήταν ένα πολύ σπάνιο γεγονός χωρίς:
- Απώλεια ικανότητας επιδιόρθωσης γενετικών σφαλμάτων, που οδηγεί σε αυξημένο ποσοστό μεταλλάξεων (γονιδιωματική αστάθεια), επιταχύνοντας έτσι όλες τις άλλες αλλαγές.
Αυτές οι βιολογικές αλλαγές είναι κλασικές στα καρκινώματα. Άλλοι κακοήθεις όγκοι μπορεί να μην χρειάζεται όες αυτές τις αλλαγές για να επιτύχουν. Για παράδειγμα, δεδομένου ότι η εισβολή ιστού και η μετατόπιση σε απομακρυσμένες τοποθεσίες είναι φυσιολογικές ιδιότητες των λευκοκυττάρων, αυτά τα βήματα δεν χρειάζονται για την ανάπτυξη της λευχαιμίας. Ούτε τα διαφορετικά βήματα αντιπροσωπεύουν απαραιτήτως μεμονωμένες μεταλλάξεις. Για παράδειγμα, η αδρανοποίηση ενός μόνο γονιδίου, που κωδικοποιεί την πρωτεΐνη p53, θα προκαλέσει γονιδιωματική αστάθεια, αποφυγή απόπτωσης και αυξημένη αγγειογένεση. Επιπλέον, δεν διαιρούνται όλα τα καρκινικά κύτταρα. Αντίθετα, ένα υποσύνολο των κυττάρων σε έναν όγκο, που ονομάζεται καρκινικά βλαστοκύτταρα, αναπαράγονται καθώς δημιουργούν διαφοροποιημένα κύτταρα.[69]
Ο καρκίνος ως ελάττωμα στις αλληλεπιδράσεις των κυττάρων
Κανονικά, μόλις τραυματιστεί ή μολυνθεί ένας ιστός, τα κατεστραμμένα κύτταρα προκαλούν φλεγμονή διεγείροντας συγκεκριμένα μοτίβα ενζυμικής δραστηριότητας και έκφρασης γονιδίου κυτοκίνης στα γύρω κύτταρα.[70][71] Εκκρίνονται διακριτές συστάδες ("συστάδες κυτοκινών") μορίων, τα οποία δρουν ως μεσολαβητές, επάγοντας τη δραστηριότητα των επόμενων καταρρακτών βιοχημικών αλλαγών.[72] Κάθε κυτοκίνη συνδέεται με συγκεκριμένους υποδοχείς σε διάφορους κυτταρικούς τύπους και κάθε κυτταρικός τύπος ανταποκρίνεται με τη σειρά του αλλάζοντας τη δραστηριότητα των ενδοκυτταρικών οδών μεταγωγής σήματος, ανάλογα με τους υποδοχείς που εκφράζει το κύτταρο και τα μόρια σηματοδότησης που υπάρχουν μέσα στο κύτταρο.[73][74] Συλλογικά, αυτή η διαδικασία επαναπρογραμματισμού προκαλεί μια σταδιακή αλλαγή στους φαινοτύπους των κυττάρων, η οποία τελικά θα οδηγήσει στην αποκατάσταση της λειτουργίας των ιστών και στην ανάκτηση της βασικής δομικής ακεραιότητας.[75][76] Ένας ιστός μπορεί έτσι να επουλωθεί, ανάλογα με την παραγωγική επικοινωνία μεταξύ των κυττάρων που υπάρχουν στο σημείο της βλάβης και του ανοσοποιητικού συστήματος.[77] Ένας βασικός παράγοντας στην επούλωση είναι η ρύθμιση της έκφρασης του γονιδίου της κυτοκίνης, η οποία επιτρέπει σε συμπληρωματικές ομάδες κυττάρων να ανταποκρίνονται στους φλεγμονώδεις μεσολαβητές με τρόπο που σταδιακά προκαλεί ουσιαστικές αλλαγές στη φυσιολογία των ιστών.[78][79][80] Τα καρκινικά κύτταρα έχουν είτε μόνιμες (γενετικές), είτε αναστρέψιμες (επιγενετικές) αλλαγές στο γονιδίωμά τους, οι οποίες αναστέλλουν εν μέρει την επικοινωνία τους με τα γύρω κύτταρα και με το ανοσοποιητικό σύστημα.[81][82] Τα καρκινικά κύτταρα δεν επικοινωνούν με το μικροπεριβάλλον των ιστών τους με τρόπο που να προστατεύει την ακεραιότητα των ιστών. Αντίθετα, η κίνηση και η επιβίωση των καρκινικών κυττάρων καθίσταται δυνατή σε θέσεις όπου μπορούν να επηρεάσουν τη λειτουργία των ιστών.[83][84] Τα καρκινικά κύτταρα επιβιώνουν με την "επανακαλωδίωση" των οδών σήματος που κανονικά προστατεύουν τον ιστό από το ανοσοποιητικό σύστημα. Αυτή η μεταβολή της ανοσολογικής απόκρισης είναι εμφανής και στα αρχικά στάδια της κακοήθειας.[85][86] Ένα παράδειγμα επανακαλωδίωσης της λειτουργίας των ιστών στον καρκίνο είναι η δραστηριότητα του μεταγραφικού παράγοντα NF-κB.[87] Το NF-κΒ ενεργοποιεί την έκφραση πολλών γονιδίων που εμπλέκονται στη μετάβαση μεταξύ φλεγμονής και αναγέννησης, τα οποία κωδικοποιούν κυτοκίνες, παράγοντες προσκόλλησης και άλλα μόρια που μπορούν να αλλάξουν τη μοίρα των κυττάρων.[88] Αυτός ο επαναπρογραμματισμός των κυτταρικών φαινοτύπων κανονικά επιτρέπει την ανάπτυξη ενός πλήρως λειτουργικού άθικτου ιστού.[89] Η δραστηριότητα του NF-κΒ ελέγχεται στενά από πολλές πρωτεΐνες, οι οποίες συλλογικά διασφαλίζουν ότι μόνο διακριτές ομάδες γονιδίων επάγονται από το NF-κΒ σε ένα δεδομένο κύτταρο και σε μια δεδομένη στιγμή.[90] Αυτή η αυστηρή ρύθμιση της ανταλλαγής σημάτων μεταξύ των κυττάρων προστατεύει τον ιστό από υπερβολική φλεγμονή και διασφαλίζει ότι διαφορετικοί τύποι κυττάρων αποκτούν σταδιακά συμπληρωματικές λειτουργίες και συγκεκριμένες θέσεις. Η αποτυχία αυτής της αμοιβαίας ρύθμισης μεταξύ του γενετικού επαναπρογραμματισμού και των κυτταρικών αλληλεπιδράσεων επιτρέπει στα καρκινικά κύτταρα να προκαλέσουν μετάσταση. Τα καρκινικά κύτταρα ανταποκρίνονται ανώμαλα στις κυτοκίνες και ενεργοποιούν καταρράκτες σημάτων που μπορούν να τα προστατεύσουν από το ανοσοποιητικό σύστημα.[87][91]
Στα ψάρια
Ο ρόλος του ιωδίου στα θαλάσσια ψάρια (πλούσια σε ιώδιο) και στα ψάρια του γλυκού νερού (με έλλειψη ιωδίου) δεν είναι πλήρως κατανοητός, αλλά έχει αναφερθεί ότι τα ψάρια του γλυκού νερού είναι πιο ευαίσθητα σε μολυσματικές και, ειδικότερα, νεοπλασματικές και αθηροσκληρωτικές ασθένειες, από τα θαλάσσια ψάρι.[92][93] Τα θαλάσσια ελασμοβράγχια ψάρια, όπως οι καρχαρίες, τα σαλάχια, κ.λπ. επηρεάζονται πολύ λιγότερο από τον καρκίνο από τα ψάρια του γλυκού νερού, και ως εκ τούτου έχουν τονώσει την ιατρική έρευνα για την καλύτερη κατανόηση της καρκινογένεσης.[94]
Προκειμένου τα κύτταρα να αρχίσουν να διαιρούνται ανεξέλεγκτα, τα γονίδια που ρυθμίζουν την κυτταρική ανάπτυξη πρέπει να απορυθμιστούν.[95] Τα πρωτοογκογονίδια είναι γονίδια που προάγουν την κυτταρική ανάπτυξη και τη μίτωση, ενώ τα ογκοκατασταλτικά γονίδια αποθαρρύνουν την κυτταρική ανάπτυξη ή σταματούν προσωρινά την κυτταρική διαίρεση για να πραγματοποιηθεί επιδιόρθωση του DNA. Τυπικά, απαιτείται μια σειρά πολλών μεταλλάξεων σε αυτά τα γονίδια πριν ένα φυσιολογικό κύτταρο μεταμορφωθεί σε καρκινικό κύτταρο.[10] Αυτή η έννοια μερικές φορές ονομάζεται "ογκοεξέλιξη (oncoevolution)". Οι μεταλλάξεις σε αυτά τα γονίδια παρέχουν τα σήματα για τα καρκινικά κύτταρα να αρχίσουν να διαιρούνται ανεξέλεγκτα. Αλλά η ανεξέλεγκτη κυτταρική διαίρεση που χαρακτηρίζει τον καρκίνο απαιτεί επίσης ότι το διαιρούμενο κύτταρο αντιγράφει όλα τα κυτταρικά συστατικά του για να δημιουργήσει δύο θυγατρικά κύτταρα. Η ενεργοποίηση της αερόβιας γλυκόλυσης (το φαινόμενο Warburg ), η οποία δεν προκαλείται απαραίτητα από μεταλλάξεις σε πρωτοογκογονίδια και ογκοκατασταλτικά γονίδια,[96] παρέχει τα περισσότερα από τα δομικά στοιχεία που απαιτούνται για την αναπαραγωγή των κυτταρικών συστατικών ενός διαιρούμενου κυττάρου και, ως εκ τούτου, είναι επίσης απαραίτητο για την καρκινογένεση.[60]
Ογκογονίδια
Τα ογκογονίδια προάγουν την κυτταρική ανάπτυξη με διάφορους τρόπους. Πολλά μπορούν να παράγουν ορμόνες, έναν "χημικό αγγελιοφόρο" μεταξύ των κυττάρων που ενθαρρύνουν τη μίτωση, η επίδραση της οποίας εξαρτάται από τη μετάδοση του σήματος του ιστού ή των κυττάρων που λαμβάνουν. Με άλλα λόγια, όταν διεγείρεται ένας ορμονικός υποδοχέας σε ένα κύτταρο δέκτη, το σήμα διοχετεύεται από την επιφάνεια του κυττάρου στον κυτταρικό πυρήνα για να επηρεάσει κάποια αλλαγή στη ρύθμιση της μεταγραφής γονιδίου σε πυρηνικό επίπεδο. Ορισμένα ογκογονίδια αποτελούν μέρος του ίδιου του συστήματος μεταγωγής σήματος ή του σήματος υποδοχέων στα ίδια τα κύτταρα και τους ιστούς, ελέγχοντας έτσι την ευαισθησία σε τέτοιες ορμόνες. Τα ογκογονίδια συχνά παράγουν μιτογόνα ή εμπλέκονται στη μεταγραφή του DNA στη πρωτεϊνοσύνθεση, η οποία δημιουργεί τις πρωτεΐνες και τα ένζυμα είναι υπεύθυνα για την παραγωγή των προϊόντων και των βιοχημικών κυττάρων που χρησιμοποιούν και αλληλεπιδρούν με αυτά. Οι μεταλλάξεις σε πρωτοογκογονίδια, τα οποία είναι τα κανονικά σε ηρεμία αντίστοιχα των ογκογονιδίων, μπορούν να τροποποιήσουν την γονιδιακή έκφραση και τη λειτουργία τους, αυξάνοντας την ποσότητα ή τη δραστικότητα της παραγόμενης πρωτεΐνης. Όταν συμβεί αυτό, τα πρωτοογκογονίδια γίνονται ογκογονίδια και αυτή η μετάβαση διαταράσσει τη φυσιολογική ισορροπία της ρύθμισης του κυτταρικού κύκλου στο κύτταρο, καθιστώντας δυνατή την ανεξέλεγκτη ανάπτυξη. Η πιθανότητα καρκίνου δεν μπορεί να μειωθεί με την αφαίρεση πρωτοογκογονιδίων από το γονιδίωμα, ακόμη κι αν αυτό ήταν δυνατό, καθώς αυτά είναι κρίσιμα για την ανάπτυξη, την επισκευή και την ομοιόσταση του οργανισμού. Μόνο όταν μεταλλάσσονται τα σήματα για ανάπτυξη γίνονται υπερβολικά. Ένα από τα πρώτα ογκογονίδια που ορίζονται στην έρευνα για τον καρκίνο είναι το ογκογονίδιο ras. Οι μεταλλάξεις στην οικογένεια των πρωτοογκογονιδίων Ras (που περιλαμβάνουν H-Ras, N-Ras και K-Ras) είναι πολύ συχνές, καθώς εντοπίζονται στο 20% έως 30% όλων των ανθρώπινων όγκων.[97]Το Ras αναγνωρίστηκε αρχικά στο γονιδίωμα του ιού σαρκώματος Harvey και οι ερευνητές εξεπλάγησαν ότι όχι μόνο αυτό το γονίδιο υπάρχει στο ανθρώπινο γονιδίωμα, αλλά και όταν απολινωθεί σε ένα διεγερτικό στοιχείο ελέγχου, θα μπορούσε να προκαλέσει καρκίνους σε καλλιέργειες κυτταρικής γραμμής.[98] Νέοι μηχανισμοί προτάθηκαν πρόσφατα ότι ο κυτταρικός μετασχηματισμός κατά τη διάρκεια της καρκινογένεσης αποφασίστηκε από το συνολικό όριο των δικτύων ογκογονιδίων (όπως η σηματοδότηση Ras), αλλά όχι από την κατάσταση του μεμονωμένου ογκογονιδίου.[99]
Πρωτοογκογονίδια
Τα πρωτοογκογονίδια προάγουν την κυτταρική ανάπτυξη με διάφορους τρόπους. Πολλά μπορούν να παράγουν ορμόνες, "χημικούς αγγελιοφόρους" μεταξύ των κυττάρων που ενθαρρύνουν τη μίτωση, η επίδραση της οποίας εξαρτάται από την μετάδοση σήματος του ιστού ή των κυττάρων που τη λαμβάνουν. Μερικά είναι υπεύθυνα για το σύστημα μεταγωγής σήματος και το σήμα υποδοχέων στα ίδια τα κύτταρα και τους ιστούς, ελέγχοντας έτσι την ευαισθησία σε τέτοιες ορμόνες. Παράγουν συχνά μιτογόνα ή εμπλέκονται στη μεταγραφή του DNA στην πρωτεϊνοσύνθεση, που δημιουργεί πρωτεΐνες και ένζυμα υπεύθυνα για την παραγωγή των προϊόντων και των βιοχημικών κυττάρων που χρησιμοποιούν και αλληλεπιδρούν με αυτά. Οι μεταλλάξεις στα πρωτοογκογονίδια μπορούν να τροποποιήσουν τη έκφραση και τη λειτουργία τους, αυξάνοντας την ποσότητα ή τη δραστικότητα της παραγόμενης πρωτεΐνης. Όταν συμβεί αυτό, γίνονται ογκογονίδια και, ως εκ τούτου, τα κύτταρα έχουν μεγαλύτερη πιθανότητα να διαιρεθούν υπερβολικά και ανεξέλεγκτα. Η πιθανότητα καρκίνου δεν μπορεί να μειωθεί με την αφαίρεση πρωτοογκογονιδίων από το γονιδίωμα, καθώς είναι κρίσιμα για την ανάπτυξη, την επισκευή και την ομοιόσταση του σώματος. Μόνο όταν μεταλλάσσονται τα σήματα για ανάπτυξη γίνονται υπερβολικά. Είναι σημαντικό να σημειωθεί ότι ένα γονίδιο που έχει έναν ρόλο προαγωγής της ανάπτυξης μπορεί να αυξήσει το καρκινογόνο δυναμικό ενός κυττάρου, υπό την προϋπόθεση ότι ενεργοποιούνται όλοι οι απαραίτητοι κυτταρικοί μηχανισμοί που επιτρέπουν την ανάπτυξη.[100] Αυτή η κατάσταση περιλαμβάνει επίσης την αδρανοποίηση συγκεκριμένων ογκοκατασταλτικών γονιδίων (βλ. παρακάτω). Εάν δεν πληρούται η προϋπόθεση, το κύτταρο μπορεί να σταματήσει να αναπτύσσεται και να πεθάνει. Αυτό καθιστά τον προσδιορισμό του σταδίου και του τύπου του καρκινικού κυττάρου που αναπτύσσεται υπό τον έλεγχο ενός δεδομένου ογκογονιδίου ζωτικής σημασίας για την ανάπτυξη στρατηγικών θεραπείας.
Ογκοκατασταλτικά γονίδια
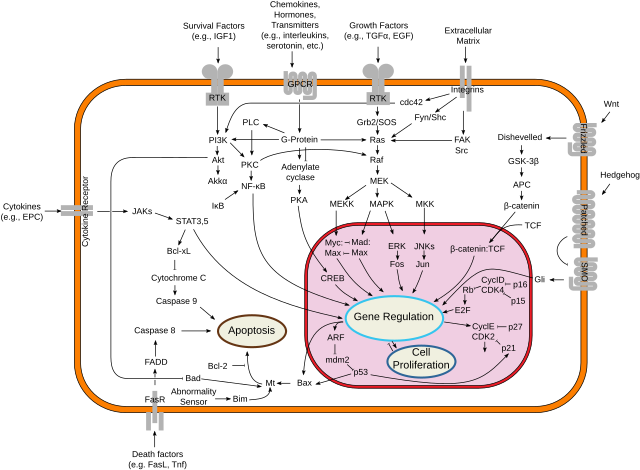
Τα ογκοκατασταλτικά γονίδια κωδικοποιούν κατά του πολλαπλασιασμού σημάτων και πρωτεϊνών που καταστέλλουν τη μίτωση και την ανάπτυξη των κυττάρων. Γενικά, τα ογκοκατασταλτικά είναι παράγοντες μεταγραφής που ενεργοποιούνται από κυτταρική καταπόνηση, ή βλάβη του DNA. Συχνά, η βλάβη του DNA θα προκαλέσει την παρουσία ελεύθερα αιωρούμενου γενετικού υλικού καθώς και άλλων σημάτων, και θα πυροδοτήσει ένζυμα και μονοπάτια που οδηγούν στην ενεργοποίηση των ογκοκατασταλτικών γονιδίων. Οι λειτουργίες τέτοιων γονιδίων είναι να σταματήσουν την εξέλιξη του κυτταρικού κύκλου προκειμένου να πραγματοποιηθεί η επιδιόρθωση του DNA, αποτρέποντας τη μετάδοση μεταλλάξεων στα θυγατρικά κύτταρα. Η πρωτεΐνη p53, ένα από τα πιο σημαντικά μελετημένα ογκοκατασταλτικά γονίδια, είναι ένας μεταγραφικός παράγοντας που ενεργοποιείται από πολλούς κυτταρικούς παράγοντες καταπόνησης, όπως η υποξία και η βλάβη από υπεριώδη ακτινοβολία. Παρά το ότι σχεδόν οι μισοί από όλους τους καρκίνους που πιθανώς περιλαμβάνουν αλλοιώσεις στο p53, η ογκοκατασταλτική του λειτουργία είναι ελάχιστα κατανοητή. Το p53 έχει σαφώς δύο λειτουργίες: η μία έναν πυρηνικό ρόλο ως μεταγραφικός παράγοντας και η άλλη έναν κυτταροπλασματικό ρόλο στη ρύθμιση του κυτταρικού κύκλου, την κυτταρική διαίρεση και την απόπτωση. Το φαινόμενο Warburg είναι η προτιμησιακή χρήση της γλυκόλυσης για ενέργεια ώστε να διατηρηθεί η ανάπτυξης του καρκίνου. Το p53 έχει αποδειχθεί ότι ρυθμίζει τη μετατόπιση από την αναπνευστική στη γλυκολυτική οδό.[101] Ωστόσο, μια μετάλλαξη μπορεί να βλάψει το ίδιο το ογκοκατασταλτικό γονίδιο, ή το μονοπάτι του σήματος που το ενεργοποιεί, "σβήνοντάς το". Η αμετάβλητη συνέπεια αυτού είναι ότι η επιδιόρθωση του DNA παρεμποδίζεται ή αναστέλλεται: η βλάβη του DNA συσσωρεύεται χωρίς επιδιόρθωση, οδηγώντας αναπόφευκτα σε καρκίνο. Οι μεταλλάξεις των ογκοκατασταλτικών γονιδίων που εμφανίζονται σε κύτταρα βλαστικής γραμμής μεταβιβάζονται στον απόγονο και αυξάνουν την πιθανότητα για διαγνώσεις καρκίνου στις επόμενες γενιές. Τα μέλη αυτών των οικογενειών έχουν αυξημένη επίπτωση και μειωμένη καθυστέρηση πολλαπλών όγκων. Οι τύποι όγκων είναι τυπικοί για κάθε τύπο ογκοκατασταλτικής γονιδιακής μετάλλαξης, με ορισμένες μεταλλάξεις να προκαλούν συγκεκριμένους καρκίνους και άλλες μεταλλάξεις να προκαλούν άλλες. Ο τρόπος κληρονομικότητας των μεταλλαγμένων ογκοκατασταλτών είναι ότι ένα προσβεβλημένο μέλος κληρονομεί ένα ελαττωματικό αντίγραφο από τον έναν γονέα και ένα κανονικό αντίγραφο από τον άλλο. Για παράδειγμα, άτομα που κληρονομούν ένα μεταλλαγμένο αλληλόμορφο p53 (και επομένως είναι ετερόζυγα για το μεταλλαγμένο p53) μπορεί να αναπτύξουν μελανώματα και καρκίνο του παγκρέατος, γνωστό ως σύνδρομο Λι-Φραουμένι. Άλλα σύνδρομα κληρονομικών ογκοκατασταλτικπών γονιδίων περιλαμβάνουν μεταλλάξεις του ρετινοβλαστώματος της πρωτεΐνης, που συνδέονται με ρετινοβλάστωμα και γονιδιακές μεταλλάξεις APC, που συνδέονται με αδενοπολυποδίαση καρκίνου του παχέος εντέρου. Ο καρκίνος αδενοπολυποδίασης του παχέος εντέρου σχετίζεται με χιλιάδες πολύποδες στο παχύ έντερο όταν είναι νεαρός, οδηγώντας σε καρκίνο του παχέος εντέρου σε σχετικά νεαρή ηλικία. Τέλος, οι κληρονομικές μεταλλάξεις στα BRCA1 και BRCA2 οδηγούν σε πρώιμη έναρξη του καρκίνου του μαστού. Η ανάπτυξη του καρκίνου προτάθηκε το 1971 να εξαρτάται από τουλάχιστον δύο μεταλλάξεις. Σε αυτό που έγινε γνωστό ως Υπόθεση Knudson (υπόθεση δύο χτυπημάτων, two-hit hypothesis), μια κληρονομική, βλαστικής σειράς μετάλλαξη σε ένα ογκοκατασταλτικό γονίδιο θα προκαλούσε καρκίνο μόνο εάν ένα άλλο γεγονός μετάλλαξης συνέβη αργότερα στη ζωή του οργανισμού, απενεργοποιώντας το άλλο αλληλόμορφο αυτού του ογκοκατασταλτικού γονιδίου.[102] Συνήθως, τα ογκογονίδια είναι επικρατή γονίδια, καθώς περιέχουν μεταλλάξεις αυξημένης λειτουργικότητας (gain-of-function mutations), ενώ τα μεταλλαγμένα ογκοκατασταλτικά είναι υπολειπόμενα γονίδια, καθώς περιέχουν μεταλλάξεις απώλειας λειτουργικότητας (loss-of-function mutations). Κάθε κύτταρο έχει δύο αντίγραφα του ίδιου γονιδίου, ένα από κάθε γονέα, και στις περισσότερες περιπτώσεις η αύξηση των μεταλλάξεων λειτουργικότητας σε ένα μόνο αντίγραφο ενός συγκεκριμένου πρωτοογκογονιδίου είναι αρκετή για να γίνει αυτό το γονίδιο πραγματικό ογκογονίδιο. Από την άλλη πλευρά, οι μεταλλάξεις απώλειας λειτουργικότητας πρέπει να συμβούν και στα δύο αντίγραφα ενός ογκοκατασταλτικού γονιδίου για να καταστεί αυτό το γονίδιο εντελώς μη λειτουργικό. Ωστόσο, υπάρχουν περιπτώσεις στις οποίες ένα μεταλλαγμένο αντίγραφο ενός ογκοκατασταλτικού γονιδίου μπορεί να καταστήσει το άλλο αντίγραφο άγριου τύπου μη λειτουργικό. Αυτό το φαινόμενο ονομάζεται επικρατές αρνητικό αποτέλεσμα (dominant negative effect) και παρατηρείται σε πολλές μεταλλάξεις p53. Το μοντέλο δύο χτυπημάτων του Knudson αμφισβητήθηκε πρόσφατα από αρκετούς ερευνητές. Η αδρανοποίηση ενός αλληλόμορφου ορισμένων ογκοκατασταλτικών γονιδίων είναι αρκετή για να προκαλέσει όγκους. Αυτό το φαινόμενο ονομάζεται απλοανεπάρκεια (haploinsufficiency) και έχει αποδειχθεί από μια σειρά πειραματικών προσεγγίσεων. Οι όγκοι που προκαλούνται από απλοανεπάρκεια έχουν συνήθως μια μεταγενέστερη ηλικία έναρξης σε σύγκριση με εκείνους από μια διαδικασία δύο χτυπημάτων.[103]
Πολλαπλές μεταλλάξεις

Γενικά, απαιτούνται μεταλλάξεις και στους δύο τύπους γονιδίων για την εμφάνιση καρκίνου. Για παράδειγμα, μια μετάλλαξη που περιορίζεται σε ένα ογκογονίδιο θα καταστέλλεται από τον φυσιολογικό έλεγχο της μίτωσης και τα ογκοκατασταλτικά γονίδια, σύμφωνα με την υπόθεση Knudson.[8] Μια μετάλλαξη σε ένα μόνο ογκοκατασταλτικό γονίδιο δεν θα προκαλούσε επίσης καρκίνο, λόγω της παρουσίας πολλών αντιγράφων ασφαλείας των γονιδίων που διπλασιάζουν τις λειτουργίες του. Μόνο όταν αρκετά πρωτοογκογονίδια έχουν μεταλλαχθεί σε ογκογονίδια και αρκετά ογκοκατασταλτικά γονίδια έχουν απενεργοποιηθεί ή καταστραφεί, τότε τα σήματα για την κυτταρική ανάπτυξη υπερισχύουν των σημάτων για τη ρύθμισή τους και η κυτταρική ανάπτυξη γρήγορα ξεφεύγει από τον έλεγχο.[10] Συχνά, επειδή αυτά τα γονίδια ρυθμίζουν τις διαδικασίες που αποτρέπουν τις περισσότερες βλάβες στα ίδια τα γονίδια, ο ρυθμός των μεταλλάξεων αυξάνεται καθώς μεγαλώνει κανείς, επειδή η βλάβη του DNA σχηματίζει έναν βρόχο ανατροφοδότησης. Η μετάλλαξη των ογκοκατασταλτικών γονιδίων που μεταβιβάζονται στην επόμενη γενιά όχι μόνο κυττάρων, αλλά και στους απογόνους τους, μπορεί να προκαλέσει αυξημένες πιθανότητες κληρονομικότητας των καρκίνων. Τα μέλη αυτών των οικογενειών έχουν αυξημένη επίπτωση και μειωμένη καθυστέρηση πολλαπλών όγκων. Ο τρόπος κληρονομικότητας των μεταλλαγμένων ογκοκατασταλτών είναι ότι το προσβεβλημένο μέλος κληρονομεί ένα ελαττωματικό αντίγραφο από έναν γονέα και ένα κανονικό αντίγραφο από έναν άλλο. Επειδή οι μεταλλάξεις στα ογκοκατασταλτικά δρουν με υπολειπόμενο τρόπο (σημειώστε, ωστόσο, υπάρχουν εξαιρέσεις), η απώλεια του φυσιολογικού αντιγράφου δημιουργεί τον φαινότυπο καρκίνου. Για παράδειγμα, άτομα που είναι ετερόζυγα για μεταλλάξεις p53 είναι συχνά θύματα του συνδρόμου Λι-Φραουμένι και αυτά που είναι ετερόζυγα για μεταλλάξεις πρωτεΐνης αμφιβληστροειδούς αναπτύσσουν ρετινοβλάστωμα. Με παρόμοιο τρόπο, μεταλλάξεις στο γονίδιο αδενωματώδους πολυποδίασης κόλου συνδέονται με αδενοπολυποδισιακό καρκίνο του παχέος εντέρου (adenopolyposis colon cancer), με χιλιάδες πολύποδες στο παχύ έντερο ενώ είναι νέοι, ενώ μεταλλάξεις σε BRCA1 και BRCA2 οδηγούν σε πρώιμη έναρξη του καρκίνου του μαστού. Μια νέα ιδέα που ανακοινώθηκε το 2011 είναι μια ακραία εκδοχή πολλαπλών μεταλλάξεων, που ονομάζεται χρωμοθρύψη (chromothripsis) από τους υποστηρικτές της. Αυτή η ιδέα, που επηρεάζει μόνο το 2-3% των περιπτώσεων καρκίνου, αν και έως και το 25% των καρκίνων των οστών, περιλαμβάνει την καταστροφική συντριβή ενός χρωμοσώματος σε δεκάδες ή εκατοντάδες κομμάτια και στη συνέχεια την εσφαλμένη επανατοποθέτηση. Αυτή η θραύση πιθανώς λαμβάνει χώρα όταν τα χρωμοσώματα συμπιέζονται κατά τη διάρκεια της φυσιολογικής κυτταρικής διαίρεσης, αλλά το έναυσμα για το θρυμματισμό είναι άγνωστο. Σύμφωνα με αυτό το μοντέλο, ο καρκίνος εμφανίζεται ως αποτέλεσμα ενός μεμονωμένου γεγονότος και όχι της αργής συσσώρευσης πολλαπλών μεταλλάξεων.[104]
Μη μεταλλαξιογόνα καρκινογόνα
Πολλά μεταλλαξιογόνα είναι επίσης καρκινογόνα, αλλά ορισμένα καρκινογόνα δεν είναι μεταλλαξιογόνα. Παραδείγματα καρκινογόνων που δεν είναι μεταλλαξιογόνα περιλαμβάνουν το οινόπνευμα και οιστρογόνα. Αυτά πιστεύεται ότι προάγουν τους καρκίνους μέσω της διεγερτικής τους δράσης στον ρυθμό της κυτταρικής μίτωσης. Οι ταχύτεροι ρυθμοί μίτωσης αφήνουν όλο και λιγότερες ευκαιρίες για επισκευαστικά ένζυμα να επιδιορθώσουν το κατεστραμμένο DNA κατά την αντιγραφή του DNA, αυξάνοντας την πιθανότητα ενός γενετικού σφάλματος. Ένα σφάλμα που γίνεται κατά τη μίτωση μπορεί να οδηγήσει στο να λάβουν τα θυγατρικά κύτταρα εσφαλμένο αριθμό χρωμοσωμάτων, κάτι που οδηγεί σε ανευπλοειδία και μπορεί να οδηγήσει σε καρκίνο.
Ο ρόλος των λοιμώξεων
Βακτηριακός
Το Ελικοβακτηρίδιο του πυλωρού μπορεί να προκαλέσει γαστρικό καρκίνωμα. Παρόλο που τα δεδομένα διαφέρουν μεταξύ των διαφόρων χωρών, συνολικά περίπου το 1% έως 3% των ατόμων που έχουν μολυνθεί με το ελικοβακτηρίδιο του πυλωρού αναπτύσσουν γαστρικό καρκίνωμα στη διάρκεια της ζωής τους σε σύγκριση με το 0,13% των ατόμων που δεν είχαν λοίμωξη από ελικοβακτηρίδιο του πυλωρού.[105][106] Η λοίμωξη ελικοβακτηρίου του πυλωρού είναι πολύ διαδεδομένη. Όπως αξιολογήθηκε το 2002, υπάρχει στους γαστρικούς ιστούς στο 74% των μεσήλικων ενηλίκων στις αναπτυσσόμενες χώρες και στο 58% στις ανεπτυγμένες χώρες.[107] Δεδομένου ότι το 1% έως 3% των μολυσμένων ατόμων είναι πιθανό να αναπτύξουν γαστρικό καρκίνο,[108] ο γαστρικός καρκίνος που επάγεται από το ελικοβακτηρίδιο του πυλωρού είναι η τρίτη υψηλότερη αιτία θνησιμότητας από καρκίνο παγκοσμίως από το 2018.[109] Η λοίμωξη από ελικοβακτηρίδιο του πυλωρού δεν προκαλεί συμπτώματα στο 80% περίπου των μολυσμένων.[110] Περίπου το 75% των ατόμων που μολύνθηκαν με ελικοβακτηρίδιο του πυλωρού αναπτύσσουν γαστρίτιδα.[111] Έτσι, η συνήθης συνέπεια της λοίμωξης από ελικοβακτηρίδιο του πυλωρού είναι χρόνια ασυμπτωματική γαστρίτιδα.[112] Λόγω της συνήθους έλλειψης συμπτωμάτων, όταν τελικά διαγνωστεί ο καρκίνος του στομάχου, είναι συχνά αρκετά προχωρημένος. Περισσότεροι από τους μισούς ασθενείς με καρκίνο του στομάχου έχουν μετάσταση στους λεμφαδένες όταν διαγιγνώσκονται αρχικά.[113] Η γαστρίτιδα που προκαλείται από το H. pylori συνοδεύεται από φλεγμονή, που χαρακτηρίζεται από διήθηση ουδετερόφιλων και μακροφάγων στο γαστρικό επιθήλιο, η οποία ευνοεί τη συσσώρευση προφλεγμονωδών κυτοκινών και δραστικών μορφών οξυγόνου/δραστικών μορφών αζώτου (reactive oxygen species/reactive nitrogen species, ROS/RNS).[114] Η ουσιαστική παρουσία ROS/RNS προκαλεί βλάβη στο DNA συμπεριλαμβανομένης της 8-οξο-2'-δεοξυγουανοσίνης. (8-OHdG).[114] Εάν το μολυσματικό H. pylori φέρει το κυτταροτοξικό γονίδιο cagA (υπάρχει σε περίπου 60% των απομονώσεων δυτικών στελεχών και σε υψηλότερο ποσοστό για τις ασιατικές απομονώσεις), μπορεί να αυξήσει το επίπεδο του 8-OHdG στα γαστρικά κύτταρα κατά 8 φορές, ενώ εάν το Η. pylori δεν φέρουν το γονίδιο cagA, η αύξηση του 8-OHdG είναι περίπου 4 φορές.[115] Εκτός από την οξειδωτική βλάβη του DNA της 8-OHdG, η λοίμωξη του ελικοβακτηριδίου του πυλωρού προκαλεί άλλες χαρακτηριστικές βλάβες στο DNA, συμπεριλαμβανομένων των θραύσεων του διπλού κλώνου του DNA.[116] Το ελικοβακτηρίδιο του πυλωρού προκαλεί επίσης πολλές επιγενετικές αλλοιώσεις που σχετίζονται με την ανάπτυξη καρκίνου.[117][118] Αυτές οι επιγενετικές αλλοιώσεις οφείλονται στη μεθυλίωση θέσεων CpG σε προαγωγείς γονιδίων του επαγόμενου H. pylori[117]. και στην αλλοιωμένη έκφραση πολλαπλών μικροRNA του επαγόμενου H. pylori.[118] Όπως αξιολογήθηκε από τους Santos και Ribeiro [119] Η λοίμωξη του ελικοβακτηρίου του πυλωρού σχετίζεται με επιγενετικά μειωμένη αποτελεσματικότητα του μηχανισμού επιδιόρθωσης του DNA, που ευνοεί τη συσσώρευση μεταλλάξεων και τη γονιδιωματική αστάθεια καθώς και τη γαστρική καρκινογένεση. Συγκεκριμένα, οι Raza κ.α.[120] έδειξαν ότι η έκφραση των δύο πρωτεϊνών επιδιόρθωσης του DNA, ERCC1 και PMS2, μειώθηκε σοβαρά μόλις η λοίμωξη του H. pylori είχε εξελιχθεί για να προκαλέσει δυσπεψία. Η δυσπεψία εμφανίζεται σε περίπου 20% των μολυσμένων ατόμων.[121] Επιπλέον, όπως αξιολογείται από τους Raza κ.α.,[120] η ανθρώπινη γαστρική λοίμωξη με H. pylori προκαλεί επιγενετικά μειωμένη πρωτεϊνική έκφραση των πρωτεϊνών επιδιόρθωσης του DNA MLH1, MGMT και MRE11. Η μειωμένη επιδιόρθωση του DNA παρουσία αυξημένης βλάβης του DNA αυξάνει τις καρκινογόνες μεταλλάξεις και είναι πιθανόν μια σημαντική αιτία της καρκινογένεσης του ελικοβακτηρίου του πυλωρού.
Ιογενής
Επιπλέον, πολλοί καρκίνοι προέρχονται από μία ιική λοίμωξη. Αυτό ισχύει ιδιαίτερα σε ζώα όπως τα πουλιά, αλλά λιγότερο σε ανθρώπους. Το 12% των ανθρώπινων καρκίνων μπορεί να αποδοθεί σε ιογενή λοίμωξη.[122] Ο τρόπος των όγκων που προκαλούνται από τον ιό μπορεί να χωριστεί σε δύο, σε οξύ μετασχηματισμό ή αργά μετασχηματιζόμενο. Σε ιούς που μετασχηματίζονται οξύτατα, τα ιικά σωματίδια φέρουν ένα γονίδιο που κωδικοποιεί ένα υπερδραστήριο ογκογονίδιο που ονομάζεται ιικό ογκογονίδιο (viral-oncogene, v-onc) και το μολυσμένο κύτταρο μετασχηματίζεται μόλις εκφραστεί το v-onc. Αντίθετα, σε ιούς που μετασχηματίζονται αργά, το γονιδίωμα του ιού εισάγεται, ειδικά καθώς η εισαγωγή ιικού γονιδιώματος είναι υποχρεωτικό μέρος των ρετροϊών, κοντά σε ένα πρωτοογκογονίδιο στο γονιδίωμα του ξενιστή. Ο ιικός προαγωγέας, ή άλλα στοιχεία ρύθμισης της μεταγραφής, με τη σειρά τους, προκαλούν υπερέκφραση αυτού του πρωτοογκογονιδίου, το οποίο, με τη σειρά του, προκαλεί ανεξέλεγκτο κυτταρικό πολλαπλασιασμό. Επειδή η εισαγωγή του ιικού γονιδιώματος δεν είναι ειδική για τα πρωτοογκογονίδια και η πιθανότητα εισαγωγής κοντά σε αυτό το πρωτοογκογονίδιο είναι χαμηλή, οι αργά μετασχηματιζόμενοι ιοί έχουν πολύ μεγάλη καθυστέρηση όγκου σε σύγκριση με τον οξύ μετασχηματιζόμενο ιό, ο οποίος ήδη φέρει το ιικό ογκογονίδιο. Ιοί που είναι γνωστό ότι προκαλούν καρκίνο όπως HPV (καρκίνος του τραχήλου της μήτρας), Ηπατίτιδα Β (καρκίνος του ήπατος) και Ιός Έπσταϊν-Μπαρ (Epstein-Barr virus, EBV) ( ένας τύπος λεμφώματος), είναι όλοι ιοί DNA. Θεωρείται ότι όταν ο ιός μολύνει ένα κύτταρο, εισάγει ένα μέρος του δικού του DNA κοντά στα γονίδια ανάπτυξης των κυττάρων, προκαλώντας κυτταρική διαίρεση. Η ομάδα των αλλαγμένων κυττάρων που σχηματίζονται από την πρώτη κυτταρική διαίρεση έχουν όλες το ίδιο ιικό DNA κοντά στα γονίδια ανάπτυξης των κυττάρων. Η ομάδα των αλλαγμένων κυττάρων είναι πλέον ειδική, επειδή ένας από τους φυσιολογικούς ελέγχους στην ανάπτυξη έχει χαθεί. Ανάλογα με τη θέση τους, τα κύτταρα μπορεί να καταστραφούν μέσω ακτινοβολίας, χημικών ουσιών από τον καπνό του τσιγάρου και φλεγμονής από βακτηριακή μόλυνση ή άλλους ιούς. Κάθε κύτταρο έχει κάποια πιθανότητα βλάβης. Τα κύτταρα συχνά πεθαίνουν εάν καταστραφούν, λόγω αποτυχίας μιας ζωτικής διαδικασίας ή του ανοσοποιητικού συστήματος, ωστόσο, μερικές φορές η βλάβη θα εξαλείψει ένα μόνο γονίδιο του καρκίνου. Σε ένα ηλικιωμένο άτομο, υπάρχουν χιλιάδες, δεκάδες χιλιάδες ή εκατοντάδες χιλιάδες νεκρά κελιά. Η πιθανότητα να εμφανιστεί κάποιος καρκίνος είναι πολύ μικρή. Όταν η βλάβη συμβαίνει σε οποιαδήποτε περιοχή αλλαγμένων κυττάρων, συμβαίνει κάτι διαφορετικό. Κάθε ένα από τα κύτταρα έχει τη δυνατότητα ανάπτυξης. Τα αλλαγμένα κύτταρα θα διαιρούνται γρηγορότερα όταν η περιοχή καταστραφεί από φυσικούς, χημικούς ή ιικούς παράγοντες. Ένας φαύλος κύκλος έχει δημιουργηθεί: Η καταστροφή της περιοχής θα προκαλέσει τη διαίρεση των αλλαγμένων κελιών, προκαλώντας μεγαλύτερη πιθανότητα να αντιμετωπίσουν εξουδετερώσεων. Αυτό το μοντέλο καρκινογένεσης είναι δημοφιλές γιατί εξηγεί γιατί αναπτύσσονται οι καρκίνοι. Θα ήταν αναμενόμενο ότι τα κύτταρα που έχουν υποστεί βλάβη από την ακτινοβολία θα πέθαιναν ή τουλάχιστον θα ήταν χειρότερα επειδή έχουν λιγότερα γονίδια που λειτουργούν. Οι ιοί αυξάνουν τον αριθμό των γονιδίων που λειτουργούν. Μια σκέψη είναι ότι μπορεί να καταλήξουμε με χιλιάδες εμβόλια για να αποτρέψουμε κάθε ιό που μπορεί να αλλάξει τα κύτταρά μας. Οι ιοί μπορούν να έχουν διαφορετικές επιπτώσεις σε διαφορετικά μέρη του σώματος. Μπορεί να είναι δυνατό να αποτραπεί ένας αριθμός διαφορετικών καρκίνων με ανοσοποίηση έναντι ενός ιικού παράγοντα. Είναι πιθανό ότι ο HPV, για παράδειγμα, έχει ρόλο σε καρκίνους των βλεννογόνων του στόματος.
Ελμινθίαση
Ορισμένα παρασιτικά σκουλήκια είναι γνωστό ότι είναι καρκινογόνα.[123] Αυτά περιλαμβάνουν:
- Clonorchis sinensis (ο οργανισμός που προκαλεί κλωνορχίαση (Clonorchiasis)) και Opisthorchis viverrini (που προκαλεί οπισθορχίαση (Opisthorchiasis)) σχετίζονται με χολαγγειοκαρκίνωμα (cholangiocarcinoma).[124]
- Το γένος σχιστόσωμα (Schistosoma) (οι οργανισμοί που προκαλούν Σχιστοσωμίαση) σχετίζεται με καρκίνο της ουροδόχου κύστης.
Επιγενετική
Η Επιγενετική είναι η μελέτη της ρύθμισης της γονιδιακής έκφρασης μέσω χημικών, μη μεταλλαγμένων αλλαγών στη δομή του DNA. Η θεωρία της επιγενετικής στην παθογένεια του καρκίνου είναι ότι οι μη μεταλλαγμένες αλλαγές στο DNA μπορούν να οδηγήσουν σε αλλαγές στη γονιδιακή έκφραση. Κανονικά, τα ογκογονίδια είναι σιωπηλά, για παράδειγμα, λόγω μεθυλίωσης του DNA. Η απώλεια αυτής της μεθυλίωσης μπορεί να προκαλέσει την ανώμαλη έκφραση των ογκογονιδίων, οδηγώντας σε παθογένεση καρκίνου. Γνωστοί μηχανισμοί επιγενετικής αλλαγής περιλαμβάνουν μεθυλίωση του DNA και μεθυλίωση ή ακετυλίωση πρωτεϊνών ιστόνης που συνδέονται με χρωμοσωμικό DNA σε συγκεκριμένες θέσεις. Οι κατηγορίες φαρμάκων, γνωστές ως αναστολείς HDAC και μεθυλομεταφοράση του DNA, μπορούν να επαναρυθμίσουν την επιγενετική σηματοδότηση στο καρκινικό κύτταρο. Οι επιμεταλλάξεις περιλαμβάνουν μεθυλίωση ή απομεθυλίωση των νησίδων CpG των περιοχών γονιδίων προαγωγέων, που έχουν ως αποτέλεσμα την καταστολή ή την αποκαταστολή, αντίστοιχα, της γονιδιακής έκφρασης.[125][126][127] Οι επιμεταλλάξεις μπορούν επίσης να προκύψουν με ακετυλίωση, μεθυλίωση, φωσφορυλίωση ή άλλες αλλοιώσεις στις ιστόνες, δημιουργώντας έναν κώδικα ιστόνης που καταστέλλει ή ενεργοποιεί την έκφραση γονιδίων και τέτοιες επιμεταλλάξεις ιστόνης μπορεί να είναι σημαντικοί επιγενετικοί παράγοντες στον καρκίνο.[128][129] Επιπρόσθετα, η καρκινογόνος επιμετάλλαξη μπορεί να συμβεί μέσω αλλαγών στην αρχιτεκτονική των χρωμοσωμάτων που προκαλούνται από πρωτεΐνες όπως η HMGA2.[130] Μια περαιτέρω πηγή επιμετάλλαξης οφείλεται στην αυξημένη ή μειωμένη έκφραση των μικροRNA (miRNAs). Για παράδειγμα, η επιπλέον έκφραση του miR-137 μπορεί να προκαλέσει μείωση της έκφρασης 491 γονιδίων και το miR-137 αποσιωπάται επιγενετικά στο 32% των καρκίνων του παχέος εντέρου[15]
Βλαστοκύτταρα καρκίνου
Ένας νέος τρόπος εξέτασης της καρκινογένεσης προέρχεται από την ενσωμάτωση των ιδεών της αναπτυξιακής βιολογίας στην ογκολογία. Η υπόθεση των καρκινικών βλαστοκυττάρων προτείνει ότι τα διαφορετικά είδη κυττάρων σε έναν ετερογενή όγκο προέρχονται από ένα μόνο κύτταρο, που ονομάζεται καρκινικό βλαστοκύτταρο. Τα καρκινικά βλαστοκύτταρα μπορεί να προκύψουν από μετασχηματισμό ενηλίκων βλαστοκυττάρων ή διαφοροποιημένων κυττάρων μέσα σε ένα σώμα. Αυτά τα κύτταρα παραμένουν ως υποσυστατικά του όγκου και διατηρούν τις βασικές ιδιότητες των βλαστοκυττάρων. Δημιουργούν μια ποικιλία κυττάρων, είναι ικανά για αυτοανανέωση και ομοιοστατικό έλεγχο.[131] Επιπλέον, η υποτροπή του καρκίνου και η εμφάνιση μετάστασης αποδίδονται επίσης σε αυτά τα κύτταρα. Η υπόθεση του καρκινικού βλαστοκυττάρου δεν έρχεται σε αντίθεση με προηγούμενες έννοιες της καρκινογένεσης. Η υπόθεση των καρκινικών βλαστοκυττάρων είναι ένας προτεινόμενος μηχανισμός που συμβάλλει στην ετερογένεια του όγκου.
Κλωνική εξέλιξη
Ενώ οι γενετικές και επιγενετικές αλλοιώσεις στα ογκοκατασταλτικά γονίδια και στα ογκογονίδια αλλάζουν τη συμπεριφορά των κυττάρων, αυτές οι αλλαγές, τελικά, καταλήγουν σε καρκίνο μέσω των επιπτώσεών τους στον πληθυσμό των νεοπλασματικών κυττάρων και στο μικροπεριβάλλον τους.[66] Τα μεταλλαγμένα κύτταρα στα νεοπλάσματα ανταγωνίζονται για χώρο και πόρους. Έτσι, ένας κλώνος με μετάλλαξη σε ένα ογκοκατασταλτικό γονίδιο ή ογκογονίδιο θα επεκταθεί μόνο σε ένα νεόπλασμα εάν αυτή η μετάλλαξη δώσει στον κλώνο ανταγωνιστικό πλεονέκτημα έναντι των άλλων κλώνων και των φυσιολογικών κυττάρων στο μικροπεριβάλλον του.[132] Έτσι, η διαδικασία της καρκινογένεσης είναι τυπικά μια διαδικασία της δαρβινικής εξέλιξης, γνωστή ως σωματική ή κλωνική εξέλιξη.[67] Επιπλέον, υπό το φως των δαρβινιστικών μηχανισμών καρκινογένεσης, έχει θεωρηθεί ότι οι διάφορες μορφές καρκίνου μπορούν να κατηγοριοποιηθούν ως εφηβικοί και γεροντολογικοί. Επί του παρόντος διεξάγεται ανθρωπολογική έρευνα για τον καρκίνο ως μια φυσική εξελικτική διαδικασία μέσω της οποίας η φυσική επιλογή καταστρέφει περιβαλλοντικά κατώτερους φαινοτύπους, ενώ υποστηρίζει άλλους. Σύμφωνα με αυτή τη θεωρία, ο καρκίνος διακρίνεται σε δύο διαφορετικούς τύπους: από τη γέννηση έως το τέλος της εφηβείας (περίπου 20 ετών) τελεολογικά τείνει προς τη δυναμική της υποστηρικτικής ομάδας και από τη μέση ηλικία έως το θάνατο (περίπου ηλικίες 40+) τελεολογικά τείνει μακριά από τη δυναμική της υπερπληθυσμένης ομάδας.
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.