Loading AI tools
organische Verbindung Aus Wikipedia, der freien Enzyklopädie
Kohlensäuredimethylester oder Dimethylcarbonat ist eine organische chemische Verbindung, die als Dimethylester der Kohlensäure gesehen werden kann.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
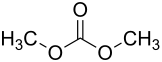 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Kohlensäuredimethylester | |||||||||||||||
| Andere Namen | ||||||||||||||||
| Summenformel | C3H6O3 | |||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit angenehmem Geruch[2] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 90,08 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
1,07 g·cm−3 (20 °C)[3] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt | ||||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit | ||||||||||||||||
| Brechungsindex |
1,3687 (20 °C)[4] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Dimethylcarbonat kann in einer Zweiphasenreaktion durch Umsetzung von Methanol mit Phosgen oder Methylchlorformiat in konzentrierter Natronlauge gewonnen werden.[6] Eine modernere Synthese verläuft als direkte oxidative Carbonylierung von Methanol mittels Kohlenmonoxid und Sauerstoff in Gegenwart von Kupferkatalysatoren.[7][8]
Dimethylcarbonat ist eine leichtentzündliche, farblose Flüssigkeit. Bei Normaldruck siedet die Verbindung bei 90 °C.[9] Der kritische Punkt wird bei einer Temperatur Tc = 284 °C und einem Druck Pc = 48 bar mit einer kritischen Dichte von 3,97 kg·l−1 erreicht.[10]
Dimethylcarbonat bildet leicht entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt von 14 °C.[2][11] Der Explosionsbereich liegt zwischen 3,26 Vol.‑% (122 g/m³) als untere Explosionsgrenze (UEG) und 12,87 Vol.‑% als obere Explosionsgrenze (OEG).[2] Die Sauerstoffgrenzkonzentration liegt bei 8,0 %.[12] Die Zündtemperatur beträgt 458 °C.[2][11] Der Stoff fällt somit in die Temperaturklasse T1.
Im Gemisch mit Ethylencarbonat wird die Verbindung in nichtwässrigen Elektrolytlösungen für Lithiumbatterien verwendet.[13] In der organischen Synthese wird Dimethylcarbonat als Methylierungsreagenz eingesetzt. Außerdem ersetzt es zunehmend das sehr giftige Phosgen bei der Herstellung von Polycarbonat-Kunststoffen.[14] Die Verwendung als Kraftstoffkomponente wird diskutiert.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.