Loading AI tools
Protocatechusäure (3,4-Dihydroxybenzoesäure) ist eine aromatische Verbindung, die sich sowohl von der Benzoesäure als auch vom Brenzcatechin (1,2-Dihydroxybenzol) ableitet. Die Struktur besteht aus einem Benzolring mit einer angefügten Carboxygruppe (–COOH) und zwei Hydroxygruppen (–OH) als Substituenten. Sie gehört zur Gruppe der Dihydroxybenzoesäuren, ist in freier Form in den Früchten des Japanischen Sternanis' (Illicium religiosum) enthalten und entsteht bei der Alkalischmelze zahlreicher Naturstoffe, z. B. aus Catechinen, aus verschiedenen Harzen, dem Farbstoff Maklurin und mehreren Anthocyanen.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Protocatechusäure | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C7H6O4 | |||||||||||||||||||||
| Kurzbeschreibung |
hellbrauner Feststoff[2] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 154,12 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| pKS-Wert |
4,48 (COOH; 25 °C)[3] | |||||||||||||||||||||
| Löslichkeit |
schlecht in Wasser (20 g·l−1 bei 20 °C)[2] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||

Protocatechusäure kommt in essbarem Gemüse, Obst und Nüssen vor, beispielsweise in Oliven,[5][6] Naturreis[5] und Pekannüssen[5][6]. Sie kommt auch in der Borstigen Taigawurzel,[6] Ginkgo,[6] Aprikosen,[6] Mönchspfeffer,[6] den Blättern des Gewürznelkenbaum,[6] und Brennnesseln[7] vor.
Chemische Synthese
Synthetisch stellt man Protocatechusäure aus p-Hydroxybenzoesäure dar; man führt diese in m-Chlor-p-hydroxybenzoesäure über und erhitzt letztere mit Ätzkali unter Druck.

Die Carboxylierung mit einer Kolbe-Schmitt-Reaktion durch Erhitzen von Brenzcatechin mit Ammoniumcarbonat im geschlossenen Rohr liefert nur schlechte Ausbeuten, in wässriger Lösung findet keine Reaktion statt.[8]
Eine weitere Synthese geht vom Vanillin aus und führt über die Demethylierung der Vanillinsäure bzw. ihres Kaliumsalzes zur Protocatechusäure:[9]

Beim Erhitzen von Piperonylsäure mit Salzsäure oder Iodwasserstoffsäure entsteht ebenfalls Protocatechusäure.[10][11] Als Nebenprodukt werden äquimolare Mengen Formaldehyd abgespalten.

Biosynthese
Protocatechualdehyd kann enzymatisch zur Protocatechusäure oxidiert werden.[12]
Protocatechusäure und schmilzt bei etwa 202–204 °C[2] und zersetzt sich dabei durch Decarboxylierung zu Brenzcatechin und Kohlenstoffdioxid. Ihre wässrige Lösung wird nach Zusatz von Eisenchlorid blaugrün. Diese Farbe schlägt nach Zugabe von wenig Soda oder Ammoniak erst nach violett, dann nach rot um. Protocatechusäure wirkt stark reduzierend.
Mit elementarem Brom bildet sich bei Raumtemperatur 5-Bromprotocatechusäure[13], die beim Schmelzen mit Kaliumcarbonat zur Gallussäure umgewandelt wird.[14]

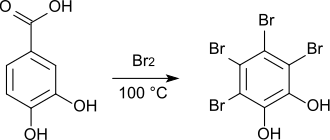
Wird die Bromierung bei 100 °C durchgeführt, entsteht unter Abspaltung von Kohlendioxid Tetrabrombrenzcatechin.[13]
Zur qualitativen und quantitativen Bestimmung kann nach adäquater Probenvorbereitung die Kopplung der UPLC mit der Massenspektrometrie und auch die HPTLC eingesetzt werden.[15][16][17]
Die Wirkung von Protocatechusäure auf lebende Zellen ist momentan Gegenstand der Forschung und wird noch kontrovers diskutiert. So wurde gezeigt, dass es ein potentes Antioxidationsmittel mit einer etwa 10-mal stärkeren Wirkung als α-Tocopherol ist.[18] In hohen Dosen jedoch, bei beispielsweise 10 mM, kann es aber auch oxidativen Stress in Zellkulturen induzieren.[19]
Gegenüber Krebszellen zeigt Protocatechusäure verschiedene Effekte. In menschlichen Magenkrebszellen (Zellen eines Magenadenokarzinoms) und andere Tumorzellen des Verdauungstraktes induziert es die Apoptose und wirkt daher im Sinne eines Krebsmittels.[5] Es liegen aber auch Studiendaten vor, die auf einen gegenteiligen Effekt von Protocatechusäure hinweisen. So induziert es die Zellteilung in neuralen Stammzellen und blockiert dort die Apoptose.[20] Auch in Hautkrebszellen der Maus wurde dies beobachtet. Wenn dort chemisch durch 12-O-Tetradecanoylphorbol-13-acetat Krebszellen induziert wurden, konnte Protocatechusäure die Tumorbildung sogar noch verstärken.[18] Wenn man in vitro maligne Zelllinien der menschlichen Unterkieferspeicheldrüse erzeugt, konnte Protocatechusäure diese Krebszellen nicht abtöten.[19]
- Paul Karrer: Lehrbuch der organischen Chemie. 10. Auflage. Georg Thieme, Stuttgart 1948, S. 569.
- Deutsche Chemische Gesellschaft: Beilsteins Handbuch der Organischen Chemie. Bd. 10, 4. Auflage, Springer, 1927: (Syst.Nr. 1105) H 389, EI 187, EII 260
- Untersuchung der antiviralen Aktivität (PDF-Datei; 527 kB)
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.
