Loading AI tools
chemische Verbindung Aus Wikipedia, der freien Enzyklopädie
Lithiumhexafluoroarsenat(V), Li[AsF6] ist ein Salz des Lithiums aus der Gruppe der Hexafluoroarsenate.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
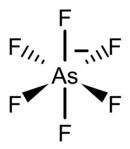 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Lithiumhexafluoroarsenat(V) | ||||||||||||||||||
| Summenformel | Li[AsF6] | ||||||||||||||||||
| Kurzbeschreibung |
weißes Pulver[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 195,85 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Löslichkeit |
nahezu unlöslich in Wasser[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Lithiumhexafluoroarsenat(V) ist ein potentielles Elektrolytmaterial für Batterien.[2]
Das Salz besitzt in Methylacetat eine Leitfähigkeit, welche zwischen −20 °C und 50 °C bestehen bleibt.[3]
Die Verbindung ist bei oraler Einnahme oder Inhalation toxisch.[1]
Starke Oxidationsmittel und Reduktionsmittel sowie starke Säuren und Basen verursachen heftige Reaktionen mit Lithiumhexafluoroarsenat(V). Bei der Zersetzung entstehen Fluorwasserstoff, Arsenoxide und Lithiumoxid.[2][1]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.