Loading AI tools
chemische Verbindung Aus Wikipedia, der freien Enzyklopädie
Der Hagemann-Ester ist ein Carbonsäureester, der neben der Esterfunktion auch über eine Ketonfunktion verfügt. Die Verbindung eignet sich als Zwischenprodukt zur Herstellung diverser Naturstoffe, beispielsweise mehrerer Terpene.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
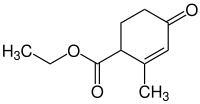 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Hagemann-Ester | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C10H14O3 | ||||||||||||||||||
| Kurzbeschreibung |
dunkelgelbe, klare Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 182,22 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[1] | ||||||||||||||||||
| Dichte |
1,078 g·cm−3 bei 27 °C[1] | ||||||||||||||||||
| Siedepunkt |
268–272 °C[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Die erste Publikation zu der Verbindung stammt aus dem Jahr 1893 mit Ergebnissen aus Carl Hagemanns Doktorarbeit.[2] Hergestellt wurde sie damals aus Ethylacetoacetat durch Umsetzung mit Diiodmethan und Natriummethanolat. 1894 klärte Emil Knoevenagel die Struktur eindeutig auf. Später wurden weitere Synthesen entwickelt und die Bezeichnung Hagemann-Ester kam auf.[3]

In der ursprünglichen Methode nach Hagemann werden zwei Äquivalente Ethylacetoacetat und ein Äquivalent Diiodmethan mit Natriummethanolat umgesetzt. Dadurch entsteht zunächst Methylenbisacetessigester, der zum Hagemann-Ester cyclisiert.[4]
In der Methode nach Knoevenagel werden unter Katalyse von Piperidin zwei Moleküle Ethylacetoacetat mit Formaldehyd kondensiert.[4]
In der Methode nach Newman und Lloyd werden 2-Methoxy-1,3-butadien und Ethyl-2-butinoat in einer Diels-Alder-Reaktion umgesetzt und das Reaktionsprodukt zum Hagemann-Ester hydrolysiert.[4]
In der Methode nach Mannich und Fourneau wird in situ aus Diethylmethyl-(3-oxobutyl)ammoniumiodid das Methylvinylketon gewonnen, welches mit Ethylacetoacetat ein Addukt bildet, das wiederum mit Natriumethanolat cyclisiert wird.[4]
Heute ist der Hagemann-Ester kommerziell erhältlich und wird oft nach der Methode von Knoevenagel hergestellt.[3]
Der Hagemann-Ester kann in vielfältigen Reaktionen zu anderen relevanten Verbindungen umgesetzt werden. Verschiedene Reaktionen zur selektiven Alkylierung sind bekannt.[4] Durch Umsetzungen mit Basen und Alkylhalogeniden ergeben sich je nach Reaktionsbedingungen in Position 1 oder 3 substituierte Derivate. Mit Lithiumdimethylcuprat entsteht eine 2,2-Dimethylverbindung. Der Ester und seine Derivate können verseift und decarboxyliert werden. Der Ester kann außerdem zu einem gesättigten Keton hydriert werden. Auch verschiedene Diene für Diels-Alder-Reaktionen, sowie Benzolderivate, Bi- und Tricyclen lassen sich aus Hagemanns Ester herstellen.[3] Verbindungen, die aus dem Hagemann-Ester hergestellt werden können, sind Vermiculin, Pinene, sowie Steroidderivate.[4][5][6]
Analog zur Herstellungsmethode nach Mannich kann aus Isopropylacetessigester und Methylvinylketon ein 1-Isopropylderivat des Hagemann-Esters hergestellt werden. Dieses kann zu Piperiton, Menthol und Thymol umgesetzt werden.[3]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.