Chlorid uranitý je anorganická sloučenina s chemickým vzorcem UCl3. Poprvé byl připraven Péligotem v roce 1842 během přípravy kovového uranu.[1]
| chlorid uranitý | |
|---|---|
 | |
| Obecné | |
| Systematický název | Chlorid uranitý |
| Anglický název | Uranium(III) chloride |
| Německý název | Uran(III)-chlorid |
| Sumární vzorec | UCl3 |
| Vzhled | Zelená pevná látka |
| Identifikace | |
| Registrační číslo CAS | 10025-93-1 |
| PubChem | 167444 |
| SMILES | Cl[U](Cl)Cl |
| InChI | InChI=1S/3ClH.U/h3*1H;/q;;;+3/p-3
Key: SAWLVFKYPSYVBL-UHFFFAOYSA-K |
| Vlastnosti | |
| Molární hmotnost | 344,39 g/mol |
| Teplota tání | 837 °C |
| Teplota varu | 1657 °C |
| Hustota | 5,5 g/cm3 |
| Rozpustnost ve vodě | dobře rozpustný |
| Struktura | |
| Krystalová struktura | hexagonální |
| Hrana krystalové mřížky | a = 745,2 pm, c = 432,8 pm |
Některá data mohou pocházet z datové položky. | |
Příprava
Chlorid uranitý lze připravit redukcí chloridu uraničitého kovovým uranem v tavenině chloridu sodného a draselného při teplotě 670–710 °C:[2]
- 3 UCl4 + U → 4 UCl3
Lze jej také připravit redukcí chloridu uraničitého vodíkem:[3][4]
- 2 UCl4 + H2 → 2 UCl3 + 2 HCl
Lze jej připravit reakcí hydridu uranitého s chlorovodíkem při teplotě 350 °C:[5]
- UH3 + 3 HCl → UCl3 + 3 H2
Vlastnosti
Chlorid uranitý je radioaktivní zelená pevná krystalická hygroskopická látka, která je rozpustná ve vodě.[6]
Krystalická struktura
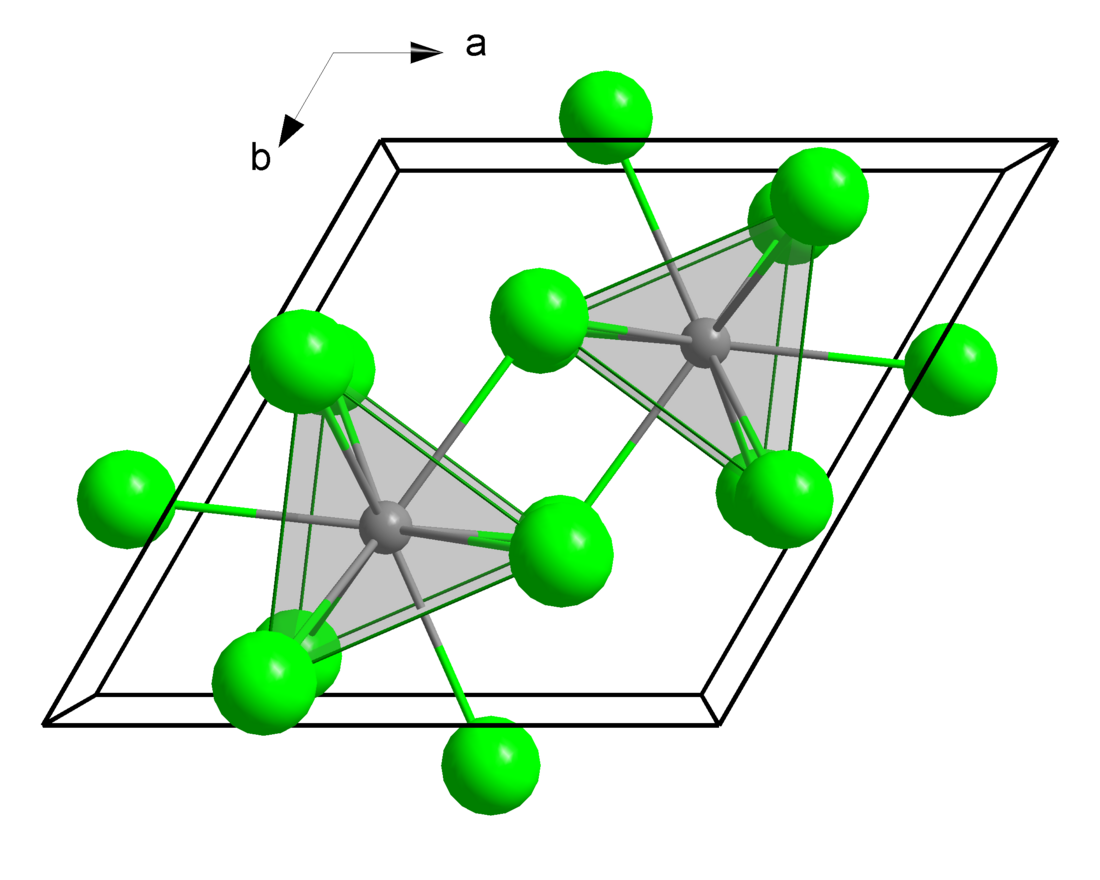
Strukturu chloridu uranitého má mnoho dalších sloučenin. Každý atom uranu je obklopen devíti atomy chloru, čímž tvoří trojboký hranol s třemi přidanými vrcholy. Tato struktura se často vyskytuje u dalších lanthanoidů a aktinoidů. Chlorid uranitý krystalizuje v hexagonální soustavě s prostorou grupou P63/m (číslo 176), mřížkovými parametry a = 745 pm a c = 433 pm a dvěma molekulami na elementární buňku.[5] Strukturu chloridu uranitého má například chlorid neptunitý, plutonitý, americitý, curitý a antimonitý.
Hydráty
Jsou známy tři solváty chloridu uranitého:
- UCl3 . 2 H2O . 2 CH3CN
- UCl3 . 6 H2O
- UCl3 . 7 H2O
Všechny lze připravit redukcí chloridu uraničitého v acetonitrilu se specifickým množstvím vody a kyseliny propionové.[7]
Využití
Chlorid uranitý je využíván k přípravě různých metalocenů uranu, například při reakci tetrahydrofuranu s methylcyklopentadienylem sodným.[8] Využívá se také jako katalyzátor, například při reakci tetrahydridohlinitanu lithného s alkeny za vzniku alkylových sloučenin s hliníkem.[9] Roztavený chlorid uranitý se také používá při přepracovávání vyhořelého jaderného paliva.[10][11]
Bezpečnost
Podobně jako jiné rozpustné sloučeniny uranu se chlorid uranitý snadno vstřebává do lidského těla.[12] Při vdechnutí nebo požití je vysoce toxický. Existuje také riziko kumulace v lidském těle, především v játrech a ledvinách. Stejně jako všechny sloučeniny uranu je radioaktivní.
Odkazy
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.