Boronové kyseliny jsou sloučeniny odvozené od kyseliny borité náhradou jedné ze tří hydroxylových skupin alkylovou nebo arylovou funkční skupinou.[1] Protože tyto sloučeniny obsahují vazbu mezi atomy uhlíku a boru, tak spadají mezi organoborany. Boronové kyseliny fungují jako Lewisovy kyseliny. Jsou jedinečné svou schopností vvratně vytvářet kovalentní komplexy například se sacharidy, aminokyselinami a hydroxyskořicovými kyselinami (molekulami obsahujícími 1,2- nebo 1,3-substituované Lewisovy zásady (alkoholy, aminy, karboxyláty). pKa kyseliny borité je ~9, boronové kyseliny ovšem mohou tvořit tetraedrické komplexy s pKa okolo 7. Používají se například k navazování sacharidů za účelem jejich fluorescenční detekce nebo selektivního transportu přes membrány.
Boronové kyseliny se používají jako stavební prvky a meziprodukty v organické syntéze, nejčastěji při Suzukiových reakcích. Jejich hlavním využitím jsou transmetalace jejich organických zbytků na přechodné kovy.
Sloučenina bortezomib, obsahující tento druh funkční skupiny, se používá při chemoterapii. Atom boru v této molekule blokuje funkci některých proteazomů, které by mohly rozkládat bílkoviny. Boronové kyseliny se vážou na serinová aktivní místa a jsou součástí prasečích inhibitorů pankreatické lipázy,[2] subtilisinu[3] a proteázy Kex2.[4] Deriváty boronových kyselin mohou také inhibovat lidské acylproteinthioesterázy 1 a 2, na které cílí protirakovinná léčiva ze skupiny ras.[5]
Boronové kyseliny mají nízkou toxicitu, což je jedním z důvodů oblíbenosti Suzukiových reakcí při vývoj i a výrobě léčiv. Velká část běžně používaných boronových kyselin a jejich derivátů ovšem vykazuje pozitivní Amesův test a má mutagenní účinky. Mutagenita je pravděpodobně způsobena tvorbou organických radikálů oxidací boronových kyselin vzdušným kyslíkem.[6]
V roce 1860 popsal Edward Frankland přípravu a izolaci první boronové kyseliny, kyseliny ethylboronové. Nejprve provedl reakci diethylzinku s triethylboritanem za vzniku triethylboranu. Tato látka byla poté oxidována na vzduchu na kyselinu ethylboronovou.[7][8]
Nyní se používá několik různých syntetických postupů a komerčně dostupných je mnoho na vzduchu stálých boronových kyselin.
Boronové kyseliny mají obvykle vysoké teploty tání. Mají tendence tvořit anhydridy odštěpením molekul vody, často tak vznikají cyklické trimery.
| Kyselina | R | Struktura | Molární hmotnost | CAS | Teplota tání °C |
|---|---|---|---|---|---|
| Kyselina fenylboronová | Fenyl | 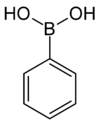 | 121,93 | 98-80-6 | 216–219 |
| Kyselina 2-thienylboronová | Thiofen |  | 127,96 | 6165-68-0 | 138–140 |
| Kyselina methylboronová | Methyl |  | 59,86 | 13061-96-6 | 91–94 |
| Kyselina cis-propenylboronová | propen | 85,90 | 7547-96-8 | 65–70 | |
| Kyselina trans-propenylboronová | propen | 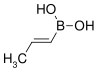 | 85,90 | 7547-97-9 | 123–127 |
Příprava
Boronové kyseliny lze získat několika způsoby; nejčastější je reakce organolithných či organohořečnatých sloučenin s estery kyseliny borité.[9][10][11][12]
Příkladem může být příprava kyseliny fenylboronové z fenylmagnesiumbromidu a trimethylborátu následovaná hydrolýzou[13]
- PhMgBr + B(OMe)3 → PhB(OMe)2 + MeOMgBr
- PhB(OMe)2 + H2O → PhB(OH)2 + MeOH
Další možností je transmetalační reakce arylsilanu (RSiR3) s bromidem boritým (BBr3) za vzniku RBBr2 a hydrolýza tohoto meziproduktu.
Třetí způsob spočívá v palladiem katalyzovaných reakcích arylhalogenidů a aryltriflátů s diboronovými estery; tato metoda se nazývá Mijaurova borylace. Místo esterů je možné použít diboronové kyseliny nebo tetrahydroxydibor ([B(OH2)]2).[14][15][16]
Boronové estery (také nazývané boronátové estery) jsou estery vytvořené z boronových kyselin a alkoholů nebo fenolů.
Tyto sloučeniny lze získat z borátových esterů kondenzací s jednosytnými alkoholy a dioly. Kyselina fenylboronová může podléhat autokondenzaci za vzniku cyklického trimeru nazývaného trifenylboroxin.[17]
| Boronový ester | Alkohol | Strukturní vzorec | Molární hmotnost | Číslo CAS | Teplota varu (°C) |
|---|---|---|---|---|---|
| Pinakolester kyseliny allylboronové | pinakol |  | 168,04 | 72824-04-5 | 50–53 (5 mmHg) |
| Trimethylenglykolester kyseliny fenylboronové | trimethylenglykol |  | 161,99 | 4406-77-3 | 106 (2 mmHg) |
| Diisopropoxymethylboran | isopropylalkohol | 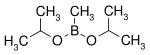 | 144,02 | 86595-27-9 | 105 -107 |
Sloučeniny s pětičlennými cykly obsahujícími řetězce C–O–B–O–C se nazývají dioxaborolany a obdobné sloučeniny s šestičlennými cykly jsou dioxaborinany.
Suzukiovy reakce
Boronové kyseliny se používají při Suzukiových reakcích, kde atomy boru vyměňují své arylové skupiny s alkoxyskupinami navázanými na palladium.
: |
|
() |
Chanovo–Lamovo párování
Při Chanově–Lamově párování reagují alkyl-, alkenyl-, nebo arylboronové kyseliny se sloučeninami obsahujícími vazby N–H nebo O–H za přítomnosti měďnaté soli, jako je například octan měďnatý, kyslíku a zásady (což může být například pyridin)[18][19] za vzniku nové vazby uhlík-dusík nebo uhlík–kyslík; příkladem může být následující reakce 2-pyridonu s kyselinou trans-1-hexenylboronovou:
Mechanismus reakce zahrnuje deprotonaci aminu, koordinaci aminu na měďnaté centrum, transmetalaci (přesun alkylboronové skupiny na měď a octanu měďnatého na bor), oxidaci Cu2+ na Cu3+ kyslíkem a redukčně eliminační přeměnu Cu3+ na Cu+ za vzniku konečného produktu. Probíhá také přímá redukční eliminace Cu2+ na Cu0, která je ovšem mnohem pomalejší. V katalytických systémech slouží kyslík také k obnově měďnatého katalyzátoru.
Liebeskindovo–Sroglovo párování
V Liebeskindově–Sroglově párování reagují thioestery s boronovými kyselinami za tvorby ketonů.
Konjugované adice
Organické zbytky boronových kyselin mohou fungovat jako nukleofily při konjugovaných adičních reakcích, pokud jsou přítomny kovy. Při jedné studii byla provedena reakce pinakolesteru allylboronové kyseliny s dibenzylidenacetonem:[20]
Dalším příkladem konjugované adice je reakce graminu s kyselinou fenylboronovou katalyzovaná dimerem cyklooktadienrhodiumchloridu:[21]
Oxidace
Boronové estery lze oxidovat na příslušné alkoholy za přítomnosti zásady a peroxidu vodíku.
Homologace
- Při homologacích boronových esterů se alkylové skupiny přesouvají z boru tvořícího boronát na atom uhlíku:[22]
- Homologace boronového esteru
- Využití homologace
Při těchto reakcích se používá dichlormethyllithium na přeměnu boronových esterů v boronáty. Lewisova kyselina následně spustí přesmyk alkylu za odštěpení jednoho chloru. Nakonec organokovová sloučenina, například Grignardovo činidlo, odštěpí druhý atom chloru a RCH2 skupina se naváže na vazbu C-B.
Další reakcí, která zahrnuje přesun alkylboronátu, je Petasisova reakce.
Elektrofilní allylové přesuny
Allylboronové estery se mohou zapojit do elektrofilních allylových přesmyků, podobně jako sloučeniny křemíku do Sakuraiových reakcí.[23]:
Hydrolýza
Hydrolýzu boronových esterů na příslušné boronové kyseliny a alkoholy je možné provést například se zapojením thionylchloridu a pyridinu.[24] Arylboronové kyseliny a estery mohou být hydrolyzovány na fenoly působením hydroxylaminu za pokojové teploty.[25]
C–H párovací reakce
Sloučenina bis(pinakoláto)dibor[26] reaguje s aromatickými heterocykly[27] nebo jednoduchými areny[28] za tvorby arylboronátových esterů; katalyzátory jsou [IrCl(COD)2] (obměna Crabtreeova katalyzátoru) a zásada 4,4′-di-terc-butyl-2,2′-bipyridin:
V jedné modifikaci této reakce se používá pouze stechiometrické množství arenu místo velkého přebytku a druhým reaktantem je namísto bis(pinakoláto)diboru levnější pinakolboran:[29]
Na rozdíl od běžné elektrofilní aromatické substituce, kde převažují elektronové efekty, zde regioselektivitu ovlivňují výhradně sterické vlastnosti iridiového komplexu. Příkladem je meta-bromace m-xylenu, u které při běžné variantě vzniká ortho produkt:[30]
Protonolýza
Protodeborace je chemická reakce, při níž dochází k protonolýze boronové kyseliny (nebo jiné organoboranové sloučeniny) zánikem vazby uhlík-bor a jejím nahrazením vazbou uhlík-vodík. Protodeborace je nežádoucí vedlejší reakcí, často se objevuje při kovy katalyzovaných párovacích reakcích, do kterých jsou zapojené boronové kyseliny (jako je Suzukiova reakce). U dané boronové kyseliny je náchylnost k protodeboraci značně proměnlivá a závisí na mnoha faktorech, jako jsou reakční podmínky a organické substituenty navázané na kyselinu:

Rozlišování sacharidů

Kovalentní interakce mezi boronovými kyselinami a hydroxylovými skupinami, například v alkoholech a karboxylovými kyselinami ve vodných roztocích probíhají rychle a jsou vratné. Rovnováha mezi boronovou kyselinou a hydroxylovými skupinami sacharidů může být využita k tvorbě senzorů detekujících přítomnost sacharidů.[32] Jednou z hlavních výhod tohoto postupu je schopnost boronových kyselin překonat problémy spojené s navazováním neutrálních částic ve vodném prostředí.[33] Při správném uspořádání vede přidání terciárního aminu do těchto supramolekulárních systémů k jejich navazování při fyziologickém pH, což umožňuje využití signálních mechanismů, jako je fotoindukovaný přenos elektronu k řízené fluorescenci, která poskytuje údaje o navazování sloučenin.
Tuto metodu je možné použít například v systémech pro sledování obsahu glukózy v krvi u pacientů majících diabetes mellitus. Protože se zde využívají optické senzory, tak je tento způsob jen minimálně invazivní.
Další možností je využití kontaktních čoček obsahujících senzorové molekuly založené na boronových kyselinách k detekci koncentrace glukózy v oční tekutině.[34]
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.


![The Suzuki reaction {\displaystyle {\begin{matrix}{}\\{\ce {{R1-BY2}+R2-X->[{\underset {\text{catalyst}}{\text{Pd}}}][{\text{Base}}]R1-R2}}\\{}\end{matrix}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/c35df36f38fec8abbc8e9d1d9f04e9b2687ae245)








