estudi del sistema immunitari biològic From Wikipedia, the free encyclopedia
La immunologia és l'estudi de les bases biològiques i bioquímiques dels mecanismes de defensa del cos contra patògens, com ara bacteris, virus i fongs, o altres substàncies alienes, com ara toxines i verins. És una subdisciplina de les ciències de la salut.[1] La immunologia també estudia els desajustaments i les disfuncions d'aquests mecanismes de defensa. L'objecte d'estudi de la immunologia és el sistema immunitari, un sistema de processos cel·lulars i moleculars que s'encarreguen de reconèixer i eliminar els patògens i les substàncies alienes. En conjunt, aquests processos formen la resposta immunitària. A causa del paper central que juga el sistema immunitari humà en una gran varietat de malalties, la immunologia té una gran importància en medicina a l'hora de comprendre, prevenir, diagnosticar i tractar les malalties.

Existeixen diverses branques de la immunologia. La immunoquímica estudia l'estructura dels antígens, els anticossos i les bases químiques de les reaccions immunitàries. La immunogenètica estudia l'aspecte genètic de les reaccions immunitàries, com per exemple els mecanismes de producció d'anticossos, de receptors dels limfòcits T i de complexos antigènics. La immunopatologia i la immunologia clínica estudien les disfuncions del sistema immunitari, com per exemple les al·lèrgies, la formació de tumors i les malalties autoimmunitàries.

Els documents més antics coneguts que contenen referències a fenòmens immunitaris rellevants daten del 430 aC. Durant la pandèmia d'Atenes, que tingué lloc durant la Guerra del Peloponès, l'historiador Tucídides afirma que les úniques persones que gosaven ocupar-se dels malalts eren les que ja havien patit la malaltia i havien sobreviscut.[2] Als voltants del 100 aC, a la Xina, es tenen notícies de la transmissió deliberada de la verola a persones sanes amb l'objectiu d'immunitzar-les. Aquesta pràctica, que implicava la inoculació de pus de persones lleugerament malaltes a persones sanes (un mètode d'immunització denominat variolització), s'estengué molt a partir del segle xv, especialment a la Xina, l'Índia i Turquia. A través de Mary Wortley Montagu, dona de l'ambaixador britànic a Constantinoble, que permeté que el seu fill fos immunitzat d'aquesta manera, la variolització arribà a Anglaterra als voltants del 1722 i en els anys següents s'estengué per la resta d'Europa.
En aquell mateix temps, el metge rural anglès Edward Jenner fou informat per altres metges amb els quals mantenia correspondència que les munyidores que s'havien infectat amb la verola bovina, inofensiva per als humans, o bé no eren afectades per les freqüents epidèmies de verola, o bé si eren afectades, es restablien ràpidament.[3] Després d'observar a consciència aquest fenomen, el 14 de maig del 1796 Jenner vacunà James Phipps, un nen sa de vuit anys, amb líquid intersticial provinent d'una pústula d'una munyidora infectada amb la verola bovina. Després que el nen es restablís fàcilment de la verola bovina, Jenner l'infectà amb verola autèntica. El nen també es recuperà d'aquesta infecció sense patir símptomes greus. En comparació amb la variolització, el procediment de Jenner oferia certs avantatges decisius: les persones vacunades amb la verola bovina no presentaven les pústules típiques de la verola, ni les cicatrius resultants; no hi havia possibilitats que la vacuna causés la mort i les persones vacunades no representaven cap risc de contagi. Per això, avui en dia Edward Jenner és considerat el fundador de la immunologia.

Una fita en el desenvolupament de la immunologia, que marcà l'inici de la investigació dirigida, fou el desenvolupament d'una vacuna contra la ràbia; ho aconseguí Louis Pasteur el 1885.[4] El 6 de juliol del 1885, la inoculà a un nen de nou anys anomenat Joseph Meister, que dos dies abans havia estat mossegat per un gos infectat. D'aquesta manera, Joseph Meister esdevingué la primera persona en la història de la medicina que sobrevisqué a una infecció de la ràbia. Al llarg de l'any següent, aquesta vacuna fou injectada a 350 persones infectades més, cap de les quals morí de ràbia. Tres anys abans, Robert Koch ja havia descobert el patogen de la tuberculosi, i poc temps després la prova de la tuberculina, que permetia detectar una infecció de tuberculosi basant-se en la resposta immunitària.[5]
El 1888, Pierre Paul Émile Roux i Alexandre Émile Jean Yersin descobriren la toxina de la diftèria. Dos anys més tard, Emil Adolf von Behring i Shibasaburo Kitasato detectaren l'antitoxina contra la diftèria en el sèrum de pacients que havien sobreviscut a la malaltia. Behring començà a utilitzar aquest antisèrum per al tractament de la diftèria.[6] En reconeixement als resultats de la seva investigació, el 1901 guanyà el primer Premi Nobel de Medicina o Fisiologia.[7] El bacteriòleg belga Jules Baptiste Vincent Bordet descobrí el 1898 que escalfar el sèrum a 55 °C gairebé no tenia efecte sobre la seva capacitat d'unir-se a certes substàncies químiques, però el seu efecte bactericida desapareixia. Basant-se en aquest descobriment, postulà l'existència d'un component sensible a la calor en el sèrum, necessari perquè aquest fes el seu efecte sobre els bacteris, i li donà el nom d'alexina. Durant els anys següents, Paul Ehrlich treballà intensament en la investigació d'aquest component i introduí el concepte de complement, encara utilitzat avui en dia.

A principis del segle xx, la investigació immunològica es dividí en dos corrents. Els humoralimmunòlegs, els més prominents dels quals foren Paul Ehrlich i Emil Adolf von Behring, donaven suport a la teoria que calia buscar les bases de la immunitat en substàncies del sèrum, és a dir, les antitoxines. Als voltants del 1900, i durant les dècades següents, aquesta fou la posició predominant. L'altre corrent era el dels immunòlegs cel·lulars, que es basaven principalment en l'obra de George Nuttall i la d'Ilià Ilitx Métxnikov entre el 1883 i el 1884. Basant-se en investigacions sobre l'efecte dels leucòcits sobre els bacteris, Métxnikov pogué demostrar la importància dels processos cel·lulars en la defensa contra patògens. Com quedaria demostrat més endavant, ambdós aspectes tenen una importància semblant en el funcionament del sistema immunitari i de la resposta immunitària. Tanmateix, no fou fins als voltants del 1940 que les teories dels immunòlegs cel·lulars trobaren un i reconeixement general, i que la idea que els anticossos són el mecanisme principal del sistema immunitari fou abandonada.
El 1901, Karl Landsteiner descobrí el sistema AB0 dels grups sanguinis, fent una important contribució a la comprensió del sistema immunitari. Clemens Peter Freiherr von Pirquet observà el 1906 que els pacients que rebien un tractament repetit amb sèrum de cavall tenien una reacció violenta a la segona donació. Pirquet encunyà el terme «al·lèrgia» per referir-se a aquesta reacció d'hipersensibilitat. Emil von Dungern i Ludwik Hirszfeld publicaren el 1910 les seves conclusions sobre l'heretabilitat dels grups sanguinis, i per tant, els primers resultats sobre la genètica dels components del sistema immunitari. En aquesta obra, també encunyaren la nova distinció «AB0». Tanmateix, no esdevingué oficial arreu del món fins al 1928. El 1917, Karl Landsteiner descrigué el concepte dels haptens, petites molècules que poden desencadenar una reacció immunitària amb la producció d'anticossos específics per mitjà de la seva unió a una proteïna. El 1926, Lloyd Felton aconseguí extreure anticossos del sèrum. A la dècada del 1930, Michael Heidelberger descobrí que els anticossos són proteïnes. A més a més, juntament amb Elvin A. Kabat, fou capaç de demostrar que corresponen a la fracció gamma de les globulines presents en el sèrum. Cap a la mateixa època, John Marrack desenvolupà per primer cop una teoria sobre el reconeixement específic dels antígens pels anticossos.

A la dècada del 1930, mentre estudiava el rebuig de tumors trasplantats a ratolins, Peter Alfred Gorer descobrí l'antigen H-2 del ratolí i, amb ell, el primer complex d'histocompatibilitat principal (MHC). També en el curs d'estudis sobre el rebuig de trasplantament, Peter Medawar i Thomas Gibson pogueren aclarir funcions importants de les cèl·lules immunitàries. Així començà finalment l'acceptació de la immunologia cel·lular. El 1948, Astrid Fagraeus descobrí que els anticossos són produïts pels limfòcits B del plasma. Un any més tard, Frank Macfarlane Burnet i Frank Fenner publicaren la seva hipòtesi sobre la tolerància immunitària, que seria confirmada alguns anys més tard per Jacques Miller amb el descobriment de l'eliminació de limfòcits T autoreactius al tim. El 1957, Frank Macfarlane Burnet descrigué la teoria de la selecció clonal com a principi central de la immunitat adaptiva.[8]
El 1957, el britànic Alick Isaacs i el suís Jean Lindenmann descobriren, durant la seva investigació dels efectes d'infeccions víriques sobre cultius de cèl·lules, que durant la infecció vírica, les cèl·lules esdevenien més resistents davant segones infeccions amb un altre virus. Aïllaren una proteïna d'aquestes cultures infectades, a la qual donaren el nom d'interferó. Al final de la dècada del 1960 i principi de la dècada del 1970, John David i Barry Bloom descobriren de manera independent el factor inhibidor de la migració dels macròfags (MIF) i una nova classe de substàncies secretades pels limfòcits. Dudley Dumonde encunyà el terme «limfocina» per a aquestes substàncies. Stanley Cohen, que el 1986 aconseguí el Premi Nobel de Fisiologia o Medicina pel seu descobriment dels factors de creixement NGF i EGF,[9][10] començà a estudiar a principis de la dècada del 1970 les funcions dels factors denominats limfocines juntament amb Takeshi Yoshida. Descobriren que aquestes substàncies pertanyen a un grup de substàncies missatgeres que són produïdes per molts tipus diferents de cèl·lules del sistema immunitari. El 1974 Stanley Cohen proposà el terme «citocina», que es consolidà amb el descobriment d'encara més substàncies d'aquest tipus. Des d'aleshores s'han descobert més de cent noves citocines, l'estructura i les funcions de les quals han estat investigades en detall.
Els principis de la immunologia moderna se situen al voltant del 1960. Rodney Porter aconseguí determinar l'estructura dels anticossos entre el 1959 i el 1961. Al mateix temps, Jean Dausset descobrí el complex d'histocompatibilitat principal humà, el denominat complex antigen leucocitari humà. A partir d'aquests anys, els fonaments de la immunologia cel·lular també foren clarificats per una sèrie de científics, comportant entre altres la diferenciació i descripció dels limfòcits B i T i el descobriment de les seves respectives funcions, tot per Jacques Miller. Així s'imposà la divisió de la defensa immunitària en una part humoral i una de cel·lular. Al llarg de les dècades següents, entre altres coses, es descobriren els diversos tipus d'anticòs i les seves funcions foren investigades. El 1975, Georges Köhler i César Milstein desenvoluparen la tècnica d'hibridomes per produir anticossos monoclonals. A causa de les amples conseqüències d'aquest descobriment per la recerca bàsica, així com pel diagnòstic i teràpia de malalties, el 1984 obtingueren el Premi Nobel de Fisiologia o Medicina.[11] Altres descobriments importants concernien la base genètica de la immunologia, com ara la descripció de la restricció per l'MHC per Rolf Zinkernagel (1974), la identificació dels gens de la immunoglobulina per Susumu Tonegawa (1985), i la dels gens dels receptors dels limfòcits T per Leroy Hood (1985).
L'objecte d'estudi principal de la immunologia és el sistema immunitari dels mamífers. Es tracta d'un complex sistema de molècules i de cèl·lules que es dediquen a reconèixer i desactivar les estructures alienes al cos. Les reaccions del sistema davant aquestes estructures són agrupades sota el nom de resposta immunitària. Els òrgans del cos responsables de la resposta immunitària són agrupats juntament amb els vasos limfàtics com a sistema limfàtic. El sistema cardiovascular també és de gran importància per la resposta immunitària.
La investigació immunològica concerneix principalment els aspectes mèdics i clínics de la resposta immunitària, com per exemple la seva disfunció en certs trastorns, així com el seu paper desitjat en el tractament de malalties. Un altre àmbit d'investigació important és l'ús de mètodes immunològics amb fins analítics i diagnòstics. La immunologia es pot dividir en diverses subdisciplines segons l'element estudiat, la metodologia utilitzada i el punt de vista que es considera.
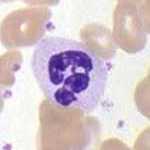
La immunologia cel·lular s'ocupa de les cèl·lules del sistema immunitari i de les reaccions que duen a terme. Entre les cèl·lules del sistema immunitari innat es troben els neutròfils, els fagòcits macròfags, o les cèl·lules NK, entre d'altres.[12] El sistema immunitari adaptatiu inclou els limfòcits B i els limfòcits T.[12] En contrast amb el sistema immunitari innat, el sistema immunitari adaptatiu pot presentar una resposta específica contra estructures alienes determinades, sempre que hi hagi tingut un contacte previ. En canvi, a la resposta immunitària innata no li cal aquest contacte previ.

La immunologia humoral s'ocupa dels processos del sistema immunitari basats en les proteïnes. El sistema del complement, que forma part de la resposta immunitària innata, n'és un exemple. En la part adaptativa del sistema immunitari, els anticossos són els responsables de la immunitat humoral. Un altre àmbit d'investigació important de la immunologia humoral són les citocines, proteïnes que s'encarreguen de la regulació del sistema immunitari i de la comunicació dels seus diferents components.[13]
La immunoquímica estudia l'estructura i les propietats dels antígens i anticossos, així com les bases químiques de la resposta immunitària. Un ús important de la immunoquímica són els processos diagnòstics i analítics basats en la reacció antigen-anticòs, com per exemple la immunohistoquímica. La immunogenètica s'ocupa de les bases genètiques del sistema immunitari, així com la variabilitat d'origen genètic de reaccions immunitàries com ara els mecanismes de producció d'anticossos, receptors dels limfòcits T i complexos presentadors d'antigen. La immunopatologia i la immunologia clínica tracten els aspectes mèdics de la immunologia.
Per motius històrics, la immunologia estudia principalment el sistema immunitari dels vertebrats, especialment el dels mamífers. Això es deu sobretot als orígens mèdics de la immunologia, i també ha fet que en els llibres de text i altres publicacions sobre immunologia només es presenti el sistema immunitari dels mamífers com a objecte d'estudi. Tanmateix, una branca de la investigació immunològica s'ocupa també del sistema immunitari dels animals invertebrats. En contrast amb el sistema immunitari dels vertebrats, aquest es caracteritza per la manca d'un sistema immunitari adaptatiu, i per tant pel predomini de respostes immunitàries inespecífiques, per mitjà de l'existència de mecanismes de defensa bioquímics en forma de pèptids antimicrobians així com estructures anatòmiques formades per la prevenció física de l'entrada de patògens i de substàncies alienes.[14] Els fagòcits tenen un paper central en la immunitat cel·lular dels animals invertebrats.
L'objectiu d'aquesta investigació és comprendre millor l'evolució del sistema immunitari i per consegüent les seves funcions. Mitjançant la comparació dels mecanismes de defensa de diferents animals es pot esbrinar quins dels seus components són comuns a tots ells, i com s'han desenvolupat. Per això, també es parla d'immunologia comparativa. Altres àmbits en què treballa la investigació de la immunologia dels invertebrats són l'ecotoxicologia, el control de plagues i la higiene. Dins de la investigació biomedicinal, la comprensió del sistema immunitari dels invertebrats permet utilitzar-los com a organisme model. Alguns components bioquímics del sistema immunitari dels invertebrats també poden tenir usos terapèutics o diagnòstics.
El sistema immunitari està implicat directament o indirecta en una multitud de malalties i altres trastorns clínicament importants. Aquests trastorns es poden distingir a partir dels mecanismes subjacents.
Durant les infeccions per part de bacteris, virus, protozous o fongs, en condicions normals es produeix una defensa immunitària contra l'entrada i l'expansió del patogen. Tanmateix, sota certes condicions la resposta immunitària pot fracassar o ser insuficient, de manera que la infecció s'estén i el sistema immunitari ja no és capaç de controlar-la. Això pot provocar que una infecció esdevingui crònica, cosa que significa que els patògens romanen a l'interior del cos i poden causar símptomes permanents o espontanis. Una greu infecció generalitzada, en què una infecció local s'ha estès arreu del cos per mitjà del reg sanguini, és denominada «sèpsia».[15] A causa de la reacció massiva del cos a aquesta condició, sovint és mortal.
Les denominades malalties autoimmunitàries són provocades per una reacció equivocada del sistema immunitari contra estructures pròpies del cos.[16] Aquestes reaccions poden comportar o bé la destrucció irreversible de teixits del cos o deteriorar el funcionament de molècules del cos com ara receptors o hormones. Alguns exemples de malalties autoimmunitàries són la diabetis mellitus de tipus 1, la tiroïditis de Hashimoto, la miastènia greu, la malaltia de Graves o la majoria de malalties reumàtiques inflamatòries, com ara l'artritis reumatoide.
En les al·lèrgies, o reaccions d'hipersensibilitat, es produeix una reacció excessiva del sistema immunitari davant certes estructures alienes. Un requisit per la formació d'una al·lèrgia és un primer contacte inofensiu amb la substància aliena, denominada al·lergogen. En aquest primer contacte es produeix la denominada sensibilització, és a dir, la formació d'una resposta immunitària específica. Cada nou contacte amb l'al·lergogen pot provocar una potent reacció del sistema immunitari. Les al·lèrgies més freqüents són al pol·len, al pèl dels animals, als aliments i als medicaments.[17] La celiaquia és una mescla d'al·lèrgia i de malaltia autoimmunitària, car es deu a una reacció encreuada del sistema immunitari amb el teixit de l'intestí prim, provocada pel gluten present en diverses espècies de cereals.
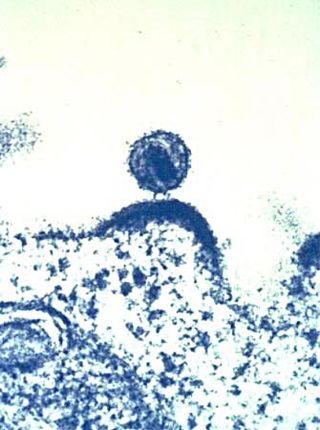
Entre les malalties que es caracteritzen per una resposta immunitària insuficient (immunoinsuficiència) es troba la síndrome d'immunodeficiència adquirida (SIDA), provocada per una infecció amb el virus de la immunodeficiència humana.[18] Les malalties innates d'immunodeficiència greus, en què estan afectades tant la immunitat humoral com la cel·lular, són agrupades sota el terme «immunodeficiència combinada greu». Els pacients amb una immunodeficiència innata o adquirida presenten una alta susceptibilitat a malalties infeccioses,[19] que amb una immunitat debilitada poden conduir fins i tot a la mort.
El sistema immunitari també té un paper important en el càncer. Els pacients amb immunodeficiència, causada per un tractament immunosupressor després d'un trasplantament d'òrgan o per una infecció amb VIH, pateixen certs tipus de càncer amb molta més freqüència. El sistema immunitari s'encarrega de controlar les cèl·lules deteriorades, desactivant-les abans que es pugui desenvolupar un tumor manifest. La part de la immunologia que estudia els processos de la creació, el desenvolupament i la lluita contra els tumors rep el nom d'immunologia del càncer, que ha trobat aplicacions pràctiques en la immunoteràpia contra el càncer.
Els processos immunològics tenen una importància capital en el trasplantament d'òrgans. Els òrgans trasplantats són reconeguts com a aliens pel sistema immunitari, causant la corresponent reacció immunitària. Sense tractament, aquesta resposta immunitària comporta el rebuig i finalment la pèrdua de funció de l'òrgan concernit. En altres casos, com ara els trasplantaments de medul·la òssia, es pot donar el fenomen invers, en el qual les cèl·lules immunitàries contingudes dins l'òrgan engeguen una resposta immunitària contra l'organisme receptor, la malaltia de l'empelt contra l'hoste. Per tant, el receptor de l'òrgan ha de rebre medicaments immunosupressors al llarg de tota la vida, medicaments que suprimeixen les respostes immunitàries a curt i llarg termini.
De manera semblant al cas del trasplantament d'òrgans o teixits aliens, el sistema immunitari està implicat en la ferma reacció del cos contra implants. Els implants es poden compondre, per exemple, de metalls o plàstics, i tenen molts usos diferents, com ara substituir temporalment o permanent ossos o vasos sanguinis, com a implants plàstics per la formació de certes estructures corporals, o com a pròtesis dentals, així com la substitució o el reforç d'òrgans del cos en el seu funcionament, com ara implants coclears o marcapassos. Com que estan compostos de materials aliens, els implants desencadenen mants processos immunitaris, particularment una reacció inflamatòria crònica. La compatibilitat immunològica d'aquests materials és doncs un aspecte important de la seva biocompatibilitat i contribueix de manera decisiva al funcionament durable de l'implant.

El conjunt d'usos terapèutics que reposen sobre els coneixements i els principis de la immunologia s'agrupen sota el terme «immunomodulació». Això concerneix totes les teràpies que apunten a influir sobre certs processos o components del sistema immunitari. Per exemple, és molt estès l'ús de vacunes, en què s'inocula un antigen per tal que el sistema immunitari pugui desenvolupar una resposta contra aquest antigen.[12] Les vacunes tenen un paper molt important en la prevenció de les malalties infeccioses. En aquest sentit, s'han obtingut els primers èxits a partir de la creació de vacunes contra virus associats al càncer, com ara el papil·lomavirus humà.[20] La sensibilització del sistema immunitari a estructures específiques dels tumors en malalts de càncer segueix el mateix principi que les vacunes.
Un altre àmbit de la immunomodulació és conegut com a hiposensibilització, o immunoteràpia específica. El seu objectiu és aconseguir una certa immunotolerància del cos davant certs antígens. Això significa una reducció de la reacció immunitària contra aquests antígens. Es fa per mitjà de la inoculació repetida dels antígens concernits, amb una dosi lleugerament superior cada vegada. La hiposensibilització té importància terapèutica en el cas de les malalties causades per al·lèrgies,[21] i se n'està estudiant l'ús en el cas de les malalties autoimmunitàries.
El terme «immunosupressió» agrupa una sèrie de teràpies que aspiren a suprimir processos immunitaris no desitjats. Això és possible per l'ús de medicaments que interfereixen en diversos processos de la resposta immunitària. Aquests medicaments immunosupressors són utilitzats principalment en la prevenció del refús de trasplantament d'òrgans, però també es fan servir per tractar malalties autoimmunitàries.
També és possible el procés contrari, la immunoestimulació, que estimula el sistema immunitari i reforça la resposta immunitària. Per això, es poden utilitzar amb fins terapèutiques determinades proteïnes pròpies del cos, que intervenen en la regulació del sistema immunitari. Les citocines són les que es fan servir més sovint. Aquestes teràpies són d'especial rellevància en el tractament de les infeccions víriques.
Un altre ús important dels principis immunològics per al tractament de malalties són els anticossos terapèutics. Es tracta d'anticossos, o globulines del sistema immunitari que són produïts per processos biotecnològics i que es dirigeixen contra determinades estructures del cos. Aquestes estructures, que són les que tenen un paper en la malaltia en qüestió, són destruïdes o neutralitzades. Sovint, les estructures objectius presenten certes proteïnes a la superfície cel·lular, com ara proteïnes de transport, proteïnes de senyalització o receptors, però també proteïnes lliures del sèrum com ara citocines o hormones. Els anticossos terapèutics són utilitzats, entre altres coses, per al tractament de diversos càncers, de malalties autoimmunitàries, d'al·lèrgies o per a la prevenció del refús de trasplantament.
Els anticossos també són utilitzats com a antisèrums contra determinades substàncies tòxiques. Per obtenir aquests antisèrums, s'injecta una quantitat petita de la toxina corresponent a un animal, sovint un cavall. Aleshores, l'animal desenvolupa anticossos específics a la seva sang, que neutralitzen els efectes tòxics. Una vegada obtinguts i purificats els anticossos a partir de la sang d'aquests animals, poden ser utilitzats com a tractament agut d'enverinaments, com per exemple en picades de serp. Els antisèrums obtinguts d'aquesta manera també serveixen per a la immunització passiva contra determinades malalties infeccioses, quan no es disposa de prou temps per una immunització activa per vacunació o no existeix una vacuna apropiada. Tanmateix, l'ús repetit d'aquests antisèrums també acaba provocant una resposta immunitària. Per això, generalment se sol preferir una immunització activa, si és possible. Com a mesura d'emergència, es recorre a la immunització passiva quan se sospita una infecció amb el virus de la ràbia.

Els mètodes de laboratori immunològics tenen un paper important en el diagnòstic de malalties i en la recerca fonamental biomèdica. Els immunoassajos són els procediments que mesuren les característiques qualitatives o quantitatives de certes substàncies en un líquid biològic per mitjà de la reacció dels anticossos als seus antígens. Els immunoassajos s'utilitzen per identificar patògens, així com per analitzar els líquids corporals a la recerca de proteïnes pròpies del cos, que en certes malalties fan la funció de biomarcadors específics. Per certes malalties, particularment les al·lèrgies, malalties autoimmunitàries i infeccions, la recerca d'anticossos específics és possible com a part del diagnòstic i del control del curs de la malaltia. També són utilitzats com a proves d'embaràs. Altres usos en la medicina són la identificació de toxines i drogues, la supervisió de principis actius dins el cos (monitoratge de fàrmacs), o la detecció de substàncies dopants en la medicina esportiva. A part dels diagnòstics mèdics, els immunoassajos també s'utilitzen per a anàlisis ambientals, alimentàries o agràries, com per exemple per detectar toxines ambientals, o al·lergògens als aliments i organismes modificats genèticament.
En els trasplantaments d'òrgans, en els empelts de medul·la òssia i en les transfusions sanguínies, la caracterització geneticomolecular de determinats marcadors d'histocompatibilitat ofereix una major possibilitat d'assegurar compatibilitat entre el donant i el receptor. La immunohistoquímica utilitza anticossos per marcar estructures específiques en preparats microscòpics, sent un ús important dels principis immunològics en el diagnòstic patològic. En la citometria de flux i la separació cel·lular magnètica (MACS, de l'anglès magnetic-activated cell sorting) s'utilitzen anticossos per revelar certes estructures superficials de les cèl·lules, desfent així la mescla de cèl·lules o permetent-ne l'anàlisi de la composició. Pel diagnòstic clínic, és d'especial rellevància en l'hematologia, on s'utilitza per analitzar la distribució cel·lular de la sang.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.