
Taula periòdica
taula que classifica, organitza i distribueix els elements químics segons les seves propietats i característiques / From Wikipedia, the free encyclopedia
La taula periòdica, taula de Mendeléiev o sistema periòdic dels elements és una taula que ordena els elements químics de menor a major nombre atòmic tot posant de manifest la periodicitat de les seves propietats químiques i físiques. S'hi reflecteix la llei periòdica formulada el 1869[1] pel químic rus Dmitri Mendeléiev de la Universitat Imperial de Sant Petersburg, això és, la semblança dels elements químics cada cert nombre de nombres atòmics.
Els químics consideren que la taula periòdica constitueix la base i l'eix vertebrador dels seus coneixements i ha esdevingut amb els anys un clar element identificador, un símbol de la química.[2]
L'estructura actual de la taula periòdica de la Unió Internacional de Química Pura i Aplicada (IUPAC) consta de:

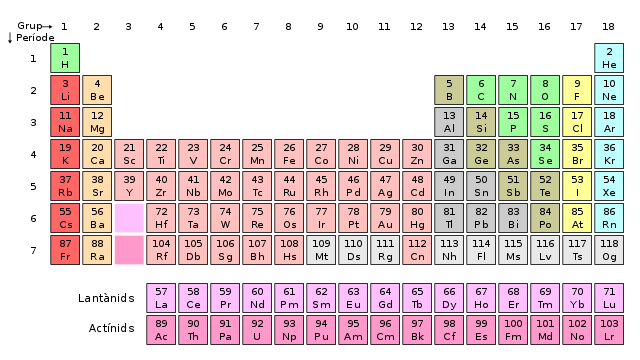
- 118 caselles, una per a cada element químic. La informació mínima de cada casella és el símbol químic de l'element que l'ocupa i el seu nombre atòmic
. Sovint també hi figura el nom de l'element i la massa atòmica relativa. Addicionalment s'hi posen dades de propietats atòmiques (radi atòmic, energia de ionització…), físiques (punts de fusió i d'ebullició, densitat…) i químiques (nombre d'oxidació, electrons de valència…).
- 7 períodes (fileres) de longituds creixents numerats de l'1 al 7 i començant per la part superior. El 1r període té només dos elements; el 2n i el 3r períodes vuit elements cadascun; el 4t i el 5è devuit cadascun, i els 6è i 7è en tenen cada un trenta-dos. Si se sintetitzen nous elements químics ocuparan el període 8è, ara buit.[3]
- 18 grups o famílies (columnes), amb propietats físiques i químiques molt similars. S'anomenen de l'1 al 18 començant per l'esquerra. Alguns grups tenen noms: el grup 1 és el dels alcalins, el 2 dels alcalinoterris, el 16 el dels calcògens, el 17 el grup dels halògens i el 18 el grup dels gasos nobles.[3]
- 4 blocs segons les seves configuracions electròniques: el bloc s els formen les dues columnes de l'esquerra (alcalins i alcalinoterris) a més de l'hidrogen i l'heli; bloc p el constitueixen els grups (columnes) del 13 al 18, ubicats a la dreta, excepte l'heli; bloc d ocupa el centre amb els grups del 3 al 12; i el bloc f amb els elements anomenats lantanoides i els actinoides, col·locats en dues files a la part inferior de la taula.[3] L'element 121 obrirà el bloc g.
Gràcies a la distribució de Mendeléiev dels elements químics coneguts a mitjans del segle xix, pogué predir l'existència d'elements químics encara no descoberts (gal·li, germani…) i les propietats físiques (punt de fusió, densitat, color…) i químiques (massa atòmica, compostos, reactivitat química amb l'aire, l'aigua, els àcids, les bases…) que tindrien. Foren aïllats pocs anys després (el gal·li el 1875, el germani el 1886…) i confirmaren les prediccions fetes pel químic rus, la qual cosa donà un fort suport a la seva taula periòdica.
Posteriorment, la taula periòdica original s'hagué de modificar per incloure grups d'elements que no havien estat predits (gasos nobles, lantanoides) o que se sintetitzaren car no existeixen a la natura (actinoides), donant lloc a la taula periòdica actual.
| Metalls alcalins | Alcalinoterris | Lantanoides | Actinoides | Metalls de transició |
| No-metalls gasos nobles | No-metalls halògens | Altres no-metalls | Semimetalls | Metalls del bloc p i del grup 12 |
| Grup | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||
| Període | ||||||||||||||||||||
| 1 | 1 H |
2 He | ||||||||||||||||||
| 2 | 3 Li |
4 Be |
5 B |
6 C |
7 N |
8 O |
9 F |
10 Ne | ||||||||||||
| 3 | 11 Na |
12 Mg |
13 Al |
14 Si |
15 P |
16 S |
17 Cl |
18 Ar | ||||||||||||
| 4 | 19 K |
20 Ca |
21 Sc |
22 Ti |
23 V |
24 Cr |
25 Mn |
26 Fe |
27 Co |
28 Ni |
29 Cu |
30 Zn |
31 Ga |
32 Ge |
33 As |
34 Se |
35 Br |
36 Kr | ||
| 5 | 37 Rb |
38 Sr |
39 Y |
40 Zr |
41 Nb |
42 Mo |
43 Tc |
44 Ru |
45 Rh |
46 Pd |
47 Ag |
48 Cd |
49 In |
50 Sn |
51 Sb |
52 Te |
53 I |
54 Xe | ||
| 6 | 55 Cs |
56 Ba |
* |
72 Hf |
73 Ta |
74 W |
75 Re |
76 Os |
77 Ir |
78 Pt |
79 Au |
80 Hg |
81 Tl |
82 Pb |
83 Bi |
84 Po |
85 At |
86 Rn | ||
| 7 | 87 Fr |
88 Ra |
** |
104 Rf |
105 Db |
106 Sg |
107 Bh |
108 Hs |
109 Mt |
110 Ds |
111 Rg |
112 Cn |
113 Nh |
114 Fl |
115 Mc |
116 Lv |
117 Ts |
118 Og | ||
| * Lantanoides | 57 La |
58 Ce |
59 Pr |
60 Nd |
61 Pm |
62 Sm |
63 Eu |
64 Gd |
65 Tb |
66 Dy |
67 Ho |
68 Er |
69 Tm |
70 Yb |
71 Lu | |||||
| ** Actinoides | 89 Ac |
90 Th |
91 Pa |
92 U |
93 Np |
94 Pu |
95 Am |
96 Cm |
97 Bk |
98 Cf |
99 Es |
100 Fm |
101 Md |
102 No |
103 Lr | |||||
Codificació de colors dels nombres atòmics dels elements:
- En blau són líquids a temperatura i pressió estàndard (TPE);
- En verd, són gasos a TPE;
- En negre, són sòlids a TPE;
- En vermell, són sintètics (tots són sòlids a TPE);
