
Estat d'oxidació
From Wikipedia, the free encyclopedia
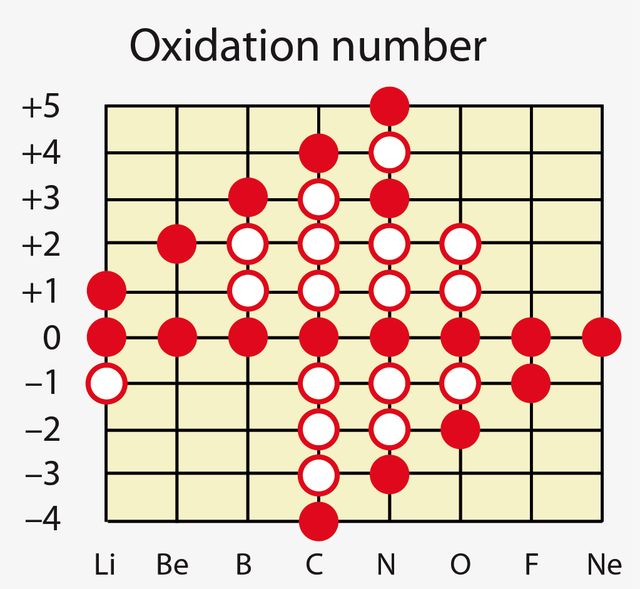
L'estat d'oxidació o nombre d'oxidació és la càrrega elèctrica, en unitats de càrrega elèctrica elemental, d'un àtom en un compost químic establerta a partir de l'assignació de més o menys electrons que els de l'àtom neutre segons la seva electronegativitat i la dels àtoms veïns amb els quals està enllaçat. Generalment, els valors són nombres sencers, positius i negatius entre –4 i +8, si bé són possibles valors fraccionaris. L'estat d'oxidació és una aproximació conceptual, útil per exemple quan es produïxen processos d'oxidació i reducció (reaccions redox).
Etimològicament, «nombre d'oxidació» prové del terme en desús «nombre de Stock» (nombre d'oxidació d'un àtom central; la càrrega que portaria si s'eliminessin tots els lligands juntament amb els parells d'electrons que estaven compartits amb l'àtom central) i del també obsolet terme «nombre d'Ewens–Bassett» (càrrega d'ions).[1]
Els protons d'un àtom tenen càrrega elèctrica positiva 
