
যোজ্যতা ইলেকট্রন
From Wikipedia, the free encyclopedia
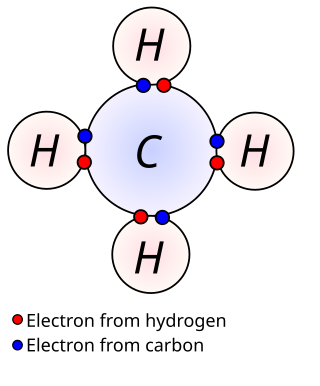
রসায়নে যোজনী ইলেকট্রন হল পরমাণুর সাথে সম্পর্কিত ইলেকট্রন যা রাসায়নিক বন্ধন গঠনে অংশগ্রহণ করে। একক সমযোজী বন্ধনে, বন্ধনে আবদ্ধ উভয় পরমাণুর একটি করে যোজনী ইলেকট্রন ভাগাভাগি করার মাধ্যমে সর্বমোট একজোড়া ইলেকট্রন ভাগাভাগি করে বন্ধন গঠন করে। বস্তুর রাসায়নিক ধর্ম এবং এটি অন্য কিছুর সাথে বন্ধন গঠন করে কিনা — তা যাচাইয়ের মাধ্যমে যোজনী ইলেকট্রন নির্ণয় করা যায়। মূল গ্রুপভুক্ত মৌলের ক্ষেত্রে সর্ববহিঃস্থ স্তরে বিদ্যমান ইলেকট্রন সংখ্যাই ঐ মৌলের যোজনী ইলেকট্রন বা যোজক ইলেকট্রন। ট্রানজিশন মৌলের ক্ষেত্রে যোজনী ইলেকট্রন নির্ণয়ে অভ্যন্তরীণ কক্ষের ক্ষেত্রেও আলোকপাত করতে হয়।
বদ্ধ শেলবিশিষ্ট একটি পরমাণুর যোজনী ইলেকট্রন (s2p6 ইলেকট্রন বিন্যাস অনুযায়ী) হয় নোবেল গ্যাসের ন্যায়। বদ্ধ শেলের জন্য এক বা দুই ততোধিক যোজনী ইলেকট্রন প্রয়োজন, কারণঃ
- এর নিম্ন শক্তি প্রয়োজন (ল্যাটিস এনথ্যালপির তুলনায়), অতিরিক্ত যোজনী ইলেকট্রন সরিয়ে ধনাত্মক আয়ন গঠন করার জন্য
- হারানো যোজনী ইলেকট্রন অর্জনের জন্য (এবং তদুপরি ঋণাত্মক আয়ন গঠনের জন্য) বা যোজনী ইলেকট্রন ভাগাভাগি করার জন্য (এবং তদুপরি সমযোজী বন্ধন গঠনের জন্য)
অভ্যন্তরীণ কক্ষের ইলেকট্রনের ন্যায় যোজনী ইলেকট্রনেরও ফোটন হিসেবে শক্তি শোষণ বা নির্গমন করতে পারে। শক্তি শোষণ একটি ইলেকট্রনকে পরবর্তী কক্ষে লাফিয়ে যেতে দেয়; একে পারমাণবিক উত্তেজনা বলা হয়। অথবা ইলেকট্রন সহযোগী পরমাণুর যোজনী শেল থেকে বের হয়েও আসতে পারে। ফলে ধনাত্মক আয়ন গঠিত হয়। যখন কোনো ইলেকট্রন শক্তি হারায় (ফলে একটি ফোটন নির্গত হয়), তখন এটি অভ্যন্তরীণ কক্ষে গমন করে।
যোজনী শক্তিস্তর [প্রধান কোয়ান্টাম সংখ্যানুযায়ী গঠিত হয় (n = ১, ২, ৩, ৪, ৫ ...) বা বর্ণানুক্রমিকভাবে [রঞ্জন রশ্মি লিপি] অনুযায়ী (K, L, M, …) হিসেবে প্রকাশ করা হয়।