Loading AI tools
উইকিপিডিয়া থেকে, বিনামূল্যে একটি বিশ্বকোষ
অভিস্রবণিক চাপ হলো ন্যূনতম চাপ যাতে অর্ধভেদ্য পর্দা দ্বারা এর দ্রাবকের অভ্যন্তরীণ প্রবাহ রোধ করার জন্য একটি দ্রবণ যোগ করা হয় । অন্যভাবে বলা যায় বিশুদ্ধ দ্রাবক গ্রহণ করার প্রবণতা পরিমাপ করাই হলো অভিস্রবণ । সম্ভাব্য অভিস্রবণিক চাপ হলো সর্বাধিক অভিস্রবণিক চাপ যা কোনো দ্রবণে বিকাশ করতে পারে যদি এটি তার অর্ধভেদ্য পর্দা দ্বারা শুদ্ধ দ্রাবক থেকে পৃথক করা হয়।
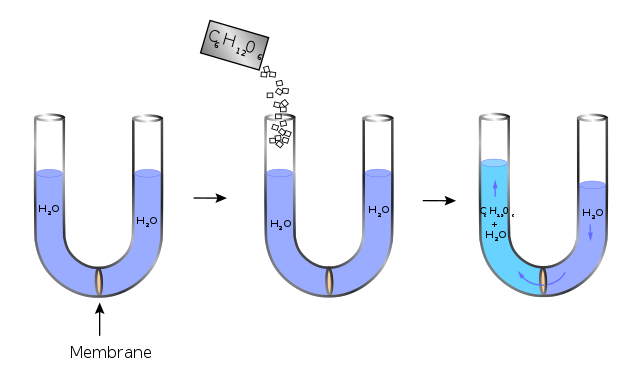
অভিস্রবণ ঘটে যখন দুইটি ভিন্ন ঘনত্ব ধারণকারী দ্রবীভূত পদার্থ একটি অর্ধভেদ্য ঝিল্লি দ্বারা বিভক্ত করা হয়। দ্রাবক অণুগুলি উচ্চ ঘনত্বের স্থান থেকে নিম্ন ঘনত্বের স্থানে ঝিল্লির মধ্য দিয়ে যায়। ভারসাম্য অর্জন না হওয়া পর্যন্ত দ্রাবক অণুগুলির স্থানান্তর চলতে থাকবে।

জ্যাকোবাস ভ্যান্ট হফ নিচের সমীকরণে প্রকাশিত অভিস্রবণিক চাপ এবং দ্রাবক ঘনত্বের মধ্যে একটি পরিমাণগত সম্পর্ক খুঁজে পেয়েছিল:
যেখানে অভিস্রবণিক চাপ, i মাত্রাবিহীন ভ্যান্ট হফ সূচক, c হল দ্রবণের ঘনত্ব, R আদর্শ গ্যাসের ধ্রুবক এবং T হল ক্যালভিনের তাপমাত্রা। এই সূত্রটি প্রয়োগ করা হয় যখন দ্রবণীয় ঘনত্ব যথেষ্ট পরিমাণে কম থাকে যে দ্রবণটিকে আদর্শ দ্রবণ হিসাবে বিবেচনা করা যেতে পারে। ঘনত্বের আনুপাতিকতার অর্থ অভিস্রবণিক চাপ একটি সংঘবদ্ধ বৈশিষ্ট্য । ফর্মের আদর্শ গ্যাস আইনের সাথে এই সূত্রের মিলটি নোট করুন যেখানে n , V আয়তনে গ্যাস অণুর মোট সংখ্যা, এবং n/ V গ্যাস অণুর মোলার ঘনত্ব। হার্মন নরথ্রপ মোর্স এবং ফ্রেজার দেখিয়েছেন যে সমীকরণ প্রয়োগ করা হয় আরো ঘনীভূত দ্রবণের ঘনত্বতে যদি তার একক মোলার না হয়ে মোলাল হত ; সুতরাং যখন মোলালিটি ব্যবহৃত হয় তখন এই সমীকরণটিকে মোর্স সমীকরণ বলা হয়।
যেখানে হলো আদর্শ চাপ এবং A একটি গবেষণামূলক পরামিতি। A পরামিতির মান (এবং উচ্চতর অর্ডার অনুমান থেকে পরামিতি ) নিরূপণ করা যেতে পারে পিটজার পরামিতি ব্যবহার করে । গবেষণামূলক পরামিতি ব্যবহার করা হয়, দ্রবণের আয়নের সংখ্যার আচরণ এবং অ-আয়নের দ্রাবকে যা থার্মোডাইনামিক অর্থে আদর্শ দ্রবণ নয় ।
পেফার সেলটি অভিস্রবণিক চাপ পরিমাপের জন্য তৈরি করা হয়েছিল।

অভিস্রবণিক চাপের মান আণবিক ওজন নির্ধারণের জন্য ব্যবহার করা যেতে পারে।
অভিস্রবণিক চাপ কোষকে প্রভাবিত করে এমন একটি গুরুত্বপূর্ণ উপাদান। ওসমোরেগুলেশন হ'ল অভিস্রবণিক চাপের ভারসাম্য বজায় রাখার জন্য একটি জীবের হোমোস্টেসিস পদ্ধতি।
যখন একটি জৈবিক কোষ হাইপোটোনিক পরিবেশে থাকে, তখন কোষের ভেতরে পানি জমে, কোষের ঝিল্লি পেরিয়ে জল কোষে প্রবাহিত হয়, যার ফলে এটি প্রসারিত হয়। উদ্ভিদ কোষগুলিতে, কোষ প্রাচীরটির প্রসারণকে সীমাবদ্ধ করে, ফলস্বরূপ কোষের প্রাচীরের উপর চাপ ঘটে যার নাম টার্গোর চাপ । টার্গোর চাপ ভেষজ উদ্ভিদগুলিকে সোজা হয়ে দাঁড়াতে দেয়। উদ্ভিদগুলি তাদের স্টোমাটার রন্ধ্রগুলিকে কীভাবে নিয়ন্ত্রণ করে তাও নির্ধারণ করে । পশুর কোষগুলিতে অত্যধিক অভিস্রবণিক চাপের ফলে সাইটোলাইসিস হতে পারে।
অভিস্রবণিক চাপ হলো ছাঁকনির ভিত্তি (" বিপরীত অভিস্রবণ "), এটি একটি সাধারণ প্রক্রিয়া যা জল পরিশোধন করতে ব্যবহৃত হয়। যে জলটি শুদ্ধ করা হবে সেটি একটি চেম্বারে স্থাপন করা হয় এবং জল দ্বারা প্রবাহিত অভিস্রবণিক চাপের চেয়ে বেশি পরিমাণে চাপের মধ্যে রাখা হয় এবং এতে দ্রব গুলো দ্রবীভূত থাকে। চেম্বারের অংশটি খোলে একটি পৃথকভাবে প্রবেশযোগ্য ঝিল্লিতে যা জলের অণুগুলির মধ্য দিয়ে যায়, তবে দ্রব কণা নয়। সমুদ্রের জলের অভিস্রবণিক চাপ প্রায় 27 atm । বিপরীত অভিস্রবণ সমুদ্রের নুনের জল থেকে বিশুদ্ধ জলকে বিচ্ছিন্ন করে।
বিবেচনা করুন সিস্টেমটি এর কোনো এক বিন্দুতে তার ভারসাম্য অবস্থায় পৌঁছেছে। এর শর্তটি হ'ল দ্রাবকের রাসায়নিক বিভব(যেহেতু কেবল এটি ভারসাম্যের দিকে প্রবাহিত হয় ) ঝিল্লির উভয় ক্ষেত্রে সমান। খাঁটি দ্রাবকযুক্ত অংশে একটি রাসায়নিক বিভব রয়েছে যা হলো , যেখানে হলো চাপ। অন্যদিকে, দ্রব যুক্ত অংশে দ্রাবকের রাসায়নিক বিভব দ্রাবকের মোল ভগ্নাংশের উপর নির্ভর করে, । এছাড়াও, এই অংশটি একটি আলাদা চাপ ধরে নিতে পারে যা হলো, । সুতরাং আমরা দ্রাবকের রাসায়নিক বিভব লিখতে পারি এভাবে । যদি আমরা লিখি , রাসায়নিক বিভবের ভারসাম্য হবে:
এখানে দুটি অংশের চাপের মধ্যে পার্থক্য কে দ্রাবকের মাধ্যমে পরিবেশন করার অভিস্রবণিক চাপ হিসাবে সংজ্ঞায়িত করা হয়। চাপটি দ্রাবক সংযোজনের রাসায়নিক বিভবকে হ্রাশ করে (একটি বিশৃঙ্খলা-মাত্রার প্রভাব )। সুতরাং, রাসায়নিক বিভবের ক্ষতি পূরণের জন্ন্য দ্রবণটির চাপকে বাড়াতে হবে।
এটি করার জন্য ,অভিস্রবণিক চাপটি, আমরা সুস্থিতি বিবেচনা করি দ্রবযুক্ত দ্রবণ এবং বিশুদ্ধ পানি্র মধ্যে ।
আমরা বাম দিকে লিখতে পারি
যেখানে দ্রাবকের সক্রিয়ক সহগ । উপাদানগুলো দ্রাবকের সক্রিয়ক হিসাবেও পরিচিত, যা পানির জন্য এবং পানির সক্রিয়ক । চাপ সংযোজন শক্তির অভিব্যক্তি এক্সপেনশনের মাধ্যমে প্রকাশ করা হয়:
যেখানে মোলার আয়তন (m³ / mol)। সম্পূর্ণ সিস্টেমের ভাবটি রাসায়নিক বিভব সমীকরণের মধ্যে প্রকাশিত এবং পুনরায় সাজালে হবে :
যদি তরলটি সংকোচনীয় হয় তবে মোলার আয়তন স্থির থাকে,, এবং অবিচ্ছেদ্য হয় । সুতরাং, আমরা পাই,
সক্রিয়ক সহগের কাজ ঘনত্ব এবং তাপমাত্রার , তবে হালকা মিশ্রণের ক্ষেত্রে এটি প্রায়শই 1.0 এর খুব কাছাকাছি থাকে, তাই
দ্রবের মোল ভগ্নাংশ,, হয় , তাই কে প্রতিস্থাপন করা যেতে পারে হিসাবে যখন ছোট, কাছাকাছি হতে পারে ।
মোল ভগ্নাংশ হয় । যখন ছোট, এটি দ্বারা প্রায় অনুমান করা যেতে পারে, এছাড়াও, মোলার আয়তন,, মোল প্রতি আয়তন হিসাবে লেখা যেতে পারে, । এগুলির সংমিশ্রণটি নিম্নলিখিতভাবে হয়।
লবণের জলীয় দ্রবণগুলির জন্য, আয়নীকরণকে অবশ্যই বিবেচনায় নেওয়া উচিত। উদাহরণস্বরূপ,1 মোল NaCl আয়নিত হয়ে 2 মলে পরিণত হয়।
অনেক বড় সংখ্যার আণবিক ভরসম্পন্ন কোন পদার্থের, যেটি অনুদবায়ী, অসংযোজিত ও তড়িৎ-অবিশ্লেষ্য, তার আণবিক ভর নির্ণয় করতে অভিস্রবণ চাপ পদ্ধতি ব্যবহার করা হয়ে থাকে।
ধরা যাক, M g/mol আণবিক ভরযুক্ত কোনো দ্রাব V লিটার দ্রবণে W গ্রাম দ্রবীভূত আছে।
তাই, মোল সংখ্যা হল (W/M) মোল, আর গাঢ়ত্ব (C) হল (W/MV) mol/L।
এখন, T নির্দিষ্ট পরাম উষ্ণতায় দ্রবণটির অভিস্রবণ চাপ হলে ভ্যান্ট হফ সমীকরণ অনুসারে,
এখান থেকে M এর মান সহজে নির্ণয় সম্ভব।
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.