Перыяд перыядычнай сістэмы
шэраг, радок перыядычнай сістэмы From Wikipedia, the free encyclopedia
Перыяд — радок перыядычнай сістэмы хімічных элементаў. Інакш кажучы, перыяд — гэта паслядоўнасць хімічных элементаў, упарадкаваных па ўзрастанню зараду ядра і запаўненню электронамі вонкавай электроннай абалонкі.
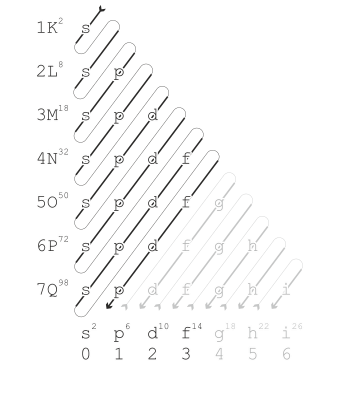
Перыядычная сістэма мае сем перыядаў. Першы перыяд, у якім толькі 2 элементы, а таксама другі і трэці, у якіх па 8 элементаў, называюцца малымі. Астатнія перыяды, у якіх 18 і больш элементаў, — вялікімі. Сёмы перыяд не завершаны. Нумар перыяда, да якога адносіцца хімічны элемент, вызначаецца колькасцю яго электронных абалонак (энергетычных узроўняў).
Кожны перыяд (за выключэннем першага) пачынаецца тыповым металам (Li, Nа, К, Rb, Cs, Fr) і заканчваецца інертным газам (Не, Ne, Ar, Kr, Хе, Rn), перад якім ідзе тыповы неметал.
У першым перыядзе, акрамя гелію, ёсць толькі адзін элемент — вадарод, які спалучае ўласцівасці, тыповыя як для металаў, так і (у большай ступені) для неметалаў. У гэтых элементаў запаўняецца электронамі 1s-падабалонка.
У элементаў другога і трэцяга перыяда адбываецца паслядоўнае запаўненне s- і р-падабалонак. Для элементаў малых перыядаў характэрна дастаткова быстрае павелічэнне электраадмоўнасці з ростам зарадаў ядзер, аслабленне металічных уласцівасцей і ўзмацненне неметалічных.
Чацвёрты і пяты перыяды ўтрымліваюць па дзесяць пераходных d-элементаў (ад скандыю да цынку і ад ітрыю да кадмію), у якіх пасля запаўнення электронамі вонкавай s-падабалонкі запаўняецца, згодна з правілам Клячкоўскага, d-падабалонка папярэдняга энергетычнага ўзроўню.
1s
2s 2p
3s 3p
4s 3d 4p
5s 4d 5p
6s 4f 5d 6p
7s 5f 6d 7p
6f 7d 7f
...
У шостым і сёмым перыядзе адбываецца насычэнне 4f- і 5f-падабалонак, таму яны ўтрымліваюць яшчэ на 14 элементаў больш у параўнанні з 4-м і 5-м перыядамі (лантаноіды ў шостым і актыноіды ў сёмым перыядзе).
У выніку адрознення перыядаў па даўжыні і іншых прыкметах існуюць розныя спосабы іх адноснага размяшчэння ў перыядычнай сістэме. У кароткаперыядным варыянце малыя перыяды маюць па аднаму раду элементаў, вялікія — па два рады. У доўгаперыядным варыянце ўсе перыяды складаюцца з аднаго рада. Рады лантаноідаў і актыноідаў звычайна выносяць асобна ў ніз табліцы.
| Колькасць элементаў | 2 ці 8 | 18 і больш |
| Колькасць радоў | 1 | 2 |
| Размеркаванне электронаў | запаўняюцца толькі s- і р-падабалонкі | запаўняюцца таксама перадвонкавыя d-падабалонкі і перадперадвонкавыя f-падабалонкі |
| Змяненне ўласцівасцей элементаў | металічныя ўласцівасці хутка памяншаюцца | павольны пераход ад металічных уласцівасцей да неметалічных |
Элементы аднаго перыяда маюць блізкія значэнні атамных мас, але розныя фізічныя і хімічныя ўласцівасці, у адрозненне ад элементаў аднае групы. З нарастанне зараду ядра ў элементаў аднаго перыяда памяншаецца радыус і расце колькасць валентных электронаў, ад чаго металічныя ўласцівасці элементаў слабеюць, а неметалічныя мацнеюць, г.зн. аслабляюцца аднаўленчыя і ўзмацняюцца акісляльныя ўласцівасці ўтвораных імі рэчываў.
Гл. таксама
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
