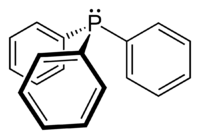
ثلاثي فينيل الفوسفين (أو ثلاثي فينيل الفوسفان حسب IUPAC) هو مركب عضوي فوسفوري له الصيغة P(C6H5)3، والتي ترمز اختصاراً PPh3. يوجد المركب على شكل بلورات عديمة اللون في الشروط العادية.
| ثلاثي فينيل الفوسفين | |
|---|---|
| الاسم النظامي (IUPAC) | |
Triphenylphosphane | |
| المعرفات | |
| رقم CAS | 603-35-0 |
| بوب كيم | 11776 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| الخواص | |
| الصيغة الجزيئية | C18H15P |
| الكتلة المولية | 262.29 غ/مول |
| المظهر | بلورات عديمة اللون |
| الكثافة | 1.1 غ/سم3 |
| نقطة الانصهار | 80 °س |
| نقطة الغليان | 377 °س |
| الذوبانية في الماء | لا ينحل في الماء |
| الذوبانية | ينحل في الإيثانول وباقي المذيبات |
| المخاطر | |
| ترميز المخاطر | |
| توصيف المخاطر | |
| تحذيرات وقائية | |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
الخصائص
- لا ينحل ثلاثي فينيل الفوسفين في الماء، لكنه ينحل في المذيبات العضوية المختلفة.
- يكون لثلاثي فينيل الفوسفين بنية هرمية، لها ترتيب يشبه شفرات المروحة. تمثل هذه البنية الجاسئة (غير المرنة) لثلاثي فينيل الفوسفين السبب الرئيسي في كون مشتقات المركب سهلة التبلور.
التحضير
يحضر ثلاثي فينيل الفوسفين مخبرياً من تفاعل ثلاثي كلوريد الفوسفور مع بروميد فينيل المغنسيوم [2] أو فينيل الليثيوم. أما على مستوى صناعي فيحضر PPh3 من تفاعل ثلاثي كلوريد الفوسفور مع كلور البنزين والصوديوم.[3]
التفاعلات
يخضع ثلاثي فينيل الفوسفين إلى تفاعل أكسدة بسبب أكسجين الهواء المحيط إلى أكسيد ثلاثي فينيل الفوسفين:
- 2 PPh3 + O2 → 2 OPPh3
ويمكن فصل هذه الإشابة عن مركب ثلاثي فينيل الفسفين بإجراء إعادة تبلور بالإيثانول الساخن أو إيزوبروبانول.[4] وذلك لأن أكسيد ثلاثي فينيل الفوسفين أكثر قطبية من PPh3 فهو أكثر انحلالية في المحلات القطبية.
تستخدم خاصية سهولة أكسدة ثلاثي فينيل الفوسفين في عملية نزع الأكسجين من فوق الأكاسيد العضوية:
- PPh3 + RO2H → OPPh3 + ROH (R = ألكيل)
يقوم ثلاثي فينيل الفوسفين بسحب الكبريت من مركبات عديد الكبريتيد Polysulfide وذلك لأن مركبات الكبريت البسيطة مثل الثيول وثيو الإيثر عبارة عن مركبات غير فعالة، وذلك لتشكل مركب Ph3PS. يمكن استخدام هذه الخاصية من أجل فحص الكبريت الحر S0 للعينات. وبشكل مشابه يتفاعل PPh3 مع السيلينيوم. يمكن لثلاثي فينيل الفوسفين أن يشكل ناتج ضم مع التيلوريوم، إلا أن ناتج الضم يكون غالباً على شكل Ph3P)2Te) أكثر من PPh3Te المنشود.[5]
يستعمل ثلاثي فينيل الفوسفين بشكل واسع في الاصطناع العضوي وذلك نظرا لخواصه الشغوفة بالنواة والاختزالية.[6]
المعقدات
يستطيع ثلاثي فينيل الفوسفين أن يشكل معقدات تساندية مع أغلب الفلزات الانتقالية خاصة مع العناصر في المجموعات من السابعة إلى العاشرة.[7]
طالع أيضاً
المراجع
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.