
قطب الهيدروجين المعياري
من ويكيبيديا، الموسوعة encyclopedia
قطب قياسي للهيدروجين في كيمياء كهربية (بالإنجليزية: standard hydrogen electrode) هو قطب أكسدة-اختزال يشكل أساس قائمة جهد القطب القياسي. وقد عين الجهد المطلق للقطب بأنه مساويا 4.44 ± 0.02 Vفولت عند 25 درجة مئوية، ولكن بغرض تشكيل أساسا لمقارنة تفاعلات أقطاب أخرى فقد اصطلح على جعل القطب القياسي للهيدروجين (E0) مساويا للصفر عند جميع درجات الحرارة.[1] وبناء على ذلك يقارن جهد أي قطب آخر بالجهد القياسي للهيدروجين عند نفس درجة الحرارة.
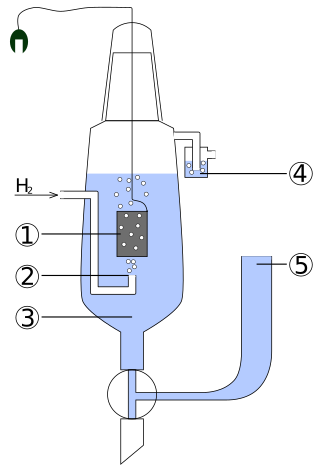
1 – قطب من البلاتين
2 – دخول غاز الهيدروجين
3 – محلول حمضي(H+ = 1 مول/لتر)
4 – مصيدة لمنع الأكسجين من الدخول
5 – خزان
ويعتمد قطب الهيدروجين على تفاعل أكسدة-اختزال لنصف خلية:
- (2H+(aq) + 2e- → H2(g
يحدث هذا تفاعل الأكسدة-اختزال في قطب بلاتين مطلي بالبلاتين شديد النقاوة.
يغمس القطب في محلول حمضي وتطلق خلاله فقاقيع الهيدروجين النقي. ويحافظ على تركيز كل من الهيدروجين وأيوناته في المحلول ليكون مساويا للواحد. هذا معناه أن يكون ضغط غاز الهيدروجين 1 بار وفاعلية أيونات الهيدروجين في المحلول 1 مول. فتكون الفاعلية الكيميائية لأيونات الهيدروجين مساوية لتركيزها الفعلي، حيث التركيز الفعلي هو التركيز الابتدائي مضروبا في معامل الفاعلية. وتكون معاملات الفاعلية قريبة من 1 للمحاليل المائية المخففة جدا، ولكنها تكون أقل من الواحد للمحاليل المركزة.
وتكتب معادلة نرنست كالآتي:
أو
حيث:
- aH+ فاعلية أيونات الهيدروجين،
- aH+=fH+ CH+ /C0
- pH2 الضغط الجزئي لغاز الهيدروجين، باسكال،
- R ثابت الغازات العام
- T درجة الحرارة ب كلفن،
- F ثابت فاراداي (كمية الشحنة الكهربائية ل 1 مول), ويساوي 9.6485309*104 كولوم مول−1
- p0 الضغط القياسي 105 باسكال

