Loading AI tools
مركب كيميائي من ويكيبيديا، الموسوعة الحرة
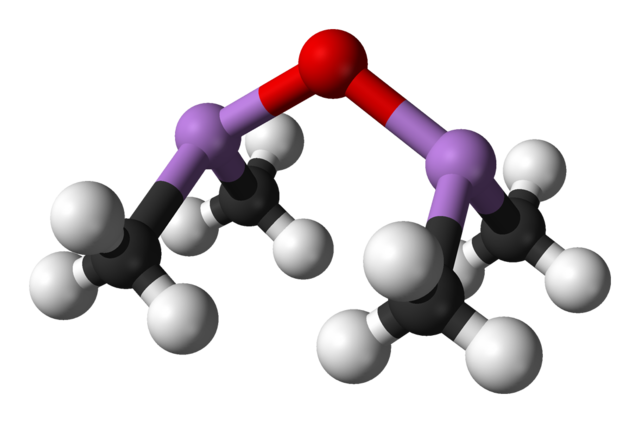
أكسيد الكاكوديل مركب كيميائي من مركبات الزرنيخ العضوية السامة، له الصيغة C4H12As2O، ويشكل مع الكاكوديل مزيجاً ساماً يدعى سائل كاديت.
| أكسيد الكاكوديل | |
|---|---|
| الاسم النظامي (IUPAC) | |
أكسيد الكاكوديل | |
| المعرفات | |
| رقم CAS | 503-80-0 |
| بوب كيم | 10431 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| الخواص | |
| الصيغة الجزيئية | C4H12As2O |
| الكتلة المولية | 255.98 غ/مول |
| المظهر | سائل |
| المخاطر | |
| ترميز المخاطر | |
| توصيف المخاطر | |
| تحذيرات وقائية | |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
يعد لأكسيد الكاكوديل أهمية تاريخية إذ يعد من قبل البعض أول مركب عضوي فلزي حُضر بصورة شبه نقية.[2][3]
يحضر أكسيد الكاكوديل من تفاعل أكسيد الزرنيخ الثلاثي مع خلات البوتاسيوم [4] حسب المعادلة:
As2O3 + 4KC2H3O2 → (CH3)2As-O-As(CH3)2 + 2K2CO3 + CO2
يعد تفاعل تشكل أكسيد الكاكوديل إحدى الوسائل في الكيمياء التحليلية من أجل الكشف عن أنيون الخلات، وذلك نظرا لرائحته المنفرة المميزة.[4] إلا أن هنالك ست أنيونات أخرى تتداخل مع وسيلة الكشف هذه وهي الكبريتيد والطرطرات والثيوسيانات والكلورات والنترات والنتريت. يمكن إزالة الطرطرات من العينة بإضافة هيدروكسيد الكالسيوم أو هيدروكسيد الباريوم حتى تمام الترسيب، ثم بإجراء عملية ترشيح. أما أيونات الكبريتيد والثيوسيانات فتزال من العينة بإضافة كلوريد الزئبق الثنائي. في حين تتم إزالة الكلورات زالنترات والنتريت بإضافة عدة مليغرامات من مسحوق الزنك وبضعة قطرات من حمض الهيدروكلوريك المركز ثم بتسخين العينة، ثم بمعادلتها بعدما تبرد بمحلول هيدروكسيد الصوديوم.
يجب تجنب استنشاق أبخرة أكسيد الكاكوديل لسميتها، لذا يجب اتخاذ إجراءات الوقاية والسلامة المخبرية.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.