آزولين
مركب كيميائي من ويكيبيديا، الموسوعة الحرة
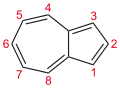
أزولين[3] هو مركب عضوي حلقي وهو مصاوغ للنفثالين وله الصيغة الكيميائية C10H8 ويكون على شكل صلب أزرق اللون.
تحتاج هذه المقالة إلى الاستشهاد بمصادر إضافية لتحسين وثوقيتها. |
| آزولين | |
|---|---|
 |
 |
| التسمية المفضلة للاتحاد الدولي للكيمياء البحتة والتطبيقية | |
Azulene | |
| تسمية الاتحاد الدولي للكيمياء | |
Bicyclo[5.3.0]decapentaene | |
| أسماء أخرى | |
Azulene | |
| المعرفات | |
| رقم التسجيل (CAS) | 275-51-4 |
| بب كيم (PubChem) | 9231 |
| |
| الخواص | |
| الصيغة الجزيئية | C10H8 |
| الكتلة المولية | 128.17 غ/مول |
| المظهر | صلب أزرق |
| نقطة الانصهار | 99 °س |
| نقطة الغليان | 242 °س |
| الذوبانية في الماء | عملياً غير منحل في الماء |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
الوفرة الطبيعية
توجد الآزولينات (مشتقات الآزولين) عادة في الطبيعة على شكل خضاب في أنواع من المشروم وزيت الجياك وبعض أنواع الفقاريات البحرية.
التحضير
يشتق اسم المركب من الاسم الإسباني آزول، والذي يعني أزرق. كان الآزولين يحصل عليه في الماضي كحامل للون الأزرق اللازودي بالتقطير بالبخار، كما عثر عليه في قيصوم ألفي الأوراق والشيح.
هناك عدة طرق لتحضير الآزولين، كان بلاتنر و بفاو أول من تمكن من اصطناعه عضوياً سنة 1939؛[4] وذلك من الإندان وديازوأسيتات الإيثيل.
هناك طريقة ذات كفاءة جيدة وذلك وفق مبدأ اصطناع الإناء الواحد، والتي تتضمن تفاعل تحلق لتشكيل حلقي البنتاديين مع وجود سينثونات خماسية الكربون وغير مشبعة.[5] كما يمكن الانطلاق من حلقي الهبتاتريين كما هو موضح في المثال أدناه:[6]

الخواص
في حين النفثالين عديم اللون فإن الآزولين يكون على شكل أزرق اللون، وكان الكيميائي ليوبولد روزيتشكا أول من وصف بنية الآزولين. ينظر إلى بنية المركب على أنها دمج حلقات من بنيتي حلقي البنتاديين وحلقي الهبتاتريين. يحوي المركب على عشرة إلكترونات باي، وله خواص عطرية. يبلغ عزم ثنائي قطب للمركب 1.08 ديباي.[7]
يمكن أن يخضع المركب لتفاعل فريدل-كرافتس. أثبتت دراسات التفاعلية الكيميائية للمركب أن الحلقة السباعية هي محبة النواة والحلقة الخماسية وهي محبة للنواة.
الاستخدامات
يستخدم الآزولين في الكيمياء العضوية الفلزية كربيطة للمراكز الفلزية قليلة التكافؤ، مثل الحديد والموليبدنوم.[8]
المشتقات

.

هناك عدد من المركبات الكيميائية تعد من مشتقات الآزولين، وتسمى الآزولينات، حيث تحوي على هيكل الآزولين في بنيتها. من هذه المركبات كل من كامآزولين وجيآزولين. من هذه المشتقات أيضاً مركب فيتيفآزولين؛ وهو مركب له بنية الآزولين، حيث يحوي على مجموعتي ميثيل مستبدلتين في الموقعين 4 و 8 بالإضافة إلى مجموعة إيزوبروبيل في الموقع 2؛ ومن هنا التسمية النظامية 4,8-dimethyl-2-isopropylazulene؛ أما التسمية الشائعة فيتيفآزولين فمشتقة من vetiver وهو المقابل الإنجليزي لنبات نجيل الهند، حيث يوجد الفيتيفآزولين في الزيت العطري المستخلص منه.
اقرأ أيضاً
المراجع
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
