
Iontová vazba
chemické vazby zahrnující přitažlivost mezi ionty / From Wikipedia, the free encyclopedia
Iontová vazba (heteropolární vazba nebo elektrovalentní vazba) je forma chemické vazby, která vzniká mezi atomy majícími rozdíl elektronegativit vyšší než je 1,7. V takovém případě atom s vyšší elektronegativitou přitáhne od druhého atomu elektron (více elektronů), který potřebuje k dosažení stabilní elektronové konfigurace a stane se záporným iontem (aniontem). Atom s nižší elektronegativitou se po ztrátě elektronu (více elektronů) stane kladným iontem (kationtem). Atomy jsou pak k sobě vázány především díky elektrostatické přitažlivé síle, která působí mezi částicemi s opačným nábojem.
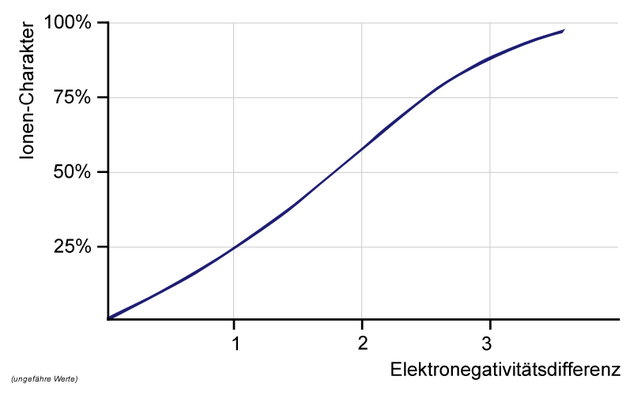

Sloučeniny s iontovou vazbou se nazývají iontové sloučeniny a jejich hlavními představiteli jsou soli. Vznikají především mezi kovy nacházejícími se v 1. a 2. skupině periodické tabulky a nekovy v 6. a 7. skupině. Tyto prvky vytvářejí nejsilnější iontové vazby.
V iontových vazbách je v nejjednodušším případě kationtem atom kovu a aniontem atom nekovu. Ve složitějších případech se ionty mohou skládat z několika atomů a nazývají se pak molekulární ionty (například kationt NH +
4 v amonných solích, aniont SO 2-
4 v síranových solích).
Iontová vazba je (spolu s kovalentní vazbou a kovovou vazbou) hlavním typem chemické vazby. Čistě iontová vazba, při které jeden atom zcela přenáší elektron na druhý, však neexistuje. Všechny iontové sloučeniny mají určitý stupeň kovalentní vazby nebo sdílení elektronů. Termín iontová vazba tedy znamená, že iontový charakter sloučeniny je větší než kovalentní charakter. Vazby s částečně iontovými a částečně kovalentními znaky se nazývají polární kovalentní vazby.